Minerálne soli dávajú kostného tkaniva pevnosť, tuhosť. Zvýšený aj znížený obsah minerálnych solí v kostnom tkanive znižuje jeho pevnostné vlastnosti. U detí nedostatočná mineralizácia kostného tkaniva sťažuje rast tubulárnych kostí, čo vedie k ich zakriveniu. Nedostatočná mineralizácia má zlý vplyv na pevnosť kostí a v dospelosti.
Pri nadmernom obsahu minerálnych solí sa kostné tkanivo stáva krehkým, jeho pevnosť sa výrazne znižuje.
Vo vode rozpustné kyseliny a soli sa v tele nachádzajú v ionizovanej forme. Z katiónov je najvyšší obsah iónov Na +, K +, Ca 2+, Mg 2+, Zn 2+, Fe 3+, Fe 2+. Zn2+, Ni2+, Cr3+, Mn2+, Cd2+, Ba2+, Cu2+, Co2+, Mo2+ a niektoré ďalšie kovové ióny sú obsiahnuté v oveľa menších množstvách. Pre nízky obsah v tele sa tieto ióny nazývajú stopové prvky.
Z aniónov sú najviac zastúpené kyslé zvyšky kyseliny uhličitej, chlorovodíkovej a fosforečnej. Anión kyseliny sírovej je obsiahnutý v oveľa menšom množstve.
Ióny môžu byť vo voľnom aj vo viazanom stave v zložení rôznych zlúčenín tela. Funkcie voľných a viazaných iónov sú rôzne. Ióny určujú osmotický tlak biologických tekutín, vytvárajú elektrický potenciál bunkových membrán, zabezpečujú tvorbu a prenos nervových impulzov, pôsobia ako aktivátory, kofaktory alebo zložky enzýmov a iných biologicky aktívnych zlúčenín.
Zastavme sa podrobnejšie pri obsahu a úlohe jednotlivých iónov v organizme.
vápenaté ióny. Vápnikové ióny sa nachádzajú v krvi aj v bunkách tela. Obsah Ca 2+ v krvi je približne 5,7 mg% (5,7 mg na 100 ml krvi). Je nerovnomerne rozdelený medzi plazmu a tvarované prvky. Erytrocyty ho obsahujú približne 1,0 mg%, leukocyty - asi 4,0-5,0 mg%. V krvnej plazme je koncentrácia vápnika výrazne vyššia.
V bunkách tela je vápnik lokalizovaný hlavne v mitochondriách, sarkoplazmatickom retikule a ribozómoch.
Vápenaté ióny aktivujú fagocytárnu funkciu leukocytov, zvyšujú odolnosť organizmu voči infekciám a intoxikáciám, znižujú priepustnosť kapilár a tým pôsobia protizápalovo a antialergicky. Normalizujú excitabilitu periférneho nervového systému, stimulujú aktivitu sympatického nervového systému. vysoko dôležitá úloha vápenaté ióny hrajú v konjugácii excitácie s kontrakciou v srdcových a kostrových svaloch.
Toto sa neobmedzuje len na úlohu iónov vápnika v tele. Sú súčasťou bunkových membrán, zabezpečujú ich stabilizáciu, podieľajú sa na synaptickom prenose nervových vzruchov, sú regulátormi aktivity mnohých enzýmov. Vápnikové ióny sú potrebné na vykonávanie činnosti mnohých žliaz s vnútornou sekréciou (hypofýza, nadobličky), žliaz zažívacie ústrojenstvo. Aktívne sa podieľajú na procesoch zrážania krvi.
Ióny Na + a K +. Hodnota sodíkových iónov v tele je mimoriadne vysoká. Na + ióny sú hlavné ióny v krvnej plazme a extracelulárnej tekutine. Zohrávajú dôležitú úlohu pri udržiavaní vodnej rovnováhy ľudského tela. Obsah sodíkových iónov v tele určuje objem tekutiny (vody) a akékoľvek narušenie jej metabolizmu okamžite vedie k redistribúcii, zadržiavaniu alebo strate vody.
Koncentrácia sodíkových iónov v tekutých médiách tela je faktorom ovplyvňujúcim aktivitu niektorých enzýmov, najmä enzýmov anaeróbnych premien uhľohydrátov, ako aj enzýmov, ktoré zabezpečujú ukladanie energie v makroergických fosfátových zlúčeninách.
Nedostatok sodíka vedie k množstvu porúch v tele: tkanivá sú dehydratované, krvný obeh je narušený, chuť do jedla sa stráca, duševné schopnosti sa znižujú. Všetky tieto poruchy vo väčšine prípadov nie sú spôsobené nedostatkom soli (hlavný zdroj sodíka a chlóru pre telo) v potrave, ale jej veľkými stratami pri určitých stavoch a ochoreniach: vracanie, hnačka, nadmerné potenie.
Ióny sodíka vykonávajú dôležité funkcie pri udržiavaní acidobázickej rovnováhy v tele. Tento účinok sa prejavuje najmä v obličkách. V obličkových tubuloch sa sodíkové ióny reabsorbujú výmenou za vylučované vodíkové ióny. Tým je zaistené zachovanie stálosti pH pri tvorbe kyslých metabolitov a zachovanie sodíkových iónov v organizme. Táto schopnosť v obličkách je taká vysoká, že pomer koncentrácií vodíkových iónov v moči a krvi môže dosiahnuť až 800:1.
Keďže hlavným zdrojom sodíka pre telo je kuchynská soľ, zvyčajne sa hovorí o potrebe kuchynskej soli, a nie sodíka. U dospelého človeka je potreba kuchynskej soli 4-5 g denne. Zvýšená potreba kuchynskej soli môže súvisieť s niektorými chorobami, ako aj so zvýšeným potením, pri ktorom sa stráca veľa sodíkových iónov. To spôsobuje zvýšenú potrebu soli u športovcov. Obzvlášť vysoká je potreba soli u ľudí, ktorí sa venujú športu, v ktorom sú tréningové a súťažné aktivity spojené s nadmerným potením.
Na rozdiel od sodíka sa ióny draslíka nachádzajú najmä v bunkách orgánov a tkanív. Celkové množstvo draslíka v ľudskom tele s hmotnosťou 70 kg je asi 140 g. Z tohto množstva je len asi 25 g v extracelulárnom priestore. Najvyšší obsah draslíkových iónov v erytrocytoch, svalových vláknach, pečeňových bunkách.
Väčšina intracelulárneho draslíka je spojená s proteínmi, sacharidmi, fosfátmi, kreatínfosfátom. Mnoho procesov syntézy v tele vyžaduje prítomnosť iónov draslíka. Draslík sa teda podieľa na syntéze glykogénu. So zvýšenou glukoneogenézou v pečeni a svaloch sa pozoruje zníženie koncentrácie voľných iónov draslíka. Naopak, pri intenzívnom odbúravaní glykogénu, napríklad pri intenzívnej svalovej práci, koncentrácia voľných iónov draslíka výrazne stúpa.
Väzba iónov draslíka sa pozoruje pri syntéze proteínu, ATP, kreatínfosfátu. Počas syntézy každých 2 g proteínu sa teda viaže približne 1 meq draselných iónov. Pri nedostatku draslíka v tele je syntéza týchto zlúčenín narušená.
Draslík sa aktívne podieľa na prenose nervových vzruchov v synaptických formáciách, podieľa sa na syntéze acetylcholínu, mediátora nervovej excitácie. Spolu s iónmi sodíka sa draslík podieľa na polarizácii bunkovej membrány a excitácii bunky, pri zabezpečovaní svalovej kontrakcie.
Draselné ióny sa podieľajú na regulácii srdcovej činnosti. Srdce je veľmi citlivé na kolísanie koncentrácie draslíka v krvi. Má tiež vazodilatačný účinok.
Ióny horčíka. Celkové množstvo horčíka v ľudskom tele s hmotnosťou 70 kg je asi 14,4 g Najvyšší obsah horčíka v kostnom tkanive, kde je vo forme fosfátových, uhličitanových a fluoridových solí. Kostný popol obsahuje až 1,5 % horčíka. Kostné tkanivo obsahuje určité množstvo vo vode rozpustných solí horčíka, čo vytvára svoj druh telesného depotu. Nedostatok horčíkových solí v kostnom tkanive spôsobuje oneskorenie ich rastu do dĺžky a hrúbky.
Horčík je súčasťou krvi, svalov, pečene, obličiek a iných orgánov a tkanív, kde plní rôzne dôležité funkcie. Je aktivátorom množstva enzýmov: cholínesterázy, fosfoglukomutázy, pyrofosfatázy, arginázy, karboxylázy, črevnej dipeptidázy. Horčík je nevyhnutný pri syntéze acetylcholínu, pri vzniku glykolýzy, pri syntéze bielkovín, tvorbe a rozklade ATP. Podieľa sa na svalovej kontrakcii, regulácii srdcovej činnosti. Početné štúdie preukázali inverzný vzťah medzi úmrtnosťou na srdcové choroby a obsahom ionizovaného horčíka v tele, ako aj v pitnej vode ako hlavného zdroja horčíka pre telo.
Okrem už spomínaných plní horčík v ľudskom tele aj ďalšie funkcie a jeho nedostatok alebo nadbytok môže spôsobiť vážne poruchy. Horčík je teda potrebný na vstrebávanie produktov trávenia v gastrointestinálnom trakte. Nadbytok horčíka však znižuje rýchlosť vstrebávania niektorých z nich, najmä mastných kyselín, v dôsledku tvorby nerozpustných komplexov s nimi.
Nedostatok horčíka vedie k výraznej zmene minerálneho zloženia buniek, k zvýšeniu koncentrácie triglyceridov v krvi, stukovateniu pečene, kalcifikácii ciev a zníženiu ich obsahu elastínu. Nedostatok horčíka spôsobuje nekrózu a ložiská kalcifikácie v myokarde, hyperémiu slizníc očí, nosa, úst, vypadávanie vlasov, kŕče a v konečnom dôsledku môže viesť až k smrti organizmu.
Ióny chlóru. Obsah chlóru v ľudskom tele s hmotnosťou 70 kg je asi 88,7 g. Ióny chlóru sú hlavné anióny v krvnej plazme, tvoria asi 75 % z celkového množstva aniónov v krvi. Podobne ako sodné ióny, aj chloridové ióny sa podieľajú na udržiavaní osmotického tlaku krvnej plazmy a iných biologických tekutín. V tomto ohľade je obsah vody v tele a jednotlivých orgánoch a tkanivách do značnej miery určený koncentráciou chloridových iónov. Nadbytok chloridových iónov je sprevádzaný zvýšeným obsahom vody, nedostatok vedie k strate vody.
Ióny chlóru sa podieľajú na detoxikácii organizmu väzbou toxických produktov látkovej premeny. Najmä sa podieľajú na odstraňovaní amoniaku a vodíkových iónov z tela cez obličky. Časť amoniaku vytvoreného v bunkách tela v procese deaminácie aminokyselín a iných zlúčenín obsahujúcich dusík sa dodáva do obličiek kyselinou glutámovou alebo asparágovou. Tam sa odštiepi z uvedených aminokyselín a spojí sa s iónmi chloridu a vodíka za vzniku chloridu amónneho (NH 4 Cl), ktorý sa z tela vylučuje močom. Zároveň dochádza k naviazaniu a odstráneniu vodíkových iónov z tela, čo zabezpečuje udržanie acidobázickej rovnováhy organizmu. Reakcia prebieha podľa rovnice:
NH3 + H + + Cl¯ → NH4Cl
Chlór sa do organizmu dostáva najmä v kombinácii so sodíkom (ako súčasť kuchynskej soli). Už spomínaná potreba kuchynskej soli uspokojuje potrebu ľudského tela tak po sodíku, ako aj po chlóre.
Mikroelementy. Okrem vyššie uvedeného obsahuje ľudské telo množstvo iónov v malých koncentráciách (nepresahujúcich 0,001%) Patria sem: Fe2+, Zn2+, Mn2+, Mo2+, Co2+, J‾ a niektoré ďalšie. Pre nízky obsah v organizme sa im hovorí stopové prvky. Funkcie stopových prvkov v ľudskom tele sú rôznorodé, hoci úloha niektorých z nich ešte nie je dostatočne preskúmaná. Zastavme sa pri úlohe niektorých stopových prvkov.
Ióny železa sú súčasťou krvného hemoglobínu a myoglobínu obsiahnutého vo svalovom tkanive, iných tkanivách a orgánoch. Ióny Fe 2+ sa podieľajú na dodávaní kyslíka do tkanív, zabezpečujú jeho prechod z krvi do tkanív a ukladanie v nich. Okrem toho je železitý ión súčasťou enzýmov aeróbnej oxidácie (cytochrómy), ako aj katalázy, enzýmu, ktorý rozkladá peroxid vodíka vznikajúci v procesoch biologickej oxidácie.
Intenzívna svalová aktivita je sprevádzaná výrazným zvýšením energetického metabolizmu a následne aj zvýšením odbúravania zlúčenín obsahujúcich železo podieľajúcich sa na jeho poskytovaní, zvýšením metabolizmu železa vo všeobecnosti. Zároveň je stupeň absorpcie železa z potravy veľmi nízky. Výsledkom je, že v období intenzívneho tréningu sa môžu vyskytnúť stavy nedostatku železa v tele a potreba používať prípravky obsahujúce zlúčeniny železa ako ďalšie nutričné faktory.
Ióny zinku sú súčasťou množstva enzýmov zapojených do syntéznych reakcií a katabolických procesov. Sú nevyhnutné pre procesy prenosu genetickej informácie v bunke, pre syntézu hemoglobínu. Ióny zinku sa podieľajú na stabilizácii štruktúry niektorých makromolekúl, procesoch rastu tela, činnosti imunitného systému, procesov hojenia rán, vývoja mozgu plodu a stimulujú hormonálnu funkciu pankreasu.
Mangánové ióny sa podieľajú na metabolizme glukózaminoglykánov, ktoré sú súčasťou spojivového tkaniva, glukózy, glykogénu a lipidov. Hrajú obzvlášť dôležitú úlohu v metabolizme v mozgu. Pri nedostatku mangánu je narušený metabolizmus v spojivovom tkanive, mozgu, znižuje sa rýchlosť syntézy glykogénu.
Mechanizmus účinku mangánových iónov nie je zatiaľ v mnohých ohľadoch jasný, zatiaľ bola jasne preukázaná len jeho úloha ako kofaktora množstva enzýmov, najmä glykozyltransferáz.
Kobalt sa podieľa na erytropoéze (syntéze hemoglobínu) a regulácii metabolizmu železa v tele. Hrá dôležitú úlohu pri regulácii krvných lipidov a niektorých metabolických reakcií prebiehajúcich v srdci, nervovom tkanive a stenách gastrointestinálneho traktu.
Ióny medi, niklu, chrómu a ďalších stopových prvkov plnia v organizme dôležité funkcie. Meď sa teda podieľa na tvorbe flavoproteínov a cytochrómoxidázy - enzýmov energetického metabolizmu, má aktivačný účinok na glykolýzu. Niektoré stopové prvky sú neoddeliteľnou súčasťou nielen enzýmov, ale aj hormónov. Jód je teda štrukturálnou zložkou hormónov štítnej žľazy: tyroxínu a trijódtyronínu.
Horčík je jedným z najdôležitejších a nenahraditeľných stopových prvkov pre ľudský organizmus. A počas obdobia nosenia dieťaťa sa jeho potreba niekoľkokrát zvyšuje. Je to dôležité pre normálne fungovanie tela matky a úspešné tehotenstvo, ako aj pre normálny rast a vývoj dieťaťa.
Tento stopový prvok sa podieľa na mnohých metabolických procesoch, prispieva k normálnemu fungovaniu svalového, kostného, nervového a imunitného systému. To je dôvod, prečo jeho nedostatok pre tehotnú ženu môže hroziť s vážnymi následkami.
Aká je úloha horčíka?
Horčík sa podieľa na mnohých metabolických procesoch v tele. Pomáha normalizovať proces prenosu nervových vzruchov vo svalovom tkanive, uvoľňuje svaly, znižuje ich nadmerný tonus a upokojuje nervový systém.
Často je žene predpísaný dodatočný príjem horčíka v štádiu prípravy na počatie. Je dokázané, že horčík podporuje a reguluje proces prenosu genetického materiálu rodičov na dieťa. Mg 2+ ión sa podieľa na syntéze štruktúrnych zložiek DNA.
Tento mikroelement sa tiež aktívne podieľa na syntéze bielkovín, ktoré sú priamo stavebným materiálom pre vnútorné orgány a systémy dieťaťa.
Horčík sa tiež podieľa na plnohodnotnom fungovaní placenty počas tehotenstva, pričom prostredníctvom neho reguluje metabolizmus medzi organizmami matky a dieťaťa.
Prečo je nedostatok horčíka nebezpečný pre tehotné ženy?
Nedostatok horčíka (hypomagnezémia) môže vyvolať tvorbu defektov v drobkoch prenatálny vývoj muskuloskeletálny systém alebo srdce. Nedostatok horčíka môže viesť k predčasnému pôrodu alebo hroziacemu potratu.
Na neskoršie dátumy a pri porode je magnezium pre tehotnu rovnako dolezite ako cele tehotenstvo. Nedostatok tohto mikroelementu vedie k zníženiu elasticity svalových vlákien a narušeniu ich kontraktility, čo môže prispieť k narušeniu pracovnej aktivity (slabosť, diskoordinácia pracovnej aktivity). V dôsledku toho sa zvyšuje riziko traumy a pretrhnutia pôrodných ciest matky.
Potreba horčíka počas tehotenstva sa zvyšuje asi o 30%. Teraz to predsa potrebujú dva organizmy – matka a dieťa.
Doplnenie nedostatku akýchkoľvek látok potrebných pre dieťa počas obdobia tehotenstvo sa blíži zo zásob tela matky. Preto je jasné, že nastávajúca mamička môže mať niekedy zjavné známky nedostatku stopových prvkov.
Ak sa do tela nedostane dostatok horčíka s jedlom, potom si ho telo berie z kostí, zubov a žliaz s vnútornou sekréciou. Snaží sa teda kompenzovať počiatočný pokles hladiny horčíka v krvnej plazme.
Preto je to také dôležité nastávajúca matka predchádzať stavom s nedostatkom horčíka v ktorejkoľvek fáze – od plánovania tehotenstva až po samotný pôrod.
Ako zistiť nedostatok horčíka v tele?
Príznaky pozorované u tehotných žien s nedostatkom horčíka:
OD svalový kŕč
Často s nedostatkom horčíka sa budúca matka obáva bolesti v dolnej časti chrbta a dolných končatín. Existuje svalová stuhnutosť a nepohodlie na krku.
Nedostatok horčíka sa prejavuje aj napätím (sťahom) svalov maternice. Ženy opisujú tento stav ako „tuhne žalúdok“, „žalúdok sa mimovoľne napína“. V tomto prípade dochádza k kŕčovitému ťahaniu bolesti v dolnej časti brucha. Takýto zvýšený tonus maternice môže viesť k ukončeniu tehotenstva.
Ďalším prejavom narušenej svalovej kontrakcie pri nedostatku horčíka sú kŕče lýtkových svalov. Prudká, pretrvávajúca, veľmi bolestivá kontrakcia lýtkových svalov nastáva hlavne v noci. Stav je dosť nepríjemný, bolestivý.
Musíte pochopiť, že kŕče v dolných končatinách môžu naznačovať nielen nedostatok horčíka, ale aj nedostatok vápnika v tele tehotnej ženy.
Zmeny v nervovom systéme
Počas tehotenstva sa psycho-emocionálny stav každej ženy mení. Existujú obavy o zdravie dieťaťa a ich vlastné blaho. A s nedostatkom horčíka sa výrazne zvyšuje závažnosť nervozity, bezdôvodná podráždenosť, poruchy spánku, emočná labilita, plačlivosť a znížená výkonnosť.
Zmeny v kardiovaskulárnom systéme
Nedostatok horčíka sa prejavuje zvýšením krvný tlak. Zároveň sa k vysokému tlaku pripájajú závraty a bolesť hlavy. Na pozadí zvýšeného tlaku dochádza k narušeniu venózneho odtoku z dolných končatín, čo sa prejavuje opuchmi nôh.
Pri výraznom nedostatku horčíkových iónov môže byť srdcové vedenie narušené s rozvojom arytmií a výskytom bolesti v oblasti srdca.
Pokles hladiny horčíka v krvnom sére pod 0,7 mmol / l naznačuje nedostatok tohto stopového prvku. V tomto stave je narušená výmena elektrolytov (sodík, draslík, horčík) pri kontrakcii srdcového svalu (myokardu).
Pri nedostatku horčíka v tele je narušená aj relaxácia svalovej steny ciev. Výsledkom je, že v dôsledku neustáleho mierneho vazospazmu je prietok krvi do posledných častí tela menší ako zvyčajne. Ľudia s nedostatkom horčíka sa preto stávajú citlivejšími na chlad, prechladnú aj v lete.
Zmeny v tráviacom systéme
Nedostatok horčíka vyvoláva porušenie kontraktility čreva, to znamená jeho peristaltiku. Preto sú zápcha a plynatosť častými spoločníkmi takéhoto nedostatočného stavu.
Vlastnosti výživy s nedostatkom horčíka
Horčík sa vstrebáva z potravy v čreve, najmä v jeho tenkej, ale čiastočne aj v hrubej časti. Ale, bohužiaľ, iba 35% horčíka sa absorbuje z potravín cez tráviaci trakt.
Čo možno urobiť, aby sa vstrebalo viac ako 35 % horčíka? Jeho vstrebávanie zlepšuje vitamín B 6 a niektoré organické kyseliny (mliečna, citrónová, asparágová).
Dôležité je aj to, v akej forme sa horčík do tela dostane. Takže jeho organické zlúčeniny, napríklad citrát horečnatý (zlúčenina horčíka s kyselinou citrónovou), laktát horečnatý (zlúčenina horčíka s kyselinou mliečnou), sa dobre vstrebávajú cez črevá. ALE anorganické soli prakticky sa neabsorbuje, napríklad síran horečnatý.
Aby sa predišlo nedostatku horčíka u tehotnej ženy, je potrebné zaradiť do stravy potraviny bohaté na horčík. Patria sem: petržlen, kôpor, orechy, strukoviny, ryby a morské plody, ovsené vločky a pohánka, melón, vaječný žĺtok, sójové bôby, otruby, banány, fenikel, celozrnný chlieb.

Veľa horčíka sa nachádza vo všetkých zelených rastlinných potravinách. Zelená farba Dodáva rastlinám chlorofyl. Ide o špeciálnu látku, komplexný proteín, vďaka ktorému rastliny vykonávajú veľmi dôležitý proces fotosyntézy.
Chemická štruktúra chlorofylu je podobná štruktúre ľudského krvného proteínu hemoglobínu. Iba hemoglobín obsahuje ióny železa a chlorofyl obsahuje ióny horčíka. Jedzte preto viac zelenej zeleniny a ovocia. Sú to najdôležitejšie zdroje horčíka pre ľudský organizmus.
No najbohatšie na obsah horčíka stále nie sú zelené potraviny. Nižšie je uvedená tabuľka potravinových lídrov z hľadiska obsahu horčíka na 100 g produktu. Pozrite sa, ktorý z týchto produktov je pre vás najvhodnejší na doplnenie zásob horčíka v tele.
| Názov produktu | Obsah horčíka, mg/100 g jedlej časti výrobku |
|---|---|
| Tekvicové semiačka | 534 |
| pšeničné otruby | 448 |
| Kakao 20% | 442 |
| Sezam (pražené semienka) | 356 |
| Kešu (surové) | 292 |
| Mandle (pražené) | 286 |
| píniové oriešky | 251 |
| Sója (suchá fazuľa) | 240 |
| Pšeničné klíčky, surové | 239 |
| Pohánka (surová) | 231 |
| Vodný melón | 224 |
| Kukuričné lupienky | 214 |
| Obilniny | 130 |
| Slnečnicové semienka (pražené) | 129 |
| Hrášok olúpaný | 128 |
| šípky (suché) | 120 |
| orech | 100 |
Teraz sa pozrite, aké faktory zasahujú do vstrebávania horčíka alebo prispievajú k vyčerpaniu jeho zásob v tele.
- kofeínové nápoje;
- monotónna strava s nadbytkom ľahko stráviteľných sacharidov a sladkostí;
- sladké limonády;
- alkohol, fajčenie;
- chronická bolesť alebo stres;
- endokrinné ochorenia: hypotyreóza, diabetes mellitus;
- choroby sprevádzané zvýšeným potením;
- užívanie určitých liekov (diuretiká, antikonvulzíva, vápenaté soli).
Denná potreba horčíka počas tehotenstva a dojčenia
Údaje o dennej potrebe horčíka pre tehotné a dojčiace ženy v rôzne zdroje sú rôzne. Odborníci na výživu a vedci zatiaľ nedospeli ku konsenzu.
Nižšie je porovnávacia tabuľka zvýšená potreba horčíka s prihliadnutím na vek ženy. Toto sú čísla, ktorých sa drží najväčší počet špecialistov.
Kedy je magnézium predpísané tehotnej žene?
Nedostatok horčíka sa dá zistiť pomocou biochemického krvného testu.
- so stredne ťažkým nedostatkom horčíka: 12 - 17 mg / l (0,5 - 0,7 mmol / l);
- so závažným nedostatkom horčíka: pod 12 mg/l (0,5 mmol/l).
Prípravky s horčíkom sú indikované pri nedostatku horčíka zistenom klinickými testami, ako aj pri výskyte príznakov nedostatku horčíka popísaných vyššie (podráždenosť, plačlivosť, zlý spánok, únava, svalové kŕče atď.).
Dodatočný príjem magnéziových prípravkov je priamo indikovaný pri hypertonicite maternice. Tento stav sa často vyvíja v prvom trimestri tehotenstva a zvyšuje riziko potratu v počiatočných štádiách.Stáva sa, že liečba je predpísaná na celé obdobie nosenia dieťaťa.
Prípravky s horčíkom môže lekár predpísať ako v štádiu plánovania tehotenstva, tak aj počas tehotenstva v rôznych obdobiach.
Výber horčíkového prípravku, stanovenie jeho dávky, dávkovej formy a trvania liečby vykonáva v každom prípade iba lekár individuálne.
Najčastejšie lekár tehotným ženám predpisuje horčík vo forme lieku Magne B 6. Nižšie je uvedený popis tohto lieku.
Použitie Magne B 6 u tehotných žien
Účinnými látkami Magne B 6 sú dihydrát laktátu horečnatého a pyridoxín hydrochlorid (aktívna forma vitamínu B 6). Pyridoxín zlepšuje vstrebávanie horčíka, podporuje jeho vstup do buniek tela.
Vyrábajú sa dve verzie lieku: Magne B 6 a Magne B 6 forte. Počas tehotenstva je povolené mať ktorúkoľvek z týchto foriem. Rozdiel medzi nimi spočíva v koncentrácii účinných látok.
V Magna B 6 forte je množstvo účinnej látky dvojnásobné. Tiež vďaka obsahu rôznych pomocných látok sa dosiahla vysoká biologická dostupnosť (schopnosť vstrebať sa v organizme). Stupeň absorpcie Magne B 6 forte je asi 90 %, zatiaľ čo biologická dostupnosť Magne B6 je blízka 50 %.
Existujú rôzne formy uvoľňovania liečiva: poťahované tablety biela farba, ampulky s roztokom na perorálne podanie a ampulky na injekciu (roztok na intramuskulárne alebo intravenózne podanie). Roztok je dostupný v ampulkách z tónovaného skla. V balení 10 ampuliek. Samotné riešenie má Hnedá farba a vôňa karamelu.
Pridelené Magne B 6 6-8 tabliet o deň. Spravidla sa odporúča užívať 2 tablety trikrát denne s jedlom. Liek v ampulkách na perorálne podanie sa užíva 2-4 ampulky denne. Táto forma vyžaduje predbežné zriedenie lieku v 200 mililitroch vody.
Kontraindikácie a vedľajšie účinky Magne B 6
Magne B 6 je kontraindikovaný pri:
- Precitlivenosť na liečivo a jeho zložky.
- Zlyhanie obličiek.
- Intolerancia fruktózy, malabsorpcia glukózy a galaktózy.
- Fenylketonúria, keď je narušený metabolizmus niektorých aminokyselín.
- Deti mladšie ako 1 rok.
- Dojčenie.
Magne B 6 je všeobecne dobre tolerovaný. Pokyny pre liek však zahŕňajú nasledujúce možné vedľajšie účinky:
- bolesť brucha;
- poruchy stolice vo forme hnačky;
- alergické reakcie vo forme urtikárie, Quinckeho edému.
Ak sa tieto príznaky objavia počas užívania lieku, mali by ste sa okamžite poradiť s lekárom.
Je dlhodobé dopĺňanie horčíka bezpečné?
Dlhý priebeh terapeutických dávok predpísaných lekárom pri normálnej funkcii obličiek nemôže viesť k predávkovaniu liekom. K absorpcii horčíka a jeho vstupu do krvi dochádza postupne. Liečivo sa vylučuje obličkami. Preto sa zdravé obličky dokážu vyrovnať s metabolickými produktmi lieku a jeho nadbytkom.
Prípravky horčíka prenikajú do materské mlieko. Preto sa dojčiacim matkám neodporúča užívať tento liek.
Pri predpisovaní doplnkov horčíka nezabudnite povedať svojmu lekárovi o užívaní ďalších multivitamínových komplexov alebo iných liekov (vápnik, železo). Lekár musí vypočítať potrebnú dávku horčíka s prihliadnutím na obsah tohto stopového prvku vo vašom komplexe.
Je to dôležité aj preto, že horčík a vápnik sú antagonistami (konkurentmi) v tele a vzájomne si narúšajú vstrebávanie. Ich príjem by mal byť rozdelený podľa času. Tiež nemôžete užívať horčík a železo súčasne, pretože to znižuje absorpciu každého z nich.
Napriek tomu, že prípravky s horčíkom sú považované za bezpečné, nikdy by ste si ich nemali predpisovať sami. Len lekár môže vypočítať dávku lieku a priebeh liečby, ktorý potrebujete.
Úloha v živote rastlín
Obsah horčíka v rastlinách je v priemere 0,07 % (hmotn.). Podieľa sa na grandióznom diele - akumulácii slnečnej energie v procese fotosyntézy, ktorá je centrálnym atómom v molekule chlorofylu. Chlorofyl absorbuje slnečnú energiu a s jej pomocou premieňa oxid uhličitý a vodu na zložité organické látky: cukry, škrob atď. Horčík je základnou zložkou ribozómov: za jeho účasti (spolu s ATP) sa aminokyseliny pri biosyntéze bielkovín viažu na tRNA . Ióny horčíka Mg 2+ „zosieťujú“ proteínové molekuly do glomerulov, pričom zachovávajú štruktúru proteínových molekúl. Horčík katalyzuje syntézu ATP z nukleozidových difosfátov, aktivuje enzýmové systémy na premenu kyseliny jablčnej na kyselinu citrónovú a kyseliny šťaveľovej na kyselinu mravčiu a oxid uhličitý.
Pri nedostatku horčíka klesá úroda pestovaných rastlín, narúša sa tvorba chloroplastov a chlorofylu: listy (predovšetkým spodné) sa „mramorujú“: blednú medzi žilami a zostávajú zelené pozdĺž žíl. Tkanivá medzi žilami môžu získať inú farbu - žltú, oranžovú, červenú, fialovú, potom odumierajú, začínajúc od okrajov listov: listy sa krútia a postupne opadávajú. V borovici sa pozoruje žltnutie špičiek ihiel.
Rastlinným indikátorom vysokého obsahu horčíka je kostenets.
Živočíšne telo obsahuje približne 0,03–0,07 % horčíka (hmotn.), je súčasťou kostí a zubov, nachádza sa v pečeni, krvi, nervovom tkanive a mozgu a podieľa sa na metabolizme bielkovín a sacharidov. Pri človeku s hmotnosťou 70 kg obsahuje telo 19–20 g horčíka. Pôsobí antisepticky a vazodilatačne, znižuje krvný tlak a cholesterol v krvi, zosilňuje procesy inhibície v mozgovej kôre, má upokojujúci (sedatívny) účinok na nervový systém, hrá dôležitú úlohu pri aktivácii obranné sily telo v boji proti rakovine. Horčík posilňuje imunitný systém, pôsobí antiarytmicky, podporuje regeneráciu po fyzickej námahe.

Pri nedostatku Mg sa zvyšuje náchylnosť na infarkty. Ukázali to experimenty maďarských vedcov uskutočnené v 20. storočí. na zvieratách (u zvierat sa toto ochorenie nazýva bylinná tetánia). Niektorí psi dostali jedlo bohaté na horečnaté soli, iné - chudobné. Na konci experimentu tí psi, ktorých strava mala nízky obsah horčíka, „zarobili“ na infarkt myokardu.
Horčík sa z tela vylučuje močom, výkalmi a potom.
Rastlinné produkty: ovocie, orechy (mandle, arašidy, vlašské orechy), zelenina (paradajky, zemiaky, tekvica, fazuľa, šalát), mäta, čakanka, olivy, petržlen, celozrnná pšenica, ovos, pohánka; ražný chlieb, proso, otruby. Živočíšne produkty: pečeň, vaječný žĺtok.

MgS04- síran horečnatý, horká alebo Epsomská soľ.
MgCO3– uhličitan horečnatý, magnezit.
MgO- oxid horečnatý, spálená magnézia.
Kremičitany horečnaté: mastenec 3 MgO X 4 Si02 X H20 a azbest Cao X 3 MgO X 4 Si02.
Chlorofyl.
Vieš to…
Horčík prvýkrát získal v roku 1808 anglický chemik G. Davy z vlhkého oxidu MgO. Názov pochádza z lat. magnesia alba(biela magnézia), podľa minerálu hydromagnezit, ktorý tento kov obsahuje a našli ho už starí Gréci pri meste Magnesia.

Počet atómov horčíka v ľudskom tele je 8,7 x 1023 a v jednej bunke - 8,7 x 109.
Celkové množstvo horčíka v chlorofyle všetkých rastlín na Zemi je asi 100 miliárd ton.
Denný príjem horčíka s jedlom v tele by mal byť 240-720 mg.
Síran horečnatý MgS04 (horká alebo Epsomská soľ) sa používa v medicíne ako laxatívum, choleretikum a analgetikum.
Ióny horčíka nielen dodávajú morskej vode slanú chuť, ale tiež ju robia nepitnou, čo spôsobuje silné hnačky a zvracanie.
Existuje niekoľko typov chlorofylu (chlorofyl a B C d), ktoré sa líšia svojou štruktúrou a absorpčnými spektrami. Vyššie rastliny a riasy obsahujú ako hlavný pigment chlorofyl. a, a ako dodatočný - chlorofyl b, rozsievky a hnedé riasy - iba chlorofyl c, a červené riasy - chlorofyl d.
Železo

Úloha v živote rastlín a mikroorganizmov
Pri jeho nedostatku sa spomaľuje tvorba chlorofylu. Možno vzhľad chlorózy (žltá farba) na prvom mieste mladých listov, ich strata farby. Pri dlhodobom nedostatku železa v bylinkách odumiera pletivo pozdĺž okrajov listovej čepele, na stromoch odumierajú výhonky a znižuje sa celková produktivita a odolnosť rastlín voči chorobám.
Palina a niektoré ďalšie rastliny sú indikátormi vysokého obsahu železa v pôde. Listy paliny zároveň zožltnú a kvety niektorých rastlín, ako sú hortenzie, získajú nezvyčajnú modrú farbu.
V prírode existujú takzvané železité baktérie. V procese chemosyntézy oxidujú železité železo na železité železo, ktoré sa ukladá na povrchu bunky. Vzniknutý hydroxid železitý sa vyzráža a tvorí takzvanú močiarnu rudu:
4FeCO 3 + O 2 + 6H 2 O ––> 4Fe(OH) 3 + 4CO 2 + energia
Chemosyntetické baktérie, ktoré oxidujú zlúčeniny železa a mangánu, objavil akademik S.N. Vinogradského. Sú mimoriadne rozšírené v sladkých aj morských vodách. Vďaka ich životne dôležitej činnosti sa na dne močiarov a morí vytvára obrovské množstvo ložísk železných a mangánových rúd. IN AND. Vernadsky, zakladateľ biogeochémie, hovoril o ložiskách takýchto rúd ako o výsledku životne dôležitej činnosti baktérií v starovekých geologických obdobiach.
Úloha v živote zvierat a ľudí
Telo zvieraťa obsahuje približne 0,01 % železa (hmotn.). Železo je nevyhnutné v procesoch hematopoézy a vnútrobunkového metabolizmu. Približne 55 % železa je súčasťou hemoglobínu erytrocytov, asi 24 % sa podieľa na tvorbe farbiva svalov (myoglobín), približne 21 % sa ukladá „v rezerve“ v pečeni a slezine.

Práve železo určuje farbu krvi, ako aj jej schopnosť viazať a uvoľňovať kyslík. Červené krvinky prenášajú kyslík z pľúc do celého tela a odstraňujú oxid uhličitý. Kyslík je silné oxidačné činidlo, no hemoglobín je vďaka železu, ktoré obsahuje, schopný prenášať kyslík. Ľudské telo obsahuje enzýmy obsahujúce železo. Existuje aj feritínový proteínový komplex, z ktorého sa tvoria všetky ostatné pre telo potrebné látky obsahujúce železo. Železité ióny sa v tele prenášajú pomocou komplexného proteínu transferínu (nachádza sa v krvnej plazme, mlieku, vaječnom bielku). Železo hrá dôležitú úlohu v procesoch uvoľňovania energie, v enzymatických reakciách, pri zabezpečovaní imunitných funkcií, v metabolizme cholesterolu.
Pri človeku s hmotnosťou 70 kg obsahuje telo 4,2–5 g železa. Denná potreba železa dospelého zdravého človeka je 10–20 mg a dopĺňa sa normálnou vyváženou stravou.
S poklesom množstva železa v krvi dochádza k anémii. Najbežnejšia je anémia z nedostatku železa alebo, ako sa to dlho nazývalo, anémia.

Železo sa z tela vylučuje močom, výkalmi a potom.
Hlavné zdroje vstupu do tela
Zelená zelenina: cibuľa, vňať mladej repy, reďkovka, horčica, mrkva, žerucha, šťaveľ, zelený hrášok, paradajky (iba surové), kapusta, cesnak, šošovica, chren, uhorky. Ovocie a bobule: jablká, granátové jablko, maliny, jahody, čerešne, hrušky, hrozno, melón, akékoľvek sušené ovocie. Živočíšne produkty: pečeň, obličky, vaječný žĺtok.
Najbežnejšie pripojenia
Hemoglobín.
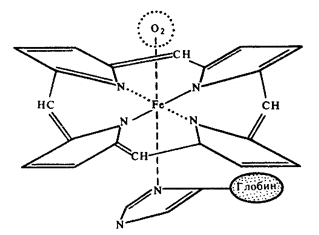
Schematický diagram väzby hem-globín v molekule hemoglobínu
Vieš to…
O oboznámení starovekého človeka so železom kozmického pôvodu svedčí, že obyvatelia Grónska, ktorí o železnej rude nemali ani potuchy, mali výrobky zo železa. Mnohé meteority pozostávajú z prírodného železa s prímesou niklu až do 5,5 %. Alchymisti označovali železo vo forme oštepu a štítu - charakteristické atribúty boha vojny Marsa. Odtiaľ pochádza jeho názov z lat. ferro- meč.
Počet atómov železa v ľudskom tele je 4,5 x 1022 a v jednej bunke - 4,5 x 108.
100 ml ľudskej krvi obsahuje 13–16 g hemoglobínu.
„Zostavenie“ molekuly hemoglobínu v ľudskom tele trvá približne 90 sekúnd a každú sekundu sa vytvorí 650 x 1012 molekúl hemoglobínu.
Mnohé živé objekty sa vyznačujú fenoménom biomagnetizmu. Ich orientácia v magnetickom poli Zeme sa uskutočňuje pomocou oxidu železa, ktorý sa nachádza v špeciálnych formáciách - magnetozómoch, vytvorených vo forme reťazcov 10–25 kryštálov s celkovou dĺžkou asi 50 nm.
Soli železnatého a trojmocného železa sa používajú na kompenzáciu nedostatku železa pri liečbe anémie.
Bola stanovená korelácia medzi zvýšeným obsahom železa v tele a skorý vývoj ateroskleróza, ischemická choroba, nádory.

Železný vitriol FeSO 4 x 7H 2 O (železitý kryštalický hydrát) sa používa na ničenie škodcov rastlín a na prípravu minerálnych farieb. Chlorid železitý (III) FeCl 3 sa používa ako moridlo pri farbení tkanín.
Zinok

Úloha v živote rastlín, húb
Zinok je dôležitý mikroelement, jeho obsah v rastlinách je v priemere 0,003 % (hmotn.). Aktivuje 30 enzýmových systémov v bunke. Na zinok sú bohaté huby (najmä jedovaté), lišajníky, ihličnany. V rastlinách spolu s účasťou na dýchaní, metabolizme bielkovín a jadier zinok reguluje rast, ovplyvňuje tvorbu aminokyseliny tryptofán a zvyšuje obsah giberelínov. Zinok je nevyhnutný pre vývoj vajíčka a plodu. Zvyšuje odolnosť rastlín voči suchu, teplu a chladu.
Jeho nedostatok vedie k narušeniu bunkového delenia (škvrnitosť listov u citrusových plodov), na rastlinách sa tvoria úzke listy stočené do špirály. Tkanivo medzi žilami sa zmení na farbu a vyniknú s jasnou zelenou sieťkou.
Nadbytok zinku je pre rastliny škodlivý, pretože. môže spôsobiť deformáciu orgánov: v maku sa kvety zdvojnásobia a v yarutke sa okvetné lístky veľmi zväčšia. V iných rastlinách je možná chloróza listov, ktorá sa šíri od vrcholu k spodnej časti listu. Rastliny-indikátory zvýšeného obsahu zinku v pôde sú fialová trojfarebná, praslička roľná, macešky.
Úloha v živote zvierat a ľudí
Obsah zinku v tele zvieraťa je približne 0,01 % (hmotn.). Niektoré morské bezstavovce, ako napríklad ustrice, obsahujú 0,4 % zinku (hmotnostných). Pomerne veľa zinku v hadom jede (na ochranu pred účinkami vlastného jedu). U zvierat Zn okrem účasti na dýchaní a metabolizme jadier zvyšuje činnosť pohlavných žliaz, ovplyvňuje tvorbu kostry plodu. Pri nedostatku zinku klesá obsah RNA a znižuje sa syntéza bielkovín v mozgu, spomaľuje sa vývoj mozgu.
Pri človeku s hmotnosťou 70 kg obsahuje telo až 3 g zinku. Je súčasťou najdôležitejších enzýmov: karboanhydráza (urýchľuje uvoľňovanie oxidu uhličitého v pľúcach), rôzne dehydrogenázy, fosfatázy (spojené s dýchaním a inými fyziologickými procesmi), proteázy a peptidázy zapojené do metabolizmu bielkovín, enzýmy metabolizmu jadier ( RNA a DNA polymerázy). Zinok hrá zásadnú úlohu pri syntéze molekúl mRNA na zodpovedajúcich úsekoch DNA (transkripcia), pri stabilizácii štruktúr ribozómov a biopolymérov (RNA, DNA, niektoré proteíny). Zinok je nevyhnutnou súčasťou krvných enzýmov. Je nevyhnutný pre udržanie normálneho rastu pokožky, vlasov a nechtov a hojenie rán, keďže sa podieľa na syntéze bielkovín. Zinok je súčasťou inzulínu, hormónu pankreasu, ktorý reguluje hladinu cukru v krvi, a hormónu týmusu. Zinok zohráva dôležitú úlohu pri spracovávaní alkoholu organizmom, preto nedostatok zinku môže zvýšiť predispozíciu k alkoholizmu (najmä u detí a dospievajúcich). Pre lepšie vstrebávanie zinku organizmom sú potrebné vitamíny A a B 6.

Nedostatok Zn vedie k nanizmu, oneskorenému sexuálnemu vývoju.
Nadbytok zinku má negatívny vplyv na funkcie srdca a krvi. Nie je náhoda, že obsah zinku v potravinách je regulovaný podľa MPC: detská a diétna strava - 5,0 mg/kg; rastlinný olej - 10,0 mg / kg; sójový proteín - 60,0 mg / kg.
V bunkách a jednotlivých orgánoch sa pri ich malígnej premene zvyšuje obsah určitých kovových iónov. Koncentrácia zinku sa niekoľkonásobne zvyšuje. Dôvody zatiaľ nie sú známe, ale špekuluje sa, že by to mohlo slúžiť skorá diagnóza rakovina.
Zinok sa vylučuje z tela močom, výkalmi, potom.

Hlavné zdroje vstupu do tela
Rastlinné produkty: zelenina, kukurica, orechy, pekárenské výrobky. Huby. Živočíšne produkty: hovädzie mäso, pečeň, mäso, mlieko; morské plody (ustrice, mušle, sleď).
Najbežnejšie pripojenia
ZnS- sulfid zinočnatý, zmes zinku.
ZnSO 4 X 7H20- hydrosíran zinočnatý, vitriol zinočnatý.
ZnCl2- chlorid zinočnatý.
Vieš to...
Predpokladá sa, že zinkové rudy sú ľuďom známe už od staroveku. V II storočí pred naším letopočtom. Už Gréci vedeli taviť mosadz – zliatinu zinku a medi. v Indii v 12. storočí. existovala výroba kovového zinku, no v Európe sa objavil oveľa neskôr. Saský hutník I. Genkel opísal zinok ako kov a v roku 1746 nemecký chemik A. Marggraf vyvinul metódy získavania zinku z minerálov kalamín a sfalerit ZnS (zinková zmes). Názov pochádza od neho. zinok- biely kov.
Počet atómov zinku v ľudskom tele je 2,2 x 1022 a v jednej bunke - 2,2 x 108.
Denný príjem zinku v tele s jedlom je 13 mg.
Existuje viac ako 200 enzýmov obsahujúcich zinok.
Suspenzia, ktorá obsahuje inzulín, protamín a chlorid zinočnatý, je účinným antidiabetikom, ktorý účinkuje lepšie ako čistý inzulín.
V modernej medicíne sa zlúčeniny zinku používajú pri liečbe rôznych imunodeficiencií, neplodnosti, ochorení kože, vlasov, nechtov a pečene. Vo forme roztoku sa ako kauterizačný prostriedok používa chlorid zinočnatý ZnCl 2, zinková masť ZnO ako vysušujúci, adstringentný a dezinfekčný prostriedok pri kožných ochoreniach, síran zinočnatý ZnSO 4 x 7H 2 O je súčasťou očných kvapiek.
Zlúčeniny zinku prispievajú k prevencii prechladnutia u detí, zlepšujú chuť do jedla, rast, vývoj, zvyšujú koncentráciu.
Pokračovanie nabudúce
Všetko to začalo fotosyntézou. Je zvláštne poznamenať, že dôležitosť horčíka pre naše telo a dôsledky jeho nedostatku sa začali posudzovať v rovnakom čase, keď boli objavené tajomstvá fotosyntézy rastlín - len pred niekoľkými desaťročiami.
Proces nepretržitej tvorby organickej hmoty sa začal pred miliardami rokov, keď sa na Zemi objavili pigmenty spôsobujúce chemické reakcie absorbovaním slnečného žiarenia. Rozhodujúcu úlohu v tom zohrali „fotosenzitívne“ látky zo skupiny tvorenej z jednoduchých zlúčenín – a glycerol. Avšak až s objavením sa horčíkového derivátu porfyrínu vo forme chlorofylu prírodná história vyšších foriem organického života. Chlorofyl má schopnosť uskutočniť ireverzibilnú fotochemickú reakciu, ktorej energia sa akumuluje v stabilných biochemických zlúčeninách.
Proces fotosyntézy sa formoval pravdepodobne na konci predkambrického obdobia (asi pred 1000 miliónmi rokov). Štruktúra chlorofylu je veľmi blízka štruktúre hemu, hlavnej zložky krvného farbiva. Rozdiel je v tom, že chlorofyl obsahuje horčík (horčíkový ión) a hem, hemoglobín - (ión železa). Tento objav profesora Jagellonskej univerzity Leona Marklevského potvrdil súvislosť medzi vývojom flóry a fauny.
Môžeme povedať, že to isté sa stane človeku, hoci ... všetko je oveľa komplikovanejšie. Človek nemôže byť zdravý, ak v potrave nie je dostatok horčíka. K tomuto záveru dospeli účastníci prvého kongresu o chorobách spôsobených nedostatkom horčíka. Kongres sa konal v máji 1971 vo Vitteli. Horčíkový ión hrá zvláštnu úlohu takmer vo všetkých procesoch, ktoré prebiehajú v tele. V imunitných procesoch teda pôsobí ako antistresové, antitoxické, antialergické, antianafylaktické (typ citlivosti), protizápalové, chrániace pred ionizujúcim žiarením, reguluje teplotu, stimuluje a podieľa sa na tvorbe protilátky. Horčík má relaxačný účinok a znižuje citlivosť organizmu. Práve vtedy na kongrese vo Vitteli profesor Dürlach povedal: „Znakom moderného civilizovaného sveta je neustále sa znižujúca hladina horčíkového iónu.“
Zdá sa, že civilizačné choroby sú z veľkej časti spôsobené nedostatkom horčíka v ľudskom tele. Preto sa oplatí pozrieť sa na horčík bližšie.
Horčík získavame z pôdy – prostredníctvom potravín rastlinného pôvodu a potravín získaných zo zvierat, ktoré sa živia rastlinami. Do nášho tela sa teda dostane toľko horčíka, koľko je v pôde.
Medzitým je v pôde málo horčíka. Nedostatok horčíka je zaznamenaný v 40 % poľských krajín, priemerný obsah v 34 % krajín a dostatočný alebo vysoký obsah v menej ako 26 %. Umelé hnojivá buď pôdu horčíkom neobohacujú vôbec, alebo ho prijíma príliš málo. Napríklad v rokoch 1971-1975. Priemerné množstvo horčíka pridávaného do poľských pozemkov bolo 10-12 kg oxidu horečnatého (MgO) na 1 ha obrábanej pôdy. Je to veľa alebo málo? Pšenica s úrodou 40 q/ha by mala prijať z pôdy asi 17 kg s 1 ha MgO a cukrová repa s úrodou len 350 q/ha - asi 66 kg.
Samozrejme, množstvo potrebného horčíkového hnojiva závisí od obsahu horčíka v pôde a druhu pestovanej plodiny. Zvyčajne je to od 130 do 260 kg/ha. Z tohto množstva kieseritu (horečnaté hnojivo) prechádza do pôdy 30-60 kg oxidu horečnatého a okrem toho 15-31 kg oxidu draselného. Maštaľný hnoj obsahuje 0,18 % horčíka, čo znamená, že ak aplikujeme 300 kg maštaľného hnoja na 1 ha, získame cca 54 kg Mg. Toto rozhodne nestačí.
Chlorofyl obsahuje 2,7% horčíka. Ióny horčíka regulujú stupeň hydratácie buniek. Pri nedostatku horčíka v rastlinách je proces odparovania vody obmedzený a pri nadbytku rastlina vodu intenzívne absorbuje, takže pôda v koreňovom systéme vysychá.
Pre záujemcov je tu tabuľka.
Minerálne prvky.doc
Minerály1. Úloha minerálnych prvkov v ľudskom organizme 1
2. Makronutrienty, ich charakteristika
3. Stopové prvky, ich charakteristika
4. Vplyv technologického spracovania
O minerálnom zložení potravinárskych výrobkov
5. Metódy stanovenia minerálnych látok
1. Úloha minerálnych prvkov v ľudskom organizme
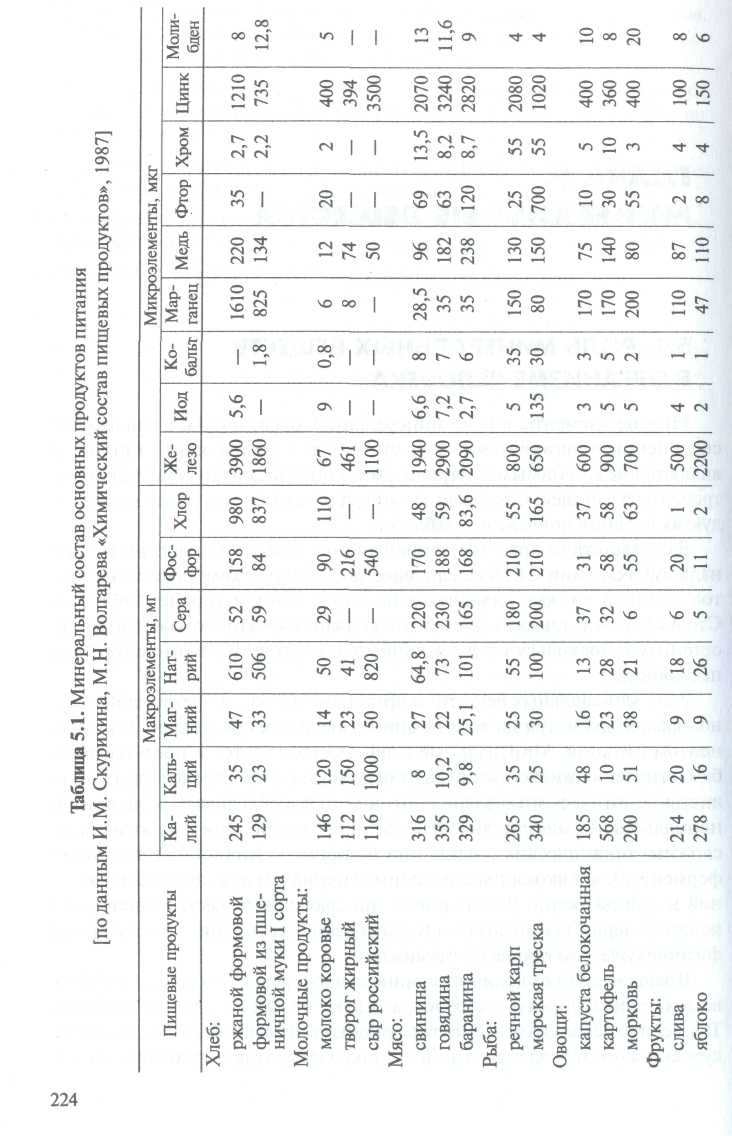
Mnoho prvkov vo forme minerálnych solí, iónov, komplexných zlúčenín a organickej hmoty sú súčasťou živej hmoty a sú základnými živinami, ktoré sa musia denne konzumovať s jedlom. Obsah minerálnych látok v hlavných potravinách je uvedený v tabuľke. 5.1.
Podľa odporúčania dietetického výboru Národná akadémia USA by mal byť denný príjem chemických prvkov s jedlom na určitej úrovni (tabuľka 5.2). Denne sa musí z tela vylúčiť rovnaký počet chemických prvkov, keďže ich obsah v ňom je relatívne konštantný.
Úloha minerálov v ľudskom organizme je mimoriadne rôznorodá, napriek tomu, že nie sú podstatnou zložkou výživy. Minerálne látky sú obsiahnuté v protoplazme a biologických tekutinách, zohrávajú hlavnú úlohu pri zabezpečovaní stálosti osmotického tlaku, ktorý je nevyhnutnou podmienkou pre normálne fungovanie buniek a tkanív. Sú súčasťou zložitých organických zlúčenín (napríklad hemoglobínu, hormónov, enzýmov), sú plastickým materiálom na stavbu kostného a zubného tkaniva. Vo forme iónov sa minerálne látky podieľajú na prenose nervových vzruchov, zabezpečujú zrážanlivosť krvi a ďalšie fyziologické procesy organizmu.
 |
V závislosti od množstva minerálov v ľudskom tele a potravinových výrobkoch sa delia na makro- a stopové prvky. Takže, ak hmotnostný zlomok prvku v tele presahuje 10 -2%, potom by sa mal považovať za makroprvok. Podiel stopových prvkov v organizme je 10 -3 -10 -5%. Ak je obsah prvku pod 10 -5%, považuje sa za ultramikroprvok. Medzi makroživiny patrí draslík, sodík, vápnik, horčík, fosfor, chlór a síra. Sú obsiahnuté v množstvách meraných v stovkách a desiatkach miligramov na 100 g tkaniva alebo potraviny. Stopové prvky sú súčasťou tkanív tela v koncentráciách vyjadrených v desatinách, stotinách a tisícinách miligramu a sú nevyhnutné pre jeho normálne fungovanie. Stopové prvky sú podmienene rozdelené do dvoch skupín: absolútne alebo životne dôležité (kobalt, železo, meď, zinok, mangán, jód, bróm, fluór) a takzvané pravdepodobne nevyhnutné (hliník, stroncium, molybdén, selén, nikel, vanád a niektoré ďalšie). ). Stopové prvky sa nazývajú životne dôležité, ak je pri ich nedostatku alebo nedostatku narušené normálne fungovanie tela.
Rozloženie stopových prvkov v tele závisí od ich chemické vlastnosti a veľmi pestrá. Železo je napríklad neoddeliteľnou súčasťou hemoglobínu, myoglobínu a iných respiračných pigmentov, teda látok, ktoré sa podieľajú na absorpcii a transporte kyslíka do všetkých tkanív tela; atómy medi sú zahrnuté v aktívnom centre množstva enzýmov atď.
Pôsobenie mikroprvkov môže byť aj nepriame – prostredníctvom vplyvu na intenzitu alebo charakter metabolizmu. Takže niektoré mikroelementy (napríklad mangán, zinok, jód) ovplyvňujú rast a ich nedostatočný príjem s jedlom bráni normálnemu fyzický vývoj dieťa. Ďalšie stopové prvky (napríklad molybdén, meď, mangán) sa podieľajú na reprodukčnej funkcii a ich nedostatok v organizme negatívne ovplyvňuje túto stránku ľudského života.
K najviac deficitným minerálom v strave moderný človek zahŕňajú vápnik a železo, prebytok - sodík a fosfor.
Nedostatok alebo prebytok akýchkoľvek minerálnych látok v strave spôsobuje narušenie metabolizmu bielkovín, tukov, sacharidov, vitamínov, čo vedie k rozvoju mnohých chorôb. Nižšie sú uvedené charakteristické (typické) príznaky nedostatku rôznych chemických prvkov v ľudskom tele: Najčastejším dôsledkom nesúladu množstva vápnika a fosforu v strave je zubný kaz, rednutie kostí. Pri nedostatku fluóru v pitnej vode sa ničí zubná sklovina, nedostatok jódu v potrave a vode vedie k ochoreniam štítnej žľazy. Minerály sú teda veľmi dôležité pre elimináciu a prevenciu množstva chorôb.


Uvádzame príčiny porúch metabolizmu minerálnych látok, ktoré sa môžu vyskytnúť aj pri ich dostatočnom množstve v potrave:
A) nevyvážená výživa (nedostatočné alebo nadmerné množstvo bielkovín, tukov, sacharidov, vitamínov atď.);
B) používanie spôsobov kulinárskeho spracovania potravín, ktoré spôsobujú stratu minerálov, napríklad pri rozmrazovaní (v horúca voda) mäso, ryby alebo pri odstraňovaní odvarov zo zeleniny a ovocia, kde prechádzajú rozpustné soli;
C) nedostatok včasnej korekcie zloženia stravy, keď sa mení potreba minerálov v tele spojená s fyziologickými dôvodmi. Napríklad ľudia pracujúci v podmienkach zvýšená teplota vonkajšie prostredie, potreba draslíka, sodíka, chlóru a iných minerálov stúpa vzhľadom na to, že väčšina z nich sa z tela vylučuje potom;
D) porušenie procesu absorpcie minerálov v gastrointestinálnom trakte alebo zvýšená strata tekutín (napríklad strata krvi).
^
2. Makronutrienty, ich charakteristika
Vápnik. Je hlavnou stavebnou zložkou kostí a zubov; je súčasťou jadier buniek, bunkových a tkanivových tekutín, je nevyhnutný pre zrážanie krvi. Vápnik tvorí zlúčeniny s proteínmi, fosfolipidmi, organickými kyselinami; podieľa sa na regulácii permeability bunkových membrán, na prenose nervových vzruchov, na molekulárnom mechanizme svalových kontrakcií, riadi činnosť radu enzýmov. Takže vápnik plní nielen plastické funkcie, ale ovplyvňuje aj mnohé biochemické a fyziologické procesy v organizme.
Vápnik je ťažko stráviteľný prvok. Zlúčeniny vápnika vstupujúce do ľudského tela s jedlom sú prakticky nerozpustné vo vode. Alkalické prostredie tenkého čreva podporuje tvorbu nestráviteľných zlúčenín vápnika a len pôsobenie žlčových kyselín zabezpečuje jeho vstrebávanie.
Asimilácia vápnika tkanivami závisí nielen od jeho obsahu v potravinách, ale aj od pomeru s ostatnými zložkami potravy a predovšetkým s tukmi, horčíkom, fosforom a bielkovinami. Pri nadbytku tuku dochádza ku konkurencii žlčových kyselín a značná časť vápnika sa vylučuje z tela cez hrubé črevo. Absorpciu vápnika nepriaznivo ovplyvňuje nadbytok horčíka; odporúčaný pomer týchto prvkov je 1:0,5. Ak množstvo fosforu prevyšuje hladinu vápnika v potravinách viac ako 2-krát, tvoria sa rozpustné soli, ktoré sú extrahované krvou z kostného tkaniva. Vápnik sa dostáva do stien ciev, čo spôsobuje ich krehkosť, ako aj do tkanív obličiek, čo môže prispieť k výskytu obličkových kameňov. Pre dospelých je odporúčaný pomer vápnika a fosforu v potravinách 1:1,5. Ťažkosti s udržaním tohto pomeru sú spôsobené tým, že väčšina bežne konzumovaných potravín je oveľa bohatšia na fosfor ako na vápnik. Fytín a kyselina šťaveľová, obsiahnuté v množstve rastlinných produktov, majú negatívny vplyv na vstrebávanie vápnika. Tieto zlúčeniny tvoria nerozpustné soli s vápnikom.
Denná potreba vápnika u dospelých je 800 mg a u detí a dospievajúcich - 1 000 mg alebo viac.
Pri nedostatočnom príjme vápnika alebo pri porušení jeho vstrebávania v tele (s nedostatkom vitamínu D) vzniká stav nedostatku vápnika. Dochádza k jeho zvýšenému vylučovaniu z kostí a zubov. U dospelých vzniká osteoporóza - demineralizácia kostného tkaniva, u detí je narušená tvorba kostry, vzniká krivica.
Najlepšími zdrojmi vápnika sú mlieko a mliečne výrobky, rôzne syry a tvaroh (100-1000 mg / 100 g výrobku), zelená cibuľa, petržlen, fazuľa. Výrazne menej vápnika obsahujú vajcia, mäso, ryby, zelenina, ovocie, bobuľové ovocie (20-40 mg/100 g výrobku).
magnézium. Tento prvok je potrebný pre činnosť mnohých kľúčových enzýmov. pre metabolizmus organizmu. Horčík sa podieľa na udržiavaní normálnej funkcie nervového systému a srdcových svalov; má vazodilatačný účinok; stimuluje sekréciu žlče; zvyšuje motorická aktivitačriev, čo pomáha odstraňovať toxíny z tela (vrátane cholesterolu).
Absorpciu horčíka bráni prítomnosť fytínu a prebytočného tuku a vápnika v potrave. Denná potreba horčíka nie je presne definovaná; predpokladá sa však, že dávka 200-300 mg/deň predchádza prejavom nedostatku (predpokladá sa, že sa vstrebe asi 30 % horčíka).
Pri nedostatku horčíka sa narúša vstrebávanie potravy, spomaľuje sa rast, ukladá sa vápnik v stenách ciev a vzniká množstvo ďalších patologických javov. U ľudí je nedostatok horčíkových iónov, vzhľadom na povahu výživy, mimoriadne nepravdepodobný. Pri hnačke však môžu nastať veľké straty tohto prvku; ich dôsledky sa prejavia, ak sa do tela dostanú tekutiny, ktoré neobsahujú horčík. Keď koncentrácia horčíka v sére klesne na približne 0,1 mmol / l, môže sa objaviť syndróm pripomínajúci delírium tremens: človek má polokomatózny stav, svalové triašky, svalové kŕče v zápästí a chodidle, zvýšenú nervovosvalovú dráždivosť v reakcii na zvuk, mechanické a vizuálne podnety. Zavedenie horčíka spôsobuje rýchle zlepšenie stavu.
Horčík je bohatý najmä na rastlinnú potravu. Veľké množstvo obsahuje pšeničné otruby, rôzne obilniny (40 - 200 mg / 100 g výrobku), strukoviny, marhule, sušené marhule, sušené slivky. Málo horčíka je v mliečnych výrobkoch, mäse, rybách, cestovinách, väčšine zeleniny a ovocia (20 - 40 mg / 100 g).
Draslík. Asi 90% draslíka je vo vnútri buniek. Spolu s inými soľami zabezpečuje osmotický tlak; podieľa sa na prenose nervových impulzov; regulácia metabolizmu voda-soľ; podporuje odstraňovanie vody a následne toxínov z tela; udržiava acidobázickú rovnováhu vnútorného prostredia tela; podieľa sa na regulácii činnosti srdca a iných orgánov; nevyhnutné pre fungovanie množstva enzýmov.
Draslík sa dobre vstrebáva z čriev a jeho prebytok sa z tela rýchlo odstraňuje močom. Denná potreba draslíka u dospelého človeka je 2000-4000 mg. Zvyšuje sa pri hojnom potení, pri užívaní diuretík, ochoreniach srdca a pečene. Draslík nie je deficitnou živinou v strave a pri pestrej strave k nedostatku draslíka nedochádza. Nedostatok draslíka v tele sa objavuje pri poruche funkcie nervovo-svalového a kardiovaskulárneho systému, ospalosti, znížení krvného tlaku a srdcových arytmiách. V takýchto prípadoch je predpísaná draslíková diéta.
Väčšina draslíka pochádza z rastlinných potravín. Jeho bohatým zdrojom sú marhule, sušené slivky, hrozienka, špenát, morské riasy, fazuľa, hrach, zemiaky, ostatná zelenina a ovocie (100 - 600 mg / 100 g výrobku). Menej draslíka obsahuje kyslá smotana, ryža, chlieb z prémiovej múky (100 - 200 mg / 100 g).
Sodík. Sodík sa nachádza vo všetkých tkanivách a telesných tekutinách. Podieľa sa na udržiavaní osmotického tlaku v tkanivových tekutinách a krvi; pri prenose nervových impulzov; regulácia acidobázickej rovnováhy, metabolizmus voda-soľ; zvyšuje aktivitu tráviacich enzýmov.
Metabolizmus sodíka bol značne študovaný kvôli jeho fyziologickým vlastnostiam a významu pre telo. Táto živina sa ľahko vstrebáva z čriev. Ióny sodíka spôsobujú opuch tkanivových koloidov, čo spôsobuje zadržiavanie vody v tele a pôsobí proti jej uvoľňovaniu. Celkové množstvo sodíka v extracelulárnej tekutine teda určuje objem týchto tekutín. Zvýšenie plazmatickej koncentrácie sodíka vedie k pocitu smädu. V horúcom podnebí a pri ťažkej fyzickej práci dochádza k výraznému úbytku sodíka potením a na doplnenie strateného množstva je potrebné do tela dodávať soľ.
V zásade sa ióny sodíka dostávajú do tela na úkor kuchynskej soli - NaCl. Pri nadmernej konzumácii chloridu sodného sa zhoršuje odstraňovanie vo vode rozpustných konečných produktov metabolizmu obličkami, kožou a inými vylučovacími orgánmi. Zadržiavanie vody v tele komplikuje činnosť kardiovaskulárneho systému, zvyšuje krvný tlak. Preto je konzumácia soli pri príslušných ochoreniach v strave obmedzená. Pri práci v horúcich obchodoch alebo horúcom podnebí sa však množstvo sodíka (vo forme kuchynskej soli) privádzaného zvonka zvyšuje, aby sa jeho strata vyrovnala potom a znížilo sa potenie, ktoré zaťažuje činnosť srdca.
Sodík je prirodzene prítomný vo všetkých potravinách. Spôsob získavania potravinárskych výrobkov do značnej miery určuje konečný obsah sodíka v nich. Napríklad mrazený zelený hrášok obsahuje oveľa viac sodíka ako čerstvý. Čerstvá zelenina a ovocie obsahujú menej ako 10 mg/kg až 1 g/kg, na rozdiel od obilnín a syrov, ktoré môžu obsahovať sodík v množstve 10 – 20 g/kg.
Odhadnúť priemerný denný príjem sodíka z potravy je ťažké, pretože koncentrácia sodíka v potravinách sa značne líši a navyše ľudia sú zvyknutí do jedla prisoľovať. Dospelý človek denne skonzumuje až 15 g kuchynskej soli a rovnaké množstvo z tela vylúči. Toto množstvo je oveľa vyššie, ako je fyziologicky potrebné a je určená predovšetkým chuťou chloridu sodného, zvykom na slané jedlá. Obsah kuchynskej soli v ľudskej potrave možno bez poškodenia zdravia znížiť na 5 g denne. Uvoľňovanie chloridu sodného z tela, a teda aj jeho potreba, je ovplyvnené množstvom draselných solí prijatých telom. Rastlinné potraviny, najmä zemiaky, sú bohaté na draslík a zvyšujú vylučovanie chloridu sodného močom, a tým aj jeho potrebu.
Fosfor. Fosfor sa nachádza vo všetkých tkanivách tela, najmä vo svaloch a mozgu. Tento prvok sa podieľa na všetkých životných procesoch tela. : syntéza a rozklad látok v bunkách; regulácia metabolizmu; je súčasťou nukleových kyselín a radu enzýmov; potrebné na tvorbu ATP.
Fosfor sa nachádza v telesných tkanivách a potravinách vo forme kyseliny fosforečnej a jej organických zlúčenín (fosfátov). Jeho hlavná hmota je v kostnom tkanive vo forme fosforečnanu vápenatého, zvyšok fosforu je súčasťou mäkkých tkanív a tekutín. Vo svaloch dochádza k najintenzívnejšej výmene zlúčenín fosforu. Kyselina fosforečná sa podieľa na konštrukcii molekúl mnohých enzýmov, nukleových kyselín atď.
Pri dlhodobom nedostatku fosforu v strave telo využíva vlastný fosfor z kostného tkaniva. To vedie k demineralizácii kostí a narušeniu ich štruktúry - riedeniu. Keď je telo vyčerpané fosforom, duševná a fyzická výkonnosť klesá, strata chuti do jedla, apatia je zaznamenaná.
Denná potreba fosforu pre dospelých je 1200 mg. Zvyšuje sa pri veľkom fyzickom alebo psychickom vypätí, pri niektorých chorobách.
Veľké množstvo fosforu sa nachádza v živočíšnych produktoch, najmä v pečeni, kaviári, ako aj v obilninách a strukovinách. Jeho obsah v týchto výrobkoch sa pohybuje od 100 do 500 mg na 100 g výrobku. Bohatým zdrojom fosforu sú obilniny (ovsené vločky, perličkový jačmeň), obsahujú 300-350 mg fosforu / 100 g.Z rastlinných produktov sa však zlúčeniny fosforu vstrebávajú horšie ako pri konzumácii potravín živočíšneho pôvodu.
Síra. Dôležitosť tohto prvku vo výžive je daná predovšetkým skutočnosťou, že je súčasťou bielkovín vo forme aminokyselín obsahujúcich síru. (metionín a cystín), a je tiež neoddeliteľnou súčasťou niektorých hormónov a vitamínov.
Ako zložka aminokyselín obsahujúcich síru sa síra podieľa na procesoch metabolizmu bielkovín a jej potreba sa dramaticky zvyšuje počas tehotenstva a rastu tela, sprevádzaná aktívnym začlenením bielkovín do výsledných tkanív, ako aj počas zápalových procesov. procesy. Aminokyseliny obsahujúce síru, najmä v kombinácii s vitamínmi C a E, majú výrazný antioxidačný účinok. Síra spolu so zinkom a kremíkom určuje funkčný stav vlasov a pokožky.
Chlór. Tento prvok sa podieľa na tvorbe žalúdočnej šťavy, tvorbe plazmy, aktivuje množstvo enzýmov. Táto živina sa ľahko vstrebáva z čriev do krvi. Zaujímavá je schopnosť chlóru ukladať sa v koži, zdržiavať sa v tele pri nadmernom príjme a vylučovať sa potením vo významnom množstve. K vylučovaniu chlóru z tela dochádza najmä močom (90 %) a potom.
Porušenie výmeny chlóru vedie k rozvoju edému, nedostatočnej sekrécii žalúdočnej šťavy atď. Prudký pokles obsahu chlóru v tele môže viesť k vážnemu stavu, dokonca k smrti. K zvýšeniu jeho koncentrácie v krvi dochádza pri dehydratácii tela, ako aj pri porušení vylučovacej funkcie obličiek.
Denná potreba chlóru je približne 5000 mg. Chlór sa do ľudského tela dostáva najmä vo forme chloridu sodného pri pridávaní do potravy.
^
3. Stopové prvky, ich charakteristika
Železo. Tento prvok je nevyhnutný pre biosyntézu zlúčenín, ktoré poskytujú dýchanie, hematopoézu; podieľa sa na imunobiologických a redoxných reakciách; je súčasťou cytoplazmy, bunkových jadier a množstva enzýmov.
Asimilácii železa bráni kyselina šťaveľová a fytín. Na asimiláciu tejto živiny je potrebný vitamín B12. Kyselina askorbová tiež prispieva k absorpcii železa, pretože železo sa absorbuje vo forme dvojmocného iónu.
^ Nedostatok železa v tele môže viesť k rozvoju anémie, výmene plynov, bunkovému dýchaniu, to znamená k narušeniu základných procesov, ktoré zabezpečujú život. K vzniku stavov nedostatku železa napomáha: nedostatočný príjem železa v organizme v asimilovanej forme, zníženie sekrečnej aktivity žalúdka, nedostatok vitamínov (najmä B 12 , kyselina listová a askorbová) a množstvo chorôb, ktoré spôsobujú stratu krvi.
Potreba železa dospelého človeka (14 mg/deň) je splnená v nadbytočnej miere bežnou stravou. Keď sa však v potravinách používa chlieb z jemnej múky obsahujúcej málo železa, u obyvateľov miest sa veľmi často pozoruje nedostatok železa. Malo by sa vziať do úvahy, že obilné produkty bohaté na fosfáty a fytín tvoria so železom ťažko rozpustné zlúčeniny a znižujú jeho asimiláciu telom.
Železo je rozšírený prvok. Nachádza sa vo vnútornostiach, mäse, vajciach, fazuli, zelenine, bobuliach. V ľahko stráviteľnej forme sa však železo nachádza len v mäsových výrobkoch, pečeni (do 2000 mg / 100 g výrobku), vaječnom žĺtku.
Meď. Meď je základným prvkom ľudského metabolizmu, zohráva úlohu pri tvorbe červených krviniek, uvoľňovaní tkanivového železa a vývoji kostry, centrálneho nervového systému a spojivového tkaniva.
Keďže meď je široko distribuovaná v potravinách, je nepravdepodobné, že by sa u ľudí, možno s výnimkou dojčiat, ktorí sú na čisto mliečnej strave, niekedy vyvinula forma podvýživy súvisiacej s meďou.
Konzumácia nadmerne veľkých dávok medi u človeka vedie k podráždeniu a erózii slizníc, rozsiahlemu poškodeniu kapilár, poškodeniu pečene a obličiek a podráždeniu centrálneho nervového systému. Denná potreba tohto prvku je asi 2 mg. Zdrojom medi sú potraviny ako pečeň, vaječný žĺtok, zelená zelenina.
jód. Jód je základným prvkom, ktorý sa podieľa na tvorbe hormónu tyroxínu. Pri nedostatku jódu vzniká struma – ochorenie štítnej žľazy.
Potreba jódu sa pohybuje od 100-150 mcg denne. Obsah jódu v potravinách je zvyčajne nízky (4-15 µg %). Morské plody sú najbohatšie na jód. Takže v morských rybách obsahuje asi 50 mcg / 100 g, v tresčej pečeni až 800, v morských riasach, v závislosti od typu a načasovania odberu - od 50 mcg do 70 000 mcg / 100 g produktu. Treba ale počítať s tým, že pri dlhodobom skladovaní a tepelnej úprave potravín sa značná časť jódu (od 20 do 60 %) stráca.
Obsah jódu v suchozemských rastlinných a živočíšnych produktoch je vysoko závislý od jeho množstva v pôde. V oblastiach, kde je v pôde málo jódu, môže byť jeho obsah v potravinách 10 až 100-krát nižší ako je priemer. Preto v týchto oblastiach na prevenciu strumy sa do kuchynskej soli pridáva malé množstvo jodičnanu draselného (25 mg na 1 kg soli). Skladovateľnosť takejto jodizovanej soli nie je dlhšia ako 6 mesiacov, pretože jód počas skladovania soli postupne mizne.
Fluór. Pri nedostatku tohto prvku vzniká zubný kaz (deštrukcia zubnej skloviny). Nadbytok fluóru má tiež negatívny vplyv na telo, pretože soli fluóru, ktoré sa hromadia v kostiach, spôsobujú zmenu farby a tvaru zubov, osteochondrózu, a po tomto zhrubnutí kĺbov a ich nehybnosti, kostných výrastkov. Rozdiel medzi užitočnými a škodlivými dávkami fluóru je taký malý, že mnohí výskumníci sú proti fluoridácii vody.
Fluór konzumovaný s vodou je takmer úplne absorbovaný, fluór obsiahnutý v potravinách je absorbovaný v menšej miere. Absorbovaný fluór je rovnomerne distribuovaný po celom tele. Zadržiava sa hlavne v kostre a malé množstvo sa ukladá v zubnom tkanive. Vo vysokých dávkach môže fluór spôsobiť narušenie metabolizmu uhľohydrátov, lipidov, bielkovín, ako aj metabolizmu vitamínov, enzýmov a minerálnych solí.
V rôznych krajinách sa robili odhady denného príjmu fluoridu z potravy; pre dospelých sa táto hodnota pohybuje od 0,2 do 3,1 mg pre deti veková skupina od 1 do 3 rokov sa príjem fluoridu odhadoval na 0,5 mg/deň.
Takmer všetky potravinárske výrobky obsahujú aspoň stopové množstvá tohto prvku. Všetky druhy vegetácie obsahujú určité množstvo fluóru, ktorý získavajú z pôdy a vody. Vysoké hladiny fluoridu sa našli v niektorých potravinách, najmä v rybách, niektorých druhoch zeleniny a čaji. Používanie fluoridovanej vody v závodoch na spracovanie potravín môže často zdvojnásobiť hladinu fluoridov v hotových výrobkoch.
Na prevenciu a liečbu zubného kazu, rôzne zubné pasty, prášky, elixíry, žuvačky a podobne, ktoré obsahujú pridaný fluór, hlavne v anorganickej forme. Tieto zlúčeniny sa bežne začleňujú do prostriedkov na čistenie zubov, typicky v koncentráciách približne 1 g/kg.
Chromium. Zdá sa, že tento prvok je nevyhnutný pre metabolizmus glukózy a lipidov a pre využitie aminokyselín niektorými systémami. Tiež má dôležitosti na prevenciu miernych foriem cukrovky a aterosklerózy u ľudí.
Chróm sa vstrebáva z gastrointestinálneho traktu aj z dýchacieho traktu. Absorbované množstvo nie je pre každý z týchto systémov rovnaké a závisí od formy chrómu. Trojmocný chróm je pre človeka nevyhnutnou formou prvku, šesťmocný chróm je toxický. Chróm je distribuovaný v tkanivách ľudského tela v nerovnakých, ale zvyčajne nízkych koncentráciách. Hladiny chrómu vo všetkých tkanivách okrem pľúc s vekom klesajú. Najväčšie množstvo chrómu sa u ľudí hromadí v koži, svaloch a tukovom tkanive. Homeostatické mechanizmy, vrátane mechanizmov transportu v pečeni a črevách, zabraňujú nadmernej akumulácii trojmocného chrómu. Chróm sa pomaly vylučuje z tela hlavne močom.
Dnes sa za normu považuje spotreba asi 150 mg chrómu denne. Je obzvlášť užitočný pre starších ľudí, ktorých telo neabsorbuje sacharidy dobre a chróm podporuje metabolické procesy týchto konkrétnych zlúčenín. Anorganický chróm sa vstrebáva zle, oveľa ľahšie - v organických zlúčeninách, teda vo forme, v akej sa nachádza v živých organizmoch.
Potravinárske výrobky sa značne líšia v hladinách chrómu, ktoré sa pohybujú od 20 do 550 µg/kg. Bohatým zdrojom chrómu sú pivovarské kvasnice, pečeň (10-80 mcg/100 g). V menšom množstve sa tento prvok nachádza v zemiakoch so šupkou, hovädzom mäse, čerstvej zelenine, celozrnnom pečive, syroch.
mangán. Mangán je nevyhnutný ako kofaktor v mnohých enzýmových systémoch; podieľa sa na správnom fungovaní flavoproteínov, pri syntéze sulfátovaných mukopolysacharidov, cholesterolu, hemoglobínu a v mnohých ďalších metabolických procesoch. Z požitého mangánu sa absorbujú len asi 3 %.
Vstrebávanie mangánu úzko súvisí so vstrebávaním železa. Potreba mangánu je 0,2-0,3 mg na 1 kg hmotnosti človeka denne. Najviac mangánu obsahujú brusnice a čaj, o niečo menej gaštany, kakao, zelenina, ovocie (100-200 mcg / 100 g).
^ Nikel. Nikel bol uznaný ako esenciálny stopový prvok relatívne nedávno. V súčasnosti je preukázaná jeho úloha ako koenzýmu v procesoch metabolizmu železa. Zároveň je zvýšený príjem železa v tele sprevádzaný zvýšením potreby potravinového niklu. Okrem toho nikel prispieva k absorpcii medi - ďalšieho prvku nevyhnutného pre hematopoézu. Význam potravinárskeho niklu alebo niklu izolovaného z prírodných produktov zvýrazňuje skutočnosť, že syntetické zlúčeniny tohto prvku sú karcinogénne.
Nikel je prítomný vo väčšine potravín, ale v koncentráciách nižších (a často oveľa nižších) ako 1 mg/kg. Uvádza sa, že príjem niklu v strave sa pohybuje od menej ako 200 do 900 µg/deň. Pri normálnej strave prichádza asi 400 mcg / deň. Ukázalo sa, že obsah niklu vo vínach a pive je 100 a 50 µg/l.
Zinok. Tento stopový prvok sa ako koenzým podieľa na širokom spektre reakcií biosyntézy bielkovín (viac ako 70) a metabolizmu nukleových kyselín (vrátane procesov replikácie a transkripcie DNA), ktoré zabezpečujú predovšetkým rast a pubertu organizmu. Zároveň je zinok spolu s mangánom špecifickým stopovým prvkom, ktorý ovplyvňuje stav sexuálnej funkcie, konkrétne aktivitu niektorých pohlavných hormónov, spermatogenézu, vývoj mužských pohlavných žliaz a sekundárne sexuálne charakteristiky. Okrem toho sa v poslednej dobe uvažuje o úlohe zinku v prevencii hypertrofických procesov v prostatickej žľaze.
Zinok sa spolu so sírou podieľa na raste a obnove pokožky a vlasov. Spolu s mangánom a meďou sa zinok významne podieľa na vnímaní chuťových a čuchových vnemov. Zinok ako nenahraditeľná zložka je súčasťou molekuly inzulínu a u pacientov s diabetes mellitus je jeho hladina znížená. Je veľmi dôležité, že tento mikroelement je koenzým alkoholdehydrogenázy, ktorý zabezpečuje metabolizmus etylalkoholu. Zároveň sa prudko znižuje úroveň absorpcie zinku pri chronickom alkoholizme. Takzvaná "nočná slepota" (t.j. zhoršené nočné videnie) sa môže vyvinúť nielen pri nedostatku vitamínu A, ale aj zinku. Zinok spolu s vitamínom B 6 zabezpečuje metabolizmus nenasýtených mastných kyselín a syntézu prostaglandínov.
Zinok je veľmi dôležitý pre trávenie a vstrebávanie živín. Zinok teda zabezpečuje syntézu najdôležitejších tráviacich enzýmov v pankrease a podieľa sa aj na tvorbe chylomikrónov – transportných častíc, v ktorých sa tuky z potravy môžu vstrebávať do krvi. Zinok je spolu s vitamínmi skupiny B dôležitým regulátorom funkcií nervového systému. V podmienkach nedostatku zinku môžu nastať emocionálne poruchy, emočná nestabilita, podráždenosť a vo veľmi ťažkých prípadoch môže dôjsť aj k cerebelárnej dysfunkcii. Napokon sa hromadí stále viac údajov v prospech účasti zinku v procesoch dozrievania lymfocytov a reakciách bunkovej imunity.
Denná potreba zinku je 8000-22000 mcg%. S bežnou stravou je celkom spokojná. Priemerný denný príjem zinku len s pitnou vodou je asi 400 mcg. Obsah zinku v potravinárskych výrobkoch sa zvyčajne pohybuje od 150 do 25 000 µg%. V pečeni, mäse a strukovinách však dosahuje 3000 - 5000 mcg%. Niekedy môže nedostatok zinku pociťovať telo detí a dospievajúcich, ktorí nekonzumujú dostatok živočíšnych produktov.
^ Selén. Dokonca aj v polovici XX storočia. selén nielenže nutričná veda nepovažovala, ale bol dokonca považovaný za veľmi toxický prvok s karcinogénnymi vlastnosťami. Avšak už v 60. rokoch. zistilo sa, že s nedostatkom selénu trpí kardiovaskulárny systém, ktorá sa prejavuje progresívnou aterosklerózou a slabosťou srdcového svalu a pri stavoch chronického nedostatku selénu môže vzniknúť takmer neliečiteľná kardiomyopatia. V poslednej dobe na úrovni súčasný výskum nachádza potvrdenie jedného z dôležitých pozorovaní starovekej čínskej medicíny, čo naznačuje dostatočné zásobenie tela selénom pomáha spomaľovať proces starnutia a vedie k dlhovekosti . Zaujímavosťou je, že známe liečivé odrody zeleného čaju, dodávané s cieľom dosiahnuť zdravie a dlhovekosť v cisárskych palácoch v r. Staroveká Čína, boli pestované v tých horských provinciách, v ktorých pôdach je už pomocou moderných analytických metód stanovený vysoký obsah selénu.
Po objavení selénu sa zistilo, že vitamín E a selén pôsobia na rôzne časti toho istého procesu a navzájom sa striktne dopĺňajú, to znamená, že ich antioxidačná aktivita sa pri spoločnom použití dramaticky zvyšuje. Synergia oboch antioxidantov je obzvlášť zaujímavá v kontexte protirakovinovej aktivity. Ukázalo sa teda, že podávanie selénových prípravkov súčasne s vitamínom E výrazne zvýšilo antikarcinogénny účinok vo vzťahu k experimentálnym nádorom.
Príjem selénu potravou závisí od podmienok a charakteru príjmu potravy a od hladiny selénu v potravinách. Zelenina a ovocie sú vo všeobecnosti chudobným zdrojom selénu, na rozdiel od obilnín, obilných produktov, mäsa (najmä vedľajších produktov), morských plodov, ktoré obsahujú značné množstvo selénu, typicky vysoko nad 0,2 mg/kg vlhkej hmotnosti . Chemické zloženie Pôda a obsah selénu v nej výrazne ovplyvňuje množstvo selénu v zrne, pohybuje sa od 0,04 mg/kg do 21 mg/kg.
molybdén. Celkové množstvo molybdénu v tele dospelého človeka je asi 7 mg. Obsah molybdénu v krvi je asi 0,5 mikrogramu na 100 ml. Vyššie koncentrácie tohto prvku boli zistené u ľudí žijúcich v regiónoch, kde je pôda najbohatšia na zlúčeniny tohto kovu. V niektorých regiónoch Arménska boli teda zaznamenané časté prípady dny medzi obyvateľmi, ktorí jedia najmä miestne produkty, v ktorých sa zistilo extrémne vysoké množstvo molybdénu. Jeho obsah v strave obyvateľov tohto regiónu bol 10-15 mg. V iných oblastiach, kde boli prípady dny menej časté, dostávali ľudia z potravy len 1-2 mg molybdénu denne.
Molybdén je neoddeliteľnou súčasťou mnohých enzýmov, ako je xantínoxidáza, aldehydoxidáza, sulfátoxidáza. Je známe, že molybdén bráni vzniku zubného kazu.
Odhadovaná denná potreba molybdénu je 2 mcg na 1 kg telesnej hmotnosti. V Rusku je denný príjem molybdénu 0,27 mg.
najbohatší na molybdén rôzne druhy zelenina (napríklad strukoviny) a vnútorné orgány zvierat.
kobalt. Biologický účinok kobaltu je známy od roku 1948, keď vedci Rickes a Smith zistili, že atóm kobaltu je ústredným prvkom molekuly vitamínu B 12. Maximálna koncentrácia kobaltu v tkanivách je asi 100 μg / kg. Celkový obsah kobaltu v tele dospelého človeka je 5 mg. Človek s jedlom denne prijme 5,63 – 7,94 mikrogramov kobaltu, z čoho sa 73 – 97 % vstrebe.
Priemerná denná potreba kobaltu je 60 mcg na 1 kg telesnej hmotnosti. Predpokladá sa, že človek potrebuje kobalt iba vo forme kyanokobalamínu (vitamín B 12). V niektorých krajinách sa zlúčeniny kobaltu používali ako potravinová prísada do piva na stabilizáciu peny. Ukázalo sa však, že práve takáto prísada bola príčinou srdcových ochorení konzumentov piva. Preto sa teraz upustilo od používania zlúčenín kobaltu ako prídavnej látky v potravinách.
^
4 Vplyv spracovania na minerálne zloženie potravín
Pri spracovaní potravinárskych surovín spravidla dochádza k znižovaniu obsahu minerálnych látok (okrem Na, pridávaného vo forme potravinárskej soli). V rastlinnej potrave sa strácajú s odpadom. Pri výrobe obilnín a múky po spracovaní zrna sa teda znižuje obsah množstva makro- a najmä mikroprvkov, keďže týchto zložiek je v odstránených škrupinách a klíčkoch viac ako v celom zrne. Porovnávacia analýza Minerálne zloženie v pšeničnej múke najvyššej kvality a celozrnnej múke je uvedené nižšie (obsah prvkov je uvedený v mg / 100 g výrobku):
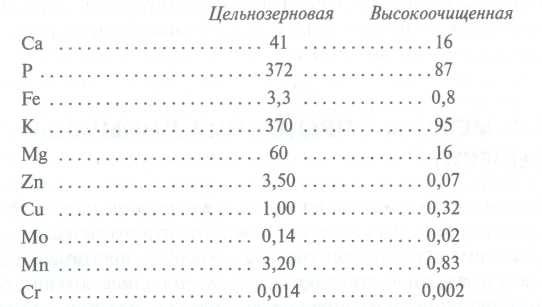
Napríklad zrno pšenice a raže obsahuje v priemere asi 1,7 % popola, zatiaľ čo v múke v závislosti od odrody od 0,5 (v najvyššej triede) do 1,5 % (v celozrnnej). Pri čistení zeleniny a zemiakov sa stráca 10 až 30 % minerálov. Ak sa podrobia tepelnému vareniu, potom sa v závislosti od technológie (varenie, vyprážanie, dusenie) stratí ďalších 5 až 30 %.
Mäso, rybie produkty a hydina pri oddeľovaní dužiny od kostí väčšinou strácajú makroživiny ako vápnik a fosfor.
Pri tepelnom varení (varenie, vyprážanie, dusenie) mäso stráca 5 až 50 % minerálov. Ak sa však spracovanie uskutočňuje za prítomnosti kostí obsahujúcich veľa vápnika, je možné zvýšiť obsah vápnika vo varených mäsových výrobkoch o 20 %.
V technologickom procese môže v dôsledku nedostatočne kvalitného zariadenia prejsť do konečného produktu určité množstvo mikroelementov. Takže pri pečení chleba počas prípravy cesta v dôsledku kontaktu cesta so zariadením obsah železa možno zvýšiť o 30 %. Tento proces je nežiaduci, pretože spolu so železom môžu do produktu prechádzať aj toxické prvky obsiahnuté vo forme nečistôt v kove. Pri skladovaní konzervovaných potravín v prefabrikovaných plechovkách (teda spájkovaných) plechovkách s nekvalitnou spájkou alebo pri porušení ochrannej vrstvy laku môžu do výrobku preniknúť vysoko toxické prvky ako olovo, kadmium a cín.
Je potrebné vziať do úvahy, že množstvo kovov, ako je železo a meď, aj v malých koncentráciách, môže spôsobiť nežiaducu oxidáciu produktov. Ich katalytické oxidačné schopnosti sú obzvlášť výrazné vo vzťahu k tukom a tukovým produktom. Takže napríklad pri koncentrácii železa nad 1,5 mg/kg a medi 0,4 mg/kg pri dlhodobom skladovaní masla a margarínov tieto kovy spôsobujú žltnutie výrobkov. Pri skladovaní nápojov v prítomnosti železa nad 5 mg/l a medi 1 mg/l možno za určitých podmienok často pozorovať zakalenie nápojov.
^
5. Metódy stanovenia minerálnych látok
Na rozbor minerálnych látok sa využívajú najmä fyzikálno-chemické metódy - optické a elektrochemické.
Takmer všetky tieto metódy vyžadujú špeciálnu prípravu vzoriek na analýzu, ktorá spočíva v predbežnej mineralizácii predmetu štúdia. Mineralizácia môže byť vykonaná dvoma spôsobmi: "suchým" a "mokrým". „Suchá“ mineralizácia zahŕňa zuhoľnatenie, spálenie a kalcináciu testovanej vzorky za určitých podmienok. „Mokrá“ mineralizácia zabezpečuje aj spracovanie predmetu štúdia koncentrované kyseliny(najčastejšie HNO 3 a H 2 SO 4).
^ Spektrálne metódy analýzy.
Fotoelektrokolorimetria - analýza založená na meraní absorpcie farebných roztokov monochromatického žiarenia vo viditeľnej oblasti spektra. Merania sa vykonávajú pomocou fotoelektrických kolorimetrov vybavených úzkopásmovými filtrami. Ak testovaná látka nie je zafarbená, musí sa premeniť na farebnú zlúčeninu chemickou reakciou s určitými činidlami (fotometrická analytická reakcia).
Spektrofotometria je analytická metóda založená na meraní absorpcie monochromatického žiarenia v ultrafialovej, viditeľnej a infračervenej oblasti spektra. Takéto merania sa vykonávajú pomocou spektrofotometrov, kde sa ako monochromatizéry používajú disperzné hranoly a difrakčné mriežky.
Kvantitatívna analýza študovaného iónu sa zvyčajne vykonáva pomocou metódy kalibračnej krivky.
Emisná spektrálna analýza. Metódy emisnej spektrálnej analýzy sú založené na meraní vlnovej dĺžky, intenzity a iných charakteristík svetla emitovaného atómami a iónmi látky v plynnom stave. Emisná spektrálna analýza umožňuje určiť elementárne zloženie anorganických a organických látok.
Intenzita spektrálnej čiary je určená počtom excitovaných atómov v zdroji excitácie, ktorý závisí nielen od koncentrácie prvku vo vzorke, ale aj od podmienok excitácie. Pri stabilnej prevádzke budiaceho zdroja je vzťah medzi intenzitou spektrálnej čiary a koncentráciou prvku (ak je dostatočne malá) lineárny, t.j. tento prípad kvantitatívnu analýzu možno vykonať aj pomocou metódy kalibračnej krivky.
Najväčšie uplatnenie ako zdroj budenia dostal elektrický oblúk, iskra, plameň. Teplota oblúka dosahuje 5000 - 6000°C. V oblúku je možné získať spektrum takmer všetkých prvkov. Pri iskrovom výboji sa vyvinie teplota 7000 - 10000 °C a všetky prvky sú vzrušené. Plameň poskytuje dostatočne jasné a stabilné emisné spektrum. Metóda analýzy využívajúca plameň ako zdroj budenia sa nazýva analýza emisií plameňa. Táto metóda stanovuje viac ako štyridsať prvkov (alkalické a alkalické zeminy, Cu 2, Mn 2 atď.).
^ Atómová absorpčná spektroskopia . Metóda je založená na schopnosti voľných atómov prvkov v plameňových plynoch absorbovať svetelnú energiu pri vlnových dĺžkach charakteristických pre každý prvok.
V atómovej absorpčnej spektroskopii je takmer úplne vylúčená možnosť prekrývania spektrálnych čiar rôznych prvkov, pretože ich počet v spektre je oveľa menší ako v emisnej spektroskopii.
Pokles intenzity rezonančného žiarenia v podmienkach atómovej absorpčnej spektroskopie sa riadi exponenciálnym zákonom poklesu intenzity v závislosti od hrúbky vrstvy a koncentrácie látky, podobne ako Bouguer-Lambert-Beerov zákon.
Stálosť hrúbky vrstvy pohlcujúcej svetlo (plameň) sa dosahuje pomocou horákov špeciálnej konštrukcie. Metódy atómovej absorpčnej spektrálnej analýzy sú široko používané na analýzu takmer akéhokoľvek technického alebo prírodného objektu, najmä v prípadoch, keď je potrebné určiť malé množstvá prvkov.
Metódy na stanovenie atómovej absorpcie boli vyvinuté pre viac ako 70 prvkov.
^ 2. Elektrochemické metódy analýzy.
Ionometria. Metóda sa používa na stanovenie K iónov , Na , Ca 2 , Mn 2 , F - , ja - , Сl - atď.
Metóda je založená na použití iónovo selektívnych elektród, ktorých membrána je priepustná pre určitý typ iónov (preto je spravidla vysoká selektivita metódy).
Kvantitatívny obsah stanovovaného iónu sa vykonáva buď pomocou kalibračného grafu, ktorý je vynesený v súradniciach E - pC, alebo metódou sčítania. Metóda štandardného pridávania sa odporúča na stanovenie iónov v komplexných systémoch obsahujúcich vysoké koncentrácie cudzorodých látok.
Polarografia. Metóda polarografie striedavého prúdu sa používa na stanovenie toxických prvkov (ortuť, kadmium, olovo, meď, železo).
Metóda je založená na štúdiu kriviek prúd-napätie získaných pri elektrolýze elektrooxidačnej alebo elektroredukčnej látky. Ako indikačná elektróda v polarografii sa najčastejšie používa ortuťová kvapková elektróda, niekedy pevné mikroelektródy - platina, grafit. Ako referenčná elektróda sa používa buď ortuť naliata na dno elektrolyzéra alebo nasýtený kalomelový poločlánok.
Pri zvyšovaní napätia nastáva moment, kedy sa všetky ióny vstupujúce do elektródy v dôsledku difúzie okamžite vybijú a ich koncentrácia vo vrstve blízkej elektróde je konštantná a prakticky sa rovná nule. Prúd pretekajúci obvodom v tomto čase sa nazýva obmedzujúci difúzny prúd.
Kvantitatívna polarografická analýza je založená na použití priamej proporcionálna závislosť veľkosť difúzneho prúdu na koncentrácii určovaného prvku.
^ MINERÁLNE PRVKY
Minerálne (popolové) prvky sa v potravinách nachádzajú vo forme organických a anorganických zlúčenín. Nachádzajú sa v mnohých organických
látky rôznych tried - bielkoviny, tuky, glykozidy, enzýmy atď. Minerálne prvky sa zvyčajne stanovujú v popole po spálení potravinárskych výrobkov, pretože je dosť ťažké presne určiť, ktoré látky a v akom množstve sú tieto prvky zahrnuté.
Úloha minerálnych prvkov v živote ľudí, zvierat a rastlín je obrovská: všetky fyziologické procesy v živých organizmoch prebiehajú za účasti týchto prvkov. Minerálne prvky sa teda v ľudskom a zvieracom organizme podieľajú na plastických procesoch, tvorbe a stavbe tkanív, na metabolizme vody, na udržiavaní osmotického tlaku krvi a iných telesných tekutín, na udržiavaní acidobázickej rovnováhy v organizme, na udržaní osmotického tlaku krvi a iných telesných tekutín. a sú zahrnuté v komplexe látok, ktoré tvoria živé bunky protoplazmy, v zložení niektorých žliaz s vnútornou sekréciou atď.
Minerálne zloženie organizmov sa mení s vekom; starnutím sa pozoruje mineralizácia organizmov. Takže novorodenci obsahujú okolo 34 g minerálov na 1 kg telesnej hmotnosti, u dospelého človeka obsah týchto látok stúpa na 43 g a viac.
V ľudskom a zvieracom tele sa našlo viac ako 70 minerálnych prvkov. Mnohé enzymatické procesy prebiehajúce v rôznych tkanivách tela vyžadujú účasť množstva minerálnych prvkov. Takže na premenu kyseliny pyrohroznovej na kyselinu octovú alebo glukózy na fruktózu alebo fosfoglycerol na glukóza-6-manóza-6- a fruktóza-6-fosfát je potrebná účasť horčíkových iónov. Vápenaté ióny inhibujú vývoj tohto procesu.
Minerály sú v tkanivách ľudského tela nerovnomerne rozložené. V tvrdých tkanivách prevládajú dvojmocné prvky: vápnik (Ca) a horčík (Mg) a v mäkkých tkanivách monovalentné prvky: draslík (K) a sodík (Na). Okrem toho sa v tvrdých tkanivách hromadí veľa fosforu (P), hlavne vo forme fosfátových solí. Pri nedostatku minerálov v potrave sa tieto zlúčeniny vylučujú z tela a dochádza k narušeniu normálneho metabolizmu.
Minerálne látky rozpustené v krvnej plazme, medzibunkových a iných telesných tekutinách vytvárajú určitý osmotický tlak, ktorý závisí od molárnej koncentrácie látok rozpustených v tekutine. Soli zvyšujú osmotický tlak vo väčšej miere
stupňa ako neelektrolyty pri rovnakej molárnej koncentrácii, pretože soli disociujú za vzniku iónov. Osmotický tlak závisí od celkového počtu nedisociovaných molekúl a iónov. Osmotický tlak krvi, lymfy a medzibunkovej tekutiny ľudského a zvieracieho tela závisí najmä od chloridu sodného (NaCl), ktorý je v nich rozpustený.
Osmotický tlak v telesných tekutinách ovplyvňuje distribúciu vody a rozpustených látok v tkanivách. U vyšších zvierat je osmotický tlak konštantný a dosahuje 7,5 - 9,0 atm. Udržiavanie stáleho osmotického tlaku je zabezpečené činnosťou vylučovacích orgánov, hlavne obličiek a potných žliaz.
Vstupom minerálnych solí do krvi dochádza k vstupu medzibunkovej vody do krvi, a preto koncentrácia soli v krvi klesá. Prebytočnú vodu a soľ potom odstránia obličky. Pokles vody v tkanivách, reflexne pôsobiaci na nervové centrá, spôsobuje smäd.
Normálna životná aktivita ľudského tela môže prebiehať len s určitými vlastnosťami medzibunkových a intersticiálnych tekutín. V tejto stálosti prostredia zohráva dôležitú úlohu acidobázická rovnováha, pri ktorej je reakcia krvi, lymfy a iných telesných tekutín takmer neutrálna. Acidobázická rovnováha je udržiavaná o komplexný systém regulátory zjednotené do jednej centrály nervový systém. Takýmito regulátormi sú krvné pufrovacie systémy, výmena kyslíka a oxidu uhličitého, oxidu uhličitého a chloridových solí, vylučovacie funkcie obličiek, pľúc, potných žliaz atď.
V procese komplexnej premeny potravín bohatých na vápnik, horčík, sodík alebo draslík v ľudskom tele môžu vznikať zásadité zlúčeniny. Medzi zdroje zásadotvorných prvkov patrí ovocie, zelenina, strukoviny, mlieko a mliečne výrobky.
Ostatné produkty, ako je mäso, ryby, vajcia, syr, chlieb, obilniny, cestoviny, v procese transformácie v ľudskom tele dávajú kyslé zlúčeniny.
Charakter výživy môže ovplyvniť posuny v acidobázickej rovnováhe v tkanivách ľudského tela. Acidobázická rovnováha sa často posúva na > stranu kyslosti. V dôsledku prudkého posunu
prípustné maximálne normy pre obsah popola a pri hodnotení takýchto produktov určujú jeho množstvo.
Zvyčajne sa rozlišujú dva pojmy - „celkový (surový) popol“ a „čistý popol“. Pojem „celkový popol" znamená súhrn minerálnych prvkov alebo ich oxidov, ktoré sú súčasťou chemickej štruktúry potravinárskych výrobkov, ako aj vložené do výrobku počas jeho výroby alebo „náhodne zachytené ako nečistoty. „Čistý popol" znamená súhrn minerálnych prvkov alebo ich oxidov bez nečistôt .
Obsah popola vo výrobku sa zisťuje spaľovaním. Na tento účel sa vzorka najskôr opatrne spáli a potom sa kalcinuje na konštantnú hmotnosť. Zvýšené množstvo popola oproti norme naznačuje kontamináciu produktu pieskom, kovovými časticami a zeminou.
Na stanovenie "čistého popola" sa výsledný popol spracuje s 10% kyselinou chlorovodíkovou. V tomto prípade sa „čistý popol“ rozpustí v kyseline chlorovodíkovej a zvyšok bude indikovať prítomnosť cudzích anorganických nečistôt v produkte. Takže v prípade zlého umývania paradajok pred spracovaním alebo v zemiakovom škrobe pri nedostatočnom umývaní hľúz dochádza k zvýšenému množstvu popola v dôsledku cudzích minerálnych nečistôt.
Vápnik v ľudskom tele sa nachádza v kostnom tkanive a zuboch - asi 99%. Zvyšok vápnika vstupuje do krvi vo forme iónov a v stave spojenom s proteínmi a inými zlúčeninami.
Denná potreba vápnika dospelého človeka je 0,8 – 1,0 g Zvýšené množstvo vápnika potrebujú tehotné a dojčiace ženy, až 1,5 – 2 g denne, ako aj deti, v organizme ktorých sa vápnik intenzívne využíva na tvorbu kostí. Nedostatok vápnika spôsobuje v tele deformáciu kostry, krehkosť kostí a svalovú atrofiu. Vápnik sa vyznačuje tým, že aj pri jeho nedostatku v potrave sa naďalej vylučuje z tela vo významných množstvách.
Vápnik sa nachádza v potravinárskych výrobkoch vo forme fosfátových a oxalátových chloridových solí, ako aj v kombinácii s mastnými kyselinami, bielkovinami atď.
Všetky zlúčeniny vápnika, s výnimkou CaC! a, sú ťažko rozpustné vo vode, a preto sa zle vstrebávajú
ľudské telo. Nerozpustné zlúčeniny vápnika čiastočne prechádzajú z produktov do roztoku v žalúdku pôsobením kyseliny chlorovodíkovej tráviace šťavy. Absorpcia vápnika v potravinách ľudským organizmom závisí vo veľkej miere od prítomnosti fosfátov, tukov, zlúčenín horčíka atď.. Absorpcia vápnika je teda najvyššia, keď pomer vápnika a fosforu I v potravinách ; 1,5 alebo 1: 2. Množstvo fosforu v potravinách zvýšené oproti uvedeným pomerom vedie k prudkému zníženiu absorpcie vápnika. Nadbytok horčíka má tiež nepriaznivý vplyv na vstrebávanie vápnika ľudským organizmom. Prudko negatívny vplyv na vstrebávanie vápnika majú zlúčeniny vápnika s kyselinou inozitol-fosforečnou, ktorá sa vo významnom množstve nachádza v obilných zrnách a produktoch ich spracovania.
Veľmi dôležitú úlohu pri vstrebávaní vápnika zohráva vitamín D, ktorý podporuje prechod solí vápnika a fosforu z čriev do krvi a ukladanie v kostiach vo forme fosforečnanu vápenatého.
Obsah vápnika v niektorých potravinárskych výrobkoch je nasledovný (mg%): v chudom mäse - 7; vo vajciach - 54; v mlieku - 118; v syre - 930; v tvarohu - 140; v ovsených vločkách - 65; v pšeničnej múke - 15; v ryži - 9; v jablkách - 7; v pomarančoch - 45; vo vlašských orechoch -89; v repe - 29; v karfiole - 89; v bielej kapuste - 45; v mrkve - 56; v zemiakoch - 14. Z uvedených údajov je vidieť, že najvýznamnejším zdrojom vápnika pre človeka sú mliečne výrobky. Vápnik v mliečnych výrobkoch, ako aj v zelenine a ovocí, je ľahko stráviteľná zlúčenina.
Horčíka je v ľudskom tele 30-35 krát menej ako vápnika, no je veľmi dôležité. Väčšina horčíka sa nachádza v kostnom tkanive. Horčík hrá zvláštnu úlohu v rastlinách nesúcich chlorofyl, kde je súčasťou molekuly chlorofylu. Podobne ako vápnik aj horčík tvorí ťažko rozpustné zlúčeniny. Horčík je obzvlášť ťažké asimilovať v prítomnosti iónu LO$.
Obsah horčíka v niektorých potravinárskych výrobkoch je nasledujúci (mg%): vo fazuli - 139; v ovsených vločkách - 133; v hrášku - 107; v prose - 87; v pšeničnom chlebe - 30; v zemiakoch - 28; v mrkve - 21; v bielej kapuste -! Anna - 12; v jablkách - 8; v citrónoch - 7; v hovädzom mäse - 15; vo vajciach - 11; v mlieku - 12. V dôsledku toho sa 2 * 35 horčíka nachádza v najväčšom množstve v obilninách a strukovinách.
Potreba horčíka pre dospelého človeka je 400 mg denne.
Sodík je široko obsiahnutý v potravinách, najmä v živočíšnych produktoch. Hlavným zdrojom sodíka pre ľudský organizmus je NaCt (obyčajná soľ). Sodík hrá dôležitú úlohu v procesoch intracelulárneho a medzitkanivového metabolizmu. Asi 90 % osmotického tlaku krvnej plazmy závisí od obsahu NaCl v nej. Typicky sa 3,3 g sodíka rozpustí v litri ľudskej krvnej plazmy. NaC! Tiež zohráva dôležitú úlohu pri regulácii vodného metabolizmu v tele. Sodné ióny spôsobujú opuch tkanivových koloidov a tým prispievajú k zadržiavaniu viazanej vody v tele. Z tela NaC! vylučuje hlavne močom a potom. Pri zvýšenej práci a konzumácii tekutín človek stratí až 3-5 litrov potu, čo je 99,5 % vody. V sušine potu je hlavná časť NaGI.
Kuchynská soľ, ktorá sa do ľudského tela dostáva s potravou, doplňuje spotrebu NaCI v krvi a používa sa na tvorbu kyseliny chlorovodíkovej v žalúdočnej šťave, ako aj na syntézu NaHCO3 pankreasovou žľazou. Prítomnosť NaHCO3 vysvetľuje alkalickú reakciu pankreatickej šťavy, ktorá je nevyhnutná pre rozklad potravinových bielkovín enzýmom trypsínom.
Denná potreba sodíka u dospelého človeka je 4-6 g, čo zodpovedá 10-15 g kuchynskej soli. Bežná strava obyvateľstva obsahuje dostatočné množstvo sodíka, keďže do jedla sa pridáva kuchynská soľ.
Draslík je neustále a vo významných množstvách prítomný v potravinách, najmä rastlinného pôvodu.V popole rastlín je obsah draslíka niekedy viac ako 50 % jeho hmotnosti.
V ľudskom tele sa draslík podieľa na enzymatických reakciách, tvorbe tlmivých systémov, ktoré zabraňujú posunom v reakcii prostredia. Draslík sa znižuje
schopnosť bielkovín zadržiavať vodu, čím sa znižuje ich hydro-schopnosti, a tým sa podporuje vylučovanie vody a sodíka z tela, preto možno draslík považovať za nejakého fyziologického antagonistu sodíka.
Denná potreba draslíka u dospelého človeka je 3-5 g.
Železo je v prírode široko rozšírené. Vo všeobecnosti takmer všetky prírodné potraviny obsahujú železo, ale v malom množstve.
V ľudskom a živočíšnom organizme je železo súčasťou najdôležitejších organických zlúčenín - hemoglobínu v krvi, myoglobínu, niektorých enzýmov - katalázy, peroxidázy, cytochrómoxidázy atď. Krvný hemoglobín obsahuje 2A, telesné železo. Významné množstvo železa sa nachádza v slezine a pečeni. Železo má schopnosť hromadiť sa v tele. Hemoglobín v krvi sa počas života ničí a železo uvoľnené v tomto prípade môže telo znovu využiť na tvorbu hemoglobínu.
Železo, ktoré je súčasťou ovocia a zeleniny, sa ľudským organizmom dobre vstrebáva, pričom väčšina železa v cereálnych výrobkoch je pre telo v nestráviteľnej forme.
Denná potreba dospelej ľudskej žľazy je 15 mg.
l l o r je súčasťou prirodzených potravín v malom množstve. Rastlinné produkty obsahujú málo chlóru, zatiaľ čo živočíšne produkty obsahujú o niečo viac. Takže obsah chlóru v hovädzom mäse je 76 mg%, v mlieku - 106, vo vajciach -
37106, v syre - 880, v prose - 19, v zemiakoch - 54, v jablkách - 5 mg%.
Významný je obsah chlóru v krvi a iných telesných tekutinách, ako aj v koži, pľúcach a obličkách. Chlór je v organizme v ionizovanom stave vo forme aniónov solí sodíka, draslíka, vápnika, horčíka, mangánu. Zlúčeniny chlóru v potravinách sú vysoko rozpustné a ľahko sa vstrebávajú v ľudskom čreve. Anióny chlóru spolu s katiónmi sodíka zohrávajú dôležitú úlohu pri vytváraní a regulácii osmotického tlaku krvi a iných telesných tekutín. Soli chlóru zabezpečujú tvorbu kyseliny chlorovodíkovej žalúdočnou sliznicou.
Hlavnú potrebu chlóru uspokojuje chlorid sodný, ktorý sa do potravín pridáva vo forme soli.
Celkové množstvo chloridu sodného v ľudskom tele je zvyčajne 10-15 g, ale pri konzumácii potravín bohatých na chlórové soli môže obsah chlóru v ľudskom organizme dosiahnuť vyššie množstvo. Denná ľudská potreba chlóru je 5-7 g.
Síra sa v najvyšších množstvách nachádza v obilných výrobkoch, strukovinách, mliečnych výrobkoch, mäse, rybách a najmä vajciach. Je súčasťou takmer všetkých bielkovín ľudského tela a hojne sa v ňom nachádzajú najmä aminokyseliny – cystín, metionín. Výmena síry v organizme je najmä jej premena na uvedené aminokyseliny. Podieľa sa aj na tvorbe vitamínu Bg (tiamín), inzulínu a niektorých ďalších zlúčenín. V proteinoidoch podporných tkanív je veľa síry, napríklad v keratíne vlasov, nechtov atď.
Pri oxidácii zlúčenín v tele sa významná časť síry vylučuje močom vo forme solí kyseliny sírovej.
Denná potreba dospelého človeka na síru pri miernej práci je asi 1 g.
Jód je obsiahnutý v tele zdravého človeka s hmotnosťou 70 kg v množstve približne 25 mg. Polovica tohto množstva je v štítnej žľaze a zvyšok je vo svalovom a kostnom tkanive a v krvi. Anorganické zlúčeniny jódu v štítnej žľaze sú nahradené Organické zlúčeniny- tyroxín, dijódtyroxín, trijódtyroxín. Jód sa rýchlo vstrebáva štítnou žľazou a niekoľko hodín po vstupe do nej sa mení na organickú
spojenia. Tieto zlúčeniny stimulujú metabolické procesy v tele. Keď sa s potravou dostane do tela nedostatočné množstvo jódu, naruší sa činnosť štítnej žľazy a vznikne závažné ochorenie nazývané endemická struma.
Najväčšie množstvo jódu sa nachádza v rastlinných a živočíšnych produktoch pobrežných oblastí, kde sa koncentruje v morskej vode, vzduchu a pôde pobrežných oblastí. Málo jódu sa hromadí v rastlinách a živočíšnych organizmoch horských alebo vzdialených od morských pobrežných oblastí jódu.
Obsah jódu v obilných výrobkoch, zelenine, sladkovodných rybách nepresahuje 5-8 mcg na 100 g surového produktu. Hovädzie mäso, vajcia, maslo, ovocie sa vyznačujú vyšším obsahom jódu. morská kapusta, morské ryby a rybí olej obsahujú najvyššie množstvo jódu. Plody Feijoa rastúce na pobreží Čierneho mora v Gruzínsku akumulujú až 390 mikrogramov jódu na 100 g ovocnej hmoty, čo je oveľa viac ako obsah tohto prvku v inom ovocí a zelenine.
V oblastiach, kde potravinárske výrobky obsahujú nedostatočné množstvo jódu, sa do kuchynskej soli pridáva jodid draselný v množstve 25 g K1 na tonu kuchynskej soli. Pri bežnej strave človek prijme 200 mikrogramov jódu denne s jódovanou soľou. Pri skladovaní jódovanej soli sa však jód postupne vytráca, preto sa po 6 mesiacoch jódovaná soľ predáva ako obyčajná kuchynská soľ.
Denná ľudská potreba jódu je 100-260 mcg.
Fluór hrá dôležitú úlohu v plastických procesoch pri tvorbe kostného tkaniva a zubnej skloviny. Najväčšie množstvo fluóru sa koncentruje v kostiach - 200-490 mg/kg a zuboch - 240-560 mg/kg.
Zdá sa, že voda je hlavným zdrojom fluoridu v ľudskom tele, pričom fluorid Doda sa vstrebáva lepšie ako fluorid z potravy. Obsah fluóru v pitnej vode sa pohybuje od 1 do 1,5 mg/l. Nedostatok fluóru vo vode často ovplyvňuje
39nne k rozvoju ochorenia zubov, známeho ako kaz. Nadbytok fluóru vo vode spôsobuje fluorózu, ktorá narúša normálnu stavbu zubov, na sklovine vznikajú škvrny a zvyšuje sa krehkosť zubov. Nedostatkom alebo nadbytkom fluóru trpia najmä deti.
Denná ľudská potreba fluóru ešte nebola stanovená. Predpokladá sa, že optimálne množstvo fluoridu v pitnej vode pre zdravie by malo byť 0,5-1,2 mg/l.
Meď v organizme zvierat spolu so železom zohráva dôležitú úlohu v procesoch krvotvorby, stimuluje oxidačné procesy a je tak spojená s metabolizmom železa. Je súčasťou enzýmov (laktáza, askorbátoxidáza, cytochrómoxidáza atď.) ako kovová zložka.
V rastlinách meď podporuje oxidačné procesy, urýchľuje rast a zvyšuje úrodu mnohých plodín.
V tých malých množstvách, v ktorých sa meď nachádza v prírodných produktoch, nepoškodzuje ľudské telo. Ale zvýšené množstvo medi môže spôsobiť otravu. Takže súčasný príjem 77-120 mg medi môže spôsobiť nevoľnosť, vracanie a niekedy hnačku. Preto obsah medi v potravinárskych výrobkoch upravujú súčasné predpisy Ministerstva zdravotníctva ZSSR. Na 1 kg produktu je v závislosti od obsahu pevných látok v ňom povolených 5 až 30 mg medi. Takže v koncentrovanej paradajkovej paste by obsah medi nemal prekročiť 30 mg / kg, v paradajkovom pretlaku - 15-20, v konzervovanej zelenine - 10, v džeme a marmeláde - 10, v ovocných kompótoch - 5 mg / kg.
Meď sa môže dostať do potravinárskych výrobkov pri ich výrobe – z medených častí zariadení, pri ošetrovaní viníc pesticídmi s obsahom medi atď.
Denná potreba medi u dospelého človeka je 2 mg.
Zinok sa nachádza vo všetkých tkanivách zvierat a rastlín. S nedostatkom zinku v organizme mladých žien,
U rastlín sa ich rast oneskoruje a pri jeho nedostatku v pôde dochádza k chorobám mnohých rastlín, čo často vedie k ich úhynu.
Zinok je súčasťou množstva enzýmov a dôležitá je najmä jeho úloha v molekule enzýmu karboanhydrázy, ktorá sa podieľa na väzbe a vylučovaní oxidu uhličitého z tela zvieraťa. Zinok je nevyhnutný pre normálnu funkciu hormónov hypofýzy, nadobličiek a pankreasu. Má tiež vplyv na metabolizmus tukov, zvyšuje odbúravanie tukov a zabraňuje stukovateniu pečene.
Zinok v potravinách vo vysokých množstvách môže spôsobiť otravu. Kyslé a mastné potraviny rozpúšťajú kovový zinok, a preto je varenie alebo skladovanie potravín v zinkových zariadeniach alebo nádobách neprijateľné. Otrava zinkom je podobná otrave meďou, je však výraznejšia a sprevádza ju pálenie a bolesť v ústach a žalúdku, vracanie, hnačka a srdcová slabosť. Zinkový riad je povolený len na skladovanie studenej pitnej vody, pretože v tomto prípade je rozpustnosť zinku zanedbateľná.
Denná potreba zinku u dospelého človeka je 10-15 mg. Zvýšená potreba zinku sa pozoruje počas rastu a puberty. Pri bežnej strave človek prijíma dostatočné množstvo zinku z potravy.
Olovo sa nachádza v živočíšnych a rastlinných produktoch vo veľmi malých množstvách. Takže v jablkách, hruškách, hrozne, jahodách je obsah olova asi 0,1 mg na 1 kg výrobku, v mlieku - 0,8, v mäse - 0,05, v jeseterovi - 0,06 mg na 1 kg.
Olovo je pre človeka toxický kov, má schopnosť hromadiť sa v organizme, hlavne v pečeni, a spôsobovať ťažké chronické otravy.
Pri dennom užívaní 2-4 mg olova s jedlom sa po niekoľkých mesiacoch môžu objaviť príznaky otravy olovom.
41 Kontaminácia potravín olovom môže pochádzať z náradia, spájok, glazúr, zariadení a insekticídov obsahujúcich olovo. Najčastejšie k otrave olovom dochádza pri skladovaní potravín v remeselnej kamenine, ktorá nie je dobre pokrytá olovenou glazúrou.
Vzhľadom na vysokú toxicitu nie je povolený obsah olova v potravinárskych výrobkoch.
Cín sa v potravinách nachádza v malom množstve. V pečeni býka a barana sa teda našlo 0,14 mg/kg cínu, 0,003 v obličkách, 0,63 v pľúcach a 0,019 mg/kg v mozgu.
Cín nie je taký toxický kov ako olovo, zinok alebo meď, preto je povolený v obmedzenom množstve v zariadeniach potravinárskych podnikov, ako aj na pocínovanie povrchu cínu, z ktorého sa pripravujú plechovky, ktoré ho chránia pred koróziou. Často však pri dlhodobom skladovaní konzervovaných potravín v konzervách dochádza k interakcii hmoty výrobku s cínovým povlakom cínu, v dôsledku čoho vznikajú cínové soli organických kyselín. Tento proces je obzvlášť aktívny, keď sú v plechovke výrobky s vysokou kyslosťou - ovocie, konzervované ryby a zelenina paradajková omáčka a iné.Pri dlhodobom skladovaní sa môže výrazne zvýšiť obsah cínu v konzervách. Obsah cínu sa obzvlášť rýchlo zvyšuje vo výrobkoch, ktoré sú v otvorených kovových plechovkách potiahnutých cínom.
Na zvýšenie ochrany plechovky proti korózii sa na povrch plechovky dodatočne nanášajú špeciálne kyselinovzdorné laky alebo emaily, prípadne sa na povrchu plechovky vytvorí tenký film stabilných oxidov cínu.
Mangán je široko distribuovaný v živočíšnych a rastlinných produktoch. Aktívne sa podieľa na tvorbe mnohých enzýmov, tvorbe kostí, procesoch hematopoézy a stimuluje rast. V rastlinách mangán podporuje proces fotosyntézy a tvorbu kyseliny askorbovej.
Rastlinné produkty sú vo väčšine prípadov bohatšie na mangán ako živočíšne produkty. Takže obsah mangánu v obilných výrobkoch dosahuje 1-15 mg na 1 kg v liste
zelenina - 10-20, v ovocí - 0,5-1, v mlieku - 0,02-0,03, vo vajciach - 0,1-0,2, v pečeni zvierat - 2,65-2,98 mg na 1 kg.
Pri nedostatku mangánu v pôde rastliny ochorejú a zle sa vyvíjajú, úroda ovocia, zeleniny a iných plodín klesá. Pridávanie mikrohnojív s obsahom mangánu do pôdy pomáha zvýšiť úrodu.
Denná potreba dospelého človeka na mangán je 5-10 mg denne.
Rádioaktívne izotopy sú prítomné v ľudskom tele, neustále vstupujú a vystupujú z tela. Existuje rovnováha medzi príjmom rádioaktívnych zlúčenín do tela a ich odstránením z tela. Všetky potravinárske výrobky obsahujú rádioaktívne izotopy draslíka (K40), uhlíka (C14), vodíka (H3) a tiež rádia s jeho produktmi rozpadu.
Najvyššia koncentrácia pripadá na draslík (K40). Izotopy sa podieľajú na metabolizme spolu s nerádioaktívnymi.
Predpokladá sa, že v najbližšom geologickom čase nenastali na Zemi žiadne veľké zmeny v intenzite žiarenia, teda u zvierat a flóry vyvinula akúsi imunitu voči týmto úrovniam žiarenia. Ale živé organizmy sú veľmi citlivé na zvýšené koncentrácie. Malé koncentrácie zvyšujú rast živých organizmov, veľké koncentrácie spôsobujú výskyt aktívnych radikálov, v dôsledku čoho dochádza k narušeniu životnej činnosti jednotlivých orgánov a tkanív, ako aj celého organizmu.
O atómové výbuchy rádioaktívne izotopy dopadajú na zemský povrch a znečisťujú atmosféru, vodu, pôdu a rastliny. Prostredníctvom potravy, atmosféry a vody sa rádioaktívne izotopy dostávajú do ľudského tela.
Zistilo sa, že keď sú potravinárske výrobky ošetrené žiarením rádioaktívnych izotopov, ich skladovateľnosť sa zvyšuje a klíčenie zemiakov sa oneskoruje. Zvyčajne však ožiarené jedlo môže vyvinúť špecifickú vôňu a chuť a je možné, že sa môžu vytvárať toxické látky. Na určenie bezpečnosti takýchto produktov sú potrebné dlhodobé experimenty.
testovacie otázky
Aké chemické prvky sú makroživiny?
Aké sú funkcie minerálov v ľudskom tele?
Aká je úloha vápnika v ľudskom tele?
Aké chemické prvky sú klasifikované ako stopové prvky a aké sú ich funkcie v ľudskom tele?
Akú úlohu hrá železo v ľudskom tele a v akých potravinách sa nachádza?
Aké sú dôsledky nedostatku jódu v tele a ako sa tomu dá vyhnúť?
Aké druhy technologického spracovania surovín a potravinárskych výrobkov prispievajú k úbytku minerálov?
Uveďte príklady vzájomného pôsobenia niektorých mikroelementov a vitamínov.
Aké metódy na stanovenie obsahu makro- a mikroprvkov poznáte?