Minerálne prvky.doc
Minerály1. Úloha minerálnych prvkov v ľudskom organizme 1
2. Makronutrienty, ich charakteristika
3. Stopové prvky, ich charakteristika
4. Vplyv technologického spracovania
O minerálnom zložení potravinárskych výrobkov
5. Metódy stanovenia minerálnych látok
1. Úloha minerálnych prvkov v ľudskom organizme
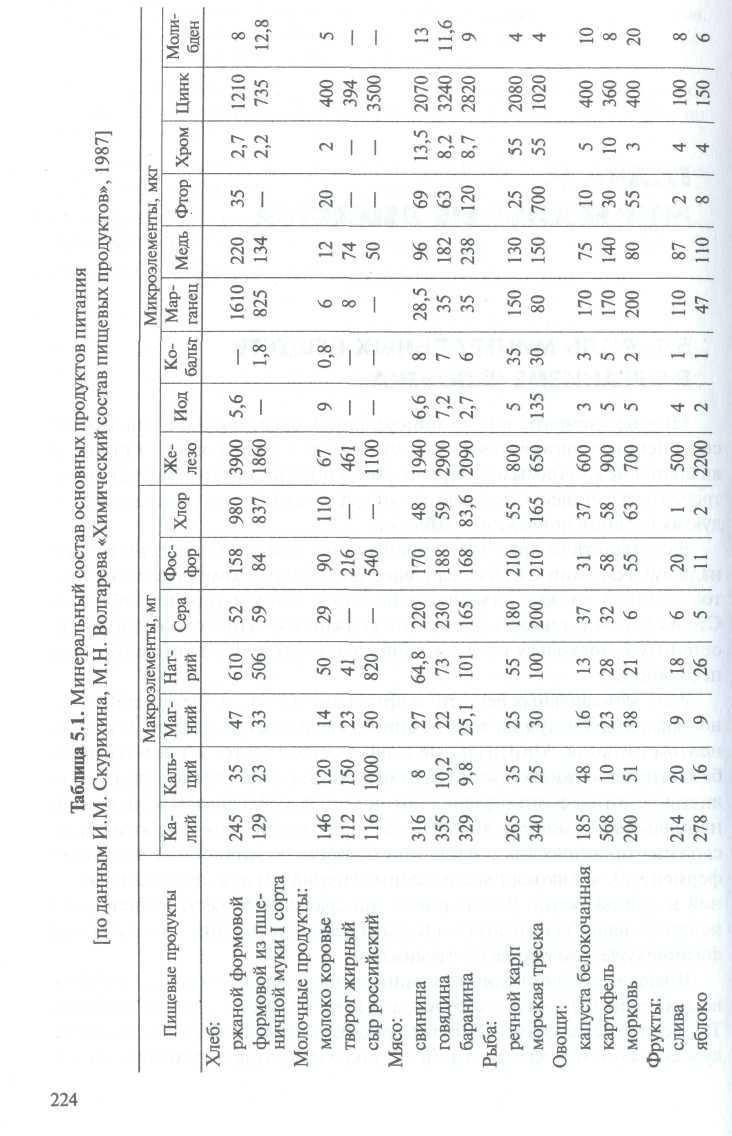
Mnoho prvkov vo forme minerálnych solí, iónov, komplexných zlúčenín a organickej hmoty sú súčasťou živej hmoty a sú základnými živinami, ktoré sa musia denne konzumovať s jedlom. Obsah minerálnych látok v hlavných potravinách je uvedený v tabuľke. 5.1.
Ako zistiť nedostatok horčíka v tele?
Prvým znakom esenciálnych kovov je zvrátenie symptómov a obnovenie optimálneho rastu u dobytka. V priebehu času viedli biochemické štúdie k izolácii enzýmov, ktoré vyžadovali fungovanie kovových iónov, a čoskoro potom mohli byť tieto špecifické enzýmy spojené so symptómami nedostatku.
Zmeny v tráviacom systéme
Interakcie kovových iónov sa považovali za škodlivé, ako aj cenné pre systém. Napríklad skorá štúdia ukázala, že meď zvyšuje účinky železa pri zmierňovaní anémie u laboratórnych potkanov kŕmených mliečnou stravou; toto pozorovanie sa zopakovalo u kurčiat a ošípaných a čoskoro pritiahlo pozornosť lekárov, ktorí prijali podobný bimetalový protokol na liečbu anemických ľudí. Spolu s príchodom poločistej stravy v rovnakom čase bola nutričná veda na pokraji dôležitých objavov o úlohe základných minerálnych prvkov.
Podľa odporúčaní dietetického výboru Národná akadémia USA by mal byť denný príjem chemických prvkov s jedlom na určitej úrovni (tabuľka 5.2). Denne sa musí z tela vylúčiť rovnaký počet chemických prvkov, keďže ich obsah v ňom je relatívne konštantný.
Minerálne kofaktory obsahujú veľká skupina anorganické látky s väčšinou kovových iónov. Doména kovových iónov zahŕňa makrokovy, stopové ióny kovov a metaloidy. Pri hľadaní dôvodu ich nevyhnutnosti musíme pochopiť, že kovové ióny sú vhodné na vykonávanie nebezpečných chemických reakcií na enzymatických povrchoch, reakcií, ktoré by mohli poškodiť citlivejšie organické aminokyselinové bočné reťazce v enzýme. Napríklad redoxné kovy, ako je železo, mangán a meď, môžu prijať elektróny vo svojej štruktúre, dočasne ich zadržať a potom ich preniesť do kyslíka za vzniku vody, čo je spôsob, ako bezpečne odstrániť elektrón.
Úloha minerálov v ľudskom organizme je mimoriadne rôznorodá, napriek tomu, že nie sú podstatnou zložkou výživy. Minerálne látky sú obsiahnuté v protoplazme a biologických tekutinách, zohrávajú významnú úlohu pri zabezpečovaní stálosti osmotického tlaku, ktorý je nevyhnutnou podmienkou pre normálne fungovanie buniek a tkanív. Sú súčasťou komplexu Organické zlúčeniny(napríklad hemoglobín, hormóny, enzýmy), sú plastickým materiálom na stavbu kostného a zubného tkaniva. Vo forme iónov sa minerálne látky podieľajú na prenose nervových vzruchov, zabezpečujú zrážanlivosť krvi a ďalšie fyziologické procesy organizmu.
V podstate treba brať do úvahy, že kofaktor kovu rozširuje repertoár dostupných katalytických funkcií a je vykonávaný enzýmami. Enzýmy, ktoré závisia od kovových iónov ako kofaktorov, spadajú do 2 kategórií: kovom aktivované enzýmy a metaloenzýmy. Ako už názov napovedá, kovom aktivované enzýmy sú stimulované k vyššej katalytickej aktivite prítomnosťou jednomocného alebo dvojmocného kovového iónu na vonkajšej strane proteínu. Kov môže aktivovať substrát, priamo viazať enzým alebo sa dostať do rovnováhy s enzýmom pomocou svojho iónového náboja, aby získal priaznivejšiu väzbu so substrátom alebo lepšie katalytické prostredie.
 |
V závislosti od množstva minerálov v ľudskom tele a potravinových výrobkoch sa delia na makro- a stopové prvky. Ak teda hmotnostný podiel prvku v tele presiahne 10 -2%, potom by sa mal považovať za makroprvok. Podiel stopových prvkov v organizme je 10 -3 -10 -5%. Ak je obsah prvku pod 10 -5 %, považuje sa za ultramikroprvok. Medzi makroživiny patrí draslík, sodík, vápnik, horčík, fosfor, chlór a síra. Sú obsiahnuté v množstvách meraných v stovkách a desiatkach miligramov na 100 g tkaniva alebo potraviny. Stopové prvky sú súčasťou tkanív tela v koncentráciách vyjadrených v desatinách, stotinách a tisícinách miligramu a sú nevyhnutné pre jeho normálne fungovanie. Stopové prvky sú podmienene rozdelené do dvoch skupín: absolútne alebo životne dôležité (kobalt, železo, meď, zinok, mangán, jód, bróm, fluór) a takzvané pravdepodobne nevyhnutné (hliník, stroncium, molybdén, selén, nikel, vanád a niektoré ďalšie). ). Stopové prvky sa nazývajú životne dôležité, ak je pri ich nedostatku alebo nedostatku narušené normálne fungovanie tela.
Rozloženie stopových prvkov v organizme závisí od ich chemických vlastností a je veľmi rôznorodé. Železo je napríklad neoddeliteľnou súčasťou hemoglobínu, myoglobínu a iných respiračných pigmentov, teda látok, ktoré sa podieľajú na absorpcii a transporte kyslíka do všetkých tkanív tela; atómy medi sú zahrnuté v aktívnom centre množstva enzýmov atď.
Preto enzýmy aktivované kovom vyžadujú, aby bol kov prítomný v nadbytku, možno 2-10-násobku koncentrácie enzýmu. Pretože sa kov nemôže viazať trvalejším spôsobom, kovom aktivované enzýmy zvyčajne strácajú aktivitu počas čistenia.
Naproti tomu kovové enzýmy majú kovový kofaktor pevne naviazaný na špecifickú oblasť na povrchu proteínu. Až na niekoľko výnimiek vstupujú do obrazu stopové kovy ako kofaktory kovových enzýmov. Silné spojenie znemožňuje stratu kovového iónu dialýzou alebo stratu slabými disociačnými činidlami. Kovové enzýmy však môžu stratiť svoj kovový kofaktor a stať sa neaktívnymi, keď sú ošetrené kovovými chelátormi, ktoré majú silnejšiu väzbovú afinitu ako enzým a prekonávajú enzýmový proteín kovovým iónom.
Pôsobenie mikroprvkov môže byť aj nepriame – prostredníctvom vplyvu na intenzitu alebo charakter metabolizmu. Takže niektoré mikroelementy (napríklad mangán, zinok, jód) ovplyvňujú rast a ich nedostatočný príjem s jedlom bráni normálnemu fyzický vývoj dieťa. Ostatné stopové prvky (napríklad molybdén, meď, mangán) sa podieľajú na reprodukčnej funkcii a ich nedostatok v organizme negatívne ovplyvňuje túto stránku ľudského života.
Ako prostetické skupiny majú kovy v metaloenzýmoch stechiometrický pomer reprezentovaný úplným integrátorom. Metaloenzýmy sa zriedkavo pripravujú na zvýšenie aktivity pridaním ich konjugovaného kovového iónu k enzýmu. Priestorová geometria je tiež problémom: kovy v prvej sérii prechodných javov musia dodržiavať prísne geometrické konfigurácie okolo miesta spájania kovu.
S výnimkou tých so zinkom, enzýmy s kovmi z prvej prechodnej série majú tendenciu byť veľmi svetlé; napríklad červená farba hemoglobínu resp modrá farba ceruloplazmín spojený s meďou. Väčšina enzýmov kombinuje železo so železom buď ako hem, alebo ako špeciálne usporiadanie železa so sírovými skupinami, známymi ako železo-sírové centrá. Železo v heme vykazuje silnú afinitu k iónom horčíka v chlorofyle. Hem, čo je v podstate porfyrínový kruhový systém so železom umiestneným v strede, je najrozšírenejšou formou železa v biologických proteínoch.
K najviac deficitným minerálom v strave moderný človek zahŕňajú vápnik a železo, prebytok - sodík a fosfor.
Nedostatok alebo prebytok akýchkoľvek minerálnych látok v strave spôsobuje narušenie metabolizmu bielkovín, tukov, sacharidov, vitamínov, čo vedie k rozvoju mnohých chorôb. Nižšie sú uvedené charakteristické (typické) príznaky nedostatku rôznych chemických prvkov v ľudskom tele: Najčastejším dôsledkom nesúladu množstva vápnika a fosforu v strave je zubný kaz, rednutie kostí. Pri nedostatku fluóru v pitnej vode sa ničí zubná sklovina, nedostatok jódu v potrave a vode vedie k ochoreniam štítnej žľazy. Minerály sú teda veľmi dôležité pre elimináciu a prevenciu množstva chorôb.
Najbežnejšie pripojenia
Ako súčasť železo-sírových centier železo vstupuje do niekoľkých skupinových schém s cysteínovými zvyškami v enzýmoch, ktoré umožňujú priamejší kontakt s proteínom. Železo v týchto centrách sa viaže na substráty, ako aj prenáša elektróny a zúčastňuje sa reakcií, ktoré zahŕňajú dehydratáciu a preskupenie. Enzýmy s centrami železa a síry zahŕňajú xantínoxidázu, sukcinátdehydrogenázu, akonitázu a kyselinu dusičnú.
Toto usporiadanie umožňuje enzýmu odstrániť atóm vodíka z veľmi stabilného S-N spojenia. Nekov môže nahradiť železo v týchto komplexoch. Enzýmy s hemovou skupinou majú zvyčajne červenohnedú farbu. Farba motivovala počiatočný záujem o tieto proteíny a bola motivačným faktorom pre označovanie hemových proteínov v mitochondriách ako „cytochrómy“.


Uvádzame príčiny porúch metabolizmu minerálnych látok, ktoré sa môžu vyskytnúť aj pri ich dostatočnom množstve v potrave:
A) nevyvážená výživa (nedostatočné alebo nadmerné množstvo bielkovín, tukov, sacharidov, vitamínov atď.);
Hoci len niekoľko rozpustných enzýmov má železo ako kofaktor, železo je obzvlášť významné v membránovo viazaných proteínoch, ktoré obsahujú dráhy transportu elektrónov. Redoxná vlastnosť železa hrá veľkú časť jeho chémie ako kofaktor. Železo sa takmer vždy podieľa na prenose elektrónov a často daruje elektróny molekule kyslíka.
Kataláza aj peroxidáza, dva hemové enzýmy, využívajú železo na interakciu s nebezpečnými oxidantmi. Oba enzýmy sa nachádzajú v cytosóle a v peroxizómoch, kde pri bežných metabolických dejoch dochádza k škodlivým oxidačným reakciám. Asi najznámejším enzýmom obsahujúcim železo je cytochróm c oxidáza, terminálny akceptor elektrónov v mitochondriálnom elektrónovom transportnom reťazci a enzým schopný štiepiť molekulu kyslíka za vzniku vody.
B) používanie spôsobov kulinárskeho spracovania potravín, ktoré spôsobujú stratu minerálov, napríklad pri rozmrazovaní (v horúca voda) mäso, ryby alebo pri odstraňovaní odvarov zo zeleniny a ovocia, kde prechádzajú rozpustné soli;
C) nedostatok včasnej korekcie zloženia stravy, keď sa potreba minerálov v tele z fyziologických dôvodov mení. Napríklad ľudia pracujúci v podmienkach zvýšená teplota vonkajšie prostredie, potreba draslíka, sodíka, chlóru a iných minerálov stúpa vzhľadom na to, že väčšina z nich sa z tela vylučuje potom;
Úloha horčíka v ľudskom tele
Zinok je možno najrozšírenejší a najuniverzálnejší zo všetkých kofaktorov kovov. Viac ako 300 enzýmov má kofaktor zinku. Približne 3 % genómu cicavcov kódujú proteíny zinkových prstov. Ako kofaktor môže zinok vykonávať štrukturálne aj katalytické funkcie. Tieto príklady ilustrujú, prečo je zinok dôležitým spoločníkom pre enzýmy a bielkoviny.
Zinok sa považuje za mäkký kov, pretože sa správa ako dvojmocný katión bez väčších geometrických preferencií. Možno táto mäkkosť umožňuje zinku prispôsobiť sa mnohým rôznym fermentačným prostrediam. Z tohto dôvodu sú komplexy zinku bezfarebné a samotný zinok sa správa primárne ako katión. Ďalším príkladom je použitie zinku na polarizáciu esterovej alebo amidovej väzby, čím sa uľahčí nukleofilný atak vody na zlúčeninu, ako pri reakciách katalyzovaných karboxypeptidázou a aminopeptidázou.
D) porušenie procesu absorpcie minerálov v gastrointestinálnom trakte alebo zvýšená strata tekutín (napríklad strata krvi).
^
2. Makronutrienty, ich charakteristika
Vápnik. Je hlavnou stavebnou zložkou kostí a zubov; je súčasťou jadier buniek, bunkových a tkanivových tekutín, je nevyhnutný pre zrážanie krvi. Vápnik tvorí zlúčeniny s proteínmi, fosfolipidmi, organickými kyselinami; podieľa sa na regulácii permeability bunkových membrán, na prenose nervových vzruchov, na molekulárnom mechanizme svalových kontrakcií, riadi činnosť radu enzýmov. Takže vápnik plní nielen plastické funkcie, ale ovplyvňuje aj mnohé biochemické a fyziologické procesy v organizme.
Meď, podobne ako železo, je redoxný kov. Enzýmy medi, hoci nie sú také početné ako enzýmy zinku, vykonávajú dôležité biologické funkcie, najmä v cytosóle. Medzi najzložitejšie enzýmy patria multicorex oxidázy, ktoré môžu mať len 4 alebo až 8 atómov medi na enzým. Meď v týchto enzýmoch existuje v troch rôznych chemických prostrediach, známych ako medené záplaty typu 1, typu 2 a typu. Medené miesto typu 1 dáva modrú farbu ceruloplazmínom a iným modrým proteínom s meďou.
Väzbové miesta pre meď v polyoxidoxidáze tvoria triádu pozostávajúcu z medi 2 typu 3 a medi typu 3 usporiadaných do rovnoramenného trojuholníka. Kyslík sa viaže na týchto dvoch medikov typu 3 v základni trojuholníka. Kvôli svojej tendencii prijímať elektróny je meď silným oxidačným činidlom v biologických systémoch. Táto reakcia spája metabolizmus železa s meďou a môže vysvetliť, ako nedostatok medi v železe bráni prenosu železa a spôsobuje anémiu u ľudí. Zriedkavo sa vyžaduje, aby meď zohrávala iba štrukturálnu úlohu a mnohé enzýmy, ktoré majú meď ako kofaktor, používajú kov na aktívnom mieste.
Vápnik je ťažko stráviteľný prvok. Zlúčeniny vápnika vstupujúce do ľudského tela s jedlom sú prakticky nerozpustné vo vode. Alkalické prostredie tenkého čreva podporuje tvorbu nestráviteľných zlúčenín vápnika a len pôsobenie žlčových kyselín zabezpečuje jeho vstrebávanie.
Asimilácia vápnika tkanivami závisí nielen od jeho obsahu v potravinách, ale aj od pomeru s ostatnými zložkami potravy a predovšetkým s tukmi, horčíkom, fosforom a bielkovinami. Pri nadbytku tuku dochádza ku konkurencii žlčových kyselín a značná časť vápnika sa vylučuje z tela cez hrubé črevo. Absorpciu vápnika nepriaznivo ovplyvňuje nadbytok horčíka; odporúčaný pomer týchto prvkov je 1:0,5. Ak množstvo fosforu prevyšuje hladinu vápnika v potravinách viac ako 2-krát, tvoria sa rozpustné soli, ktoré sú extrahované krvou z kostného tkaniva. Vápnik sa dostáva do stien ciev, čo spôsobuje ich krehkosť, ako aj do tkanív obličiek, čo môže prispieť k výskytu obličkových kameňov. Pre dospelých je odporúčaný pomer vápnika a fosforu v potravinách 1:1,5. Ťažkosti s udržaním tohto pomeru sú spôsobené tým, že väčšina bežne konzumovaných potravín je oveľa bohatšia na fosfor ako na vápnik. Fytín a kyselina šťaveľová, obsiahnuté v množstve rastlinných produktov, majú negatívny vplyv na vstrebávanie vápnika. Tieto zlúčeniny tvoria nerozpustné soli s vápnikom.
Výskum spájal ióny medi s tvorbou tepien alebo angiogenézou. Jedným z najzaujímavejších objavov, ktorý ešte nebol úplne pochopený, je, že zbavenie zvieraťa medi oneskoruje alebo dokonca brzdí rast rakovinových nádorov. Z nutričného hľadiska to môže znamenať, že meď je nevyhnutná pre mikrovaskulárny vývoj.
Vieš to
Hoci zinok môže byť najbežnejším prechodným kovom v enzýmoch, mangán je možno najmenej bežný, čiastočne preto, že komplexy mangánu s proteínmi majú tendenciu byť slabo stabilné a ľahko sa disociujú. Známe mangánové metaloenzýmy zahŕňajú pyruvátkarboxylázu a superoxiddismutázu mangánu v mitochondriách a arginázu v cykle močoviny. Mangán môže tiež fungovať ako kofaktor aktivujúci kov pre mnohé enzýmy, ktoré vyžadujú horčík.
denná požiadavka u dospelých je vápnik 800 mg a u detí a dospievajúcich - 1 000 mg alebo viac.
Pri nedostatočnom príjme vápnika alebo pri porušení jeho vstrebávania v tele (s nedostatkom vitamínu D) vzniká stav nedostatku vápnika. Dochádza k jeho zvýšenému vylučovaniu z kostí a zubov. U dospelých vzniká osteoporóza – demineralizácia kostného tkaniva, u detí je narušená tvorba skeletu, vzniká rachitída.
Vlastnosti výživy s nedostatkom horčíka
Hoci mangán nie je považovaný za redoxný kov na základe jeho reaktivity, napriek tomu môže existovať v 6 oxidačných stavoch, z ktorých tri nie sú pozorované v biologických systémoch. Kobalt je pripevnený v štvorcovom, plochom usporiadaní ku krúžku podobnému tomu u gayov, ale s veľmi špeciálnymi vlastnosťami. Na rozdiel od hemu má kobalt 2 axiálne ligandy, ktoré neobsahujú proteín, čo umožňuje proteínovým skupinám prístup k centrálnemu kovu nad a pod rovinou.
Najlepšími zdrojmi vápnika sú mlieko a mliečne výrobky, rôzne syry a tvaroh (100-1000 mg / 100 g výrobku), zelená cibuľa, petržlen, fazuľa. Výrazne menej vápnika sa nachádza vo vajciach, mäse, rybách, zelenine, ovocí, bobuľových plodoch (20-40 mg / 100 g produktu).
horčík. Tento prvok je potrebný pre činnosť mnohých kľúčových enzýmov. pre metabolizmus organizmu. Horčík sa podieľa na udržiavaní normálnej funkcie nervového systému a srdcových svalov; má vazodilatačný účinok; stimuluje sekréciu žlče; zvyšuje motorická aktivitačriev, čo pomáha odstraňovať toxíny z tela (vrátane cholesterolu).
Prečo je nedostatok horčíka nebezpečný pre tehotné ženy?
V jednom oktaedrickom komplexe je jedna axiálna poloha zvyčajne obsadená jedným benzimidazolom a druhou metylovou skupinou. Zariadenie je jedinečné a umožňuje kobaltu vytvárať väzby uhlík-kov s potenciálom pre dve rôzne reakcie. Napríklad metylová skupina môže byť odstránená ako karbóniový ión držaním oboch elektrónov v kobalte, ktorý sa potom premení na menej stabilný.
V polohových permutáciách si kobalt zachováva iba jeden elektrón a vytvára stabilný koión 7 s uvoľnením voľného radikálu. Voľné radikály sú vysoko reaktívne a prekonávajú energetické bariéry, ktoré môžu držať iné reaktanty. teda Chemické vlastnosti kobaltové prenosové skupiny, ako sú karbóniové ióny alebo vysoko reaktívne uhlíkovo centrované radikály. Oba produkty sú možné a vysvetľujú potrebu kobaltu ako kofaktora, aby reakcia prebiehala mechanizmom voľných radikálov.
Absorpciu horčíka bráni prítomnosť fytínu a prebytočného tuku a vápnika v potrave. Denná potreba horčíka nie je presne definovaná; predpokladá sa však, že dávka 200-300 mg/deň predchádza prejavom nedostatku (predpokladá sa, že sa vstrebe asi 30 % horčíka).
Pri nedostatku horčíka sa narúša vstrebávanie potravy, spomaľuje sa rast, ukladá sa vápnik v stenách ciev a vzniká množstvo ďalších patologických javov. U ľudí je nedostatok horčíkových iónov vzhľadom na povahu výživy mimoriadne nepravdepodobný. Pri hnačke však môžu nastať veľké straty tohto prvku; ich následky sa prejavia, ak sa do tela dostanú tekutiny, ktoré neobsahujú horčík. Keď koncentrácia horčíka v sére klesne na približne 0,1 mmol / l, môže sa objaviť syndróm pripomínajúci delírium tremens: človek má polokomatózny stav, svalové chvenie, svalové kŕče v zápästí a chodidle, zvýšenú nervovosvalovú dráždivosť v reakcii na zvuk, mechanické a vizuálne podnety. Zavedenie horčíka spôsobuje rýchle zlepšenie stavu.
Horčík je bohatý najmä na rastlinnú potravu. Veľké množstvo obsahuje pšeničné otruby, rôzne obilniny (40 - 200 mg / 100 g výrobku), strukoviny, marhule, sušené marhule, sušené slivky. Málo horčíka je v mliečnych výrobkoch, mäse, rybách, cestovinách, väčšine zeleniny a ovocia (20 - 40 mg / 100 g).
Draslík. Asi 90 % draslíka je vo vnútri buniek. Spolu s inými soľami zabezpečuje osmotický tlak; podieľa sa na prenose nervových impulzov; regulácia metabolizmu voda-soľ; podporuje odstraňovanie vody a následne toxínov z tela; udržiava acidobázickú rovnováhu vnútorného prostredia tela; podieľa sa na regulácii činnosti srdca a iných orgánov; nevyhnutné pre fungovanie množstva enzýmov.
Draslík sa dobre vstrebáva z čriev a jeho prebytok sa z tela rýchlo odstraňuje močom. Denná potreba draslíka u dospelého človeka je 2000-4000 mg. Zvyšuje sa pri hojnom potení, pri užívaní diuretík, ochoreniach srdca a pečene. Draslík nie je deficitnou živinou v strave a pri pestrej strave k nedostatku draslíka nedochádza. Nedostatok draslíka v tele sa objaví, keď je narušená funkcia nervovosvalového a kardiovaskulárneho systému, ospalosť, znížená krvný tlak, srdcové arytmie. V takýchto prípadoch je predpísaná draslíková diéta.
Väčšina draslíka pochádza z rastlinných potravín. Jeho bohatým zdrojom sú marhule, sušené slivky, hrozienka, špenát, morské riasy, fazuľa, hrach, zemiaky, ostatná zelenina a ovocie (100 - 600 mg / 100 g výrobku). Menej draslíka obsahuje kyslá smotana, ryža, chlieb z prémiovej múky (100 - 200 mg / 100 g).
Sodík. Sodík sa nachádza vo všetkých tkanivách a telesných tekutinách. Podieľa sa na udržiavaní osmotického tlaku v tkanivových tekutinách a krvi; pri prenose nervových impulzov; regulácia acidobázickej rovnováhy, metabolizmus voda-soľ; zvyšuje aktivitu tráviacich enzýmov.
Metabolizmus sodíka bol značne študovaný kvôli jeho fyziologickým vlastnostiam a významu pre telo. Táto živina sa ľahko vstrebáva z čriev. Sodné ióny spôsobujú opuch tkanivových koloidov, čo spôsobuje zadržiavanie vody v tele a pôsobí proti jej uvoľňovaniu. Celkové množstvo sodíka v extracelulárnej tekutine teda určuje objem týchto tekutín. Zvýšenie koncentrácie sodíka v plazme vedie k pocitu smädu. V horúcom podnebí a pri ťažkej fyzickej práci dochádza k výraznému úbytku sodíka potením a na doplnenie strateného množstva je potrebné do tela dodávať soľ.
V zásade sa ióny sodíka dostávajú do tela na úkor kuchynskej soli - NaCl. Pri nadmernej konzumácii chloridu sodného sa zhoršuje odstraňovanie vo vode rozpustných konečných produktov metabolizmu obličkami, kožou a inými vylučovacími orgánmi. Zadržiavanie vody v tele komplikuje činnosť kardiovaskulárneho systému, zvyšuje krvný tlak. Preto je konzumácia soli pri príslušných ochoreniach v strave obmedzená. Pri práci v horúcich obchodoch alebo horúcom podnebí sa však množstvo sodíka (vo forme kuchynskej soli) privádzaného zvonku zvyšuje, aby sa jeho strata vyrovnala potom a znížilo sa potenie, ktoré zaťažuje činnosť srdca.
Sodík je prirodzene prítomný vo všetkých potravinách. Spôsob získavania potravinárskych výrobkov do značnej miery určuje konečný obsah sodíka v nich. Napríklad mrazený zelený hrášok obsahuje oveľa viac sodíka ako čerstvý. Čerstvá zelenina a ovocie obsahujú menej ako 10 mg/kg až 1 g/kg, na rozdiel od obilnín a syrov, ktoré môžu obsahovať sodík v množstve 10-20 g/kg.
Odhadnúť priemerný denný príjem sodíka z potravy je ťažké, pretože koncentrácia sodíka v potravinách sa značne líši a navyše ľudia sú zvyknutí do jedla prisoľovať. Dospelý človek denne skonzumuje až 15 g kuchynskej soli a rovnaké množstvo z tela vylúči. Toto množstvo je oveľa vyššie, ako je fyziologicky potrebné a je určená predovšetkým chuťou chloridu sodného, zvykom na slané jedlá. Obsah kuchynskej soli v ľudskej potrave možno bez poškodenia zdravia znížiť na 5 g denne. Uvoľňovanie chloridu sodného z tela, a teda aj jeho potreba, je ovplyvnené množstvom draselných solí prijatých telom. Rastlinné potraviny, najmä zemiaky, sú bohaté na draslík a zvyšujú vylučovanie chloridu sodného močom, a tým aj jeho potrebu.
Fosfor. Fosfor sa nachádza vo všetkých tkanivách tela, najmä vo svaloch a mozgu. Tento prvok sa podieľa na všetkých životných procesoch tela. : syntéza a rozklad látok v bunkách; regulácia metabolizmu; je súčasťou nukleových kyselín a radu enzýmov; potrebné na tvorbu ATP.
Fosfor sa nachádza v telesných tkanivách a potravinách vo forme kyseliny fosforečnej a jej organických zlúčenín (fosfátov). Jeho hlavná hmota je v kostnom tkanive vo forme fosforečnanu vápenatého, zvyšok fosforu je súčasťou mäkkých tkanív a tekutín. Vo svaloch dochádza k najintenzívnejšej výmene zlúčenín fosforu. Kyselina fosforečná sa podieľa na konštrukcii molekúl mnohých enzýmov, nukleových kyselín atď.
Pri dlhodobom nedostatku fosforu v potrave telo využíva vlastný fosfor z kostného tkaniva. To vedie k demineralizácii kostí a narušeniu ich štruktúry - riedeniu. Pri úbytku fosforu v tele klesá duševná a fyzická výkonnosť, strata chuti do jedla, apatia je zaznamenaná.
Denná potreba fosforu pre dospelých je 1200 mg. Zvyšuje sa pri veľkom fyzickom alebo psychickom vypätí, pri niektorých chorobách.
Veľké množstvo fosforu sa nachádza v živočíšnych produktoch, najmä v pečeni, kaviári, ako aj v obilninách a strukovinách. Jeho obsah v týchto výrobkoch sa pohybuje od 100 do 500 mg na 100 g výrobku. Bohatým zdrojom fosforu sú obilniny (ovsené vločky, perličkový jačmeň), obsahujú 300-350 mg fosforu / 100 g.Z rastlinných produktov sa však zlúčeniny fosforu vstrebávajú horšie ako pri konzumácii potravín živočíšneho pôvodu.
Síra. Dôležitosť tohto prvku vo výžive je daná predovšetkým skutočnosťou, že je súčasťou bielkovín vo forme aminokyselín obsahujúcich síru. (metionín a cystín), a je tiež neoddeliteľnou súčasťou niektorých hormónov a vitamínov.
Ako zložka aminokyselín obsahujúcich síru sa síra podieľa na procesoch metabolizmu bielkovín a jej potreba sa dramaticky zvyšuje počas tehotenstva a rastu tela, sprevádzaná aktívnym začlenením bielkovín do výsledných tkanív, ako aj počas zápalových procesov. procesy. Aminokyseliny obsahujúce síru, najmä v kombinácii s vitamínmi C a E, majú výrazný antioxidačný účinok. Síra spolu so zinkom a kremíkom určuje funkčný stav vlasov a pokožky.
Chlór. Tento prvok sa podieľa na tvorbe žalúdočnej šťavy, tvorbe plazmy, aktivuje množstvo enzýmov. Táto živina sa ľahko vstrebáva z čriev do krvi. Zaujímavá je schopnosť chlóru ukladať sa v koži, zdržiavať sa v tele pri nadmernom príjme a vylučovať sa potením vo výraznom množstve. K vylučovaniu chlóru z tela dochádza najmä močom (90 %) a potom.
Porušenie výmeny chlóru vedie k rozvoju edému, nedostatočnej sekrécii žalúdočnej šťavy atď. Prudký pokles obsahu chlóru v tele môže viesť k vážnemu stavu, dokonca k smrti. K zvýšeniu jeho koncentrácie v krvi dochádza pri dehydratácii tela, ako aj pri porušení vylučovacej funkcie obličiek.
Denná potreba chlóru je približne 5000 mg. Chlór sa do ľudského tela dostáva najmä vo forme chloridu sodného pri pridávaní do potravy.
^
3. Stopové prvky, ich charakteristika
železo. Tento prvok je nevyhnutný pre biosyntézu zlúčenín, ktoré poskytujú dýchanie, hematopoézu; podieľa sa na imunobiologických a redoxných reakciách; je súčasťou cytoplazmy, bunkových jadier a množstva enzýmov.
Asimilácii železa bráni kyselina šťaveľová a fytín. Na asimiláciu tejto živiny je potrebný vitamín B12. Kyselina askorbová tiež prispieva k absorpcii železa, pretože železo sa absorbuje vo forme dvojmocného iónu.
^ Nedostatok železa v tele môže viesť k rozvoju anémie, výmene plynov, bunkovému dýchaniu, teda narušeniu základných procesov zabezpečujúcich život. K vzniku stavov nedostatku železa napomáha: nedostatočný príjem železa v organizme v asimilovanej forme, zníženie sekrečnej aktivity žalúdka, nedostatok vitamínov (najmä B 12 , kyselina listová a askorbová) a množstvo chorôb, ktoré spôsobujú stratu krvi.
Potreba železa dospelého človeka (14 mg/deň) je pokrytá v nadbytku bežnou stravou. Keď sa však v potravinách používa chlieb z jemnej múky obsahujúcej málo železa, u obyvateľov miest sa veľmi často pozoruje nedostatok železa. Zároveň je potrebné vziať do úvahy, že obilné produkty bohaté na fosfáty a fytín tvoria so železom ťažko rozpustné zlúčeniny a znižujú jeho asimiláciu telom.
Železo je rozšírený prvok. Nachádza sa vo vnútornostiach, mäse, vajciach, fazuli, zelenine, bobuliach. V ľahko stráviteľnej forme sa však železo nachádza len v mäsových výrobkoch, pečeni (do 2000 mg / 100 g výrobku), vaječnom žĺtku.
Meď. Meď je základným prvkom ľudského metabolizmu, zohráva úlohu pri tvorbe červených krviniek, uvoľňovaní tkanivového železa a vývoji kostry, centrálneho nervového systému a spojivového tkaniva.
Keďže meď je široko distribuovaná v potravinách, je nepravdepodobné, že by sa u ľudí, možno s výnimkou dojčiat, na čisto mliečnej strave, niekedy vyvinula forma podvýživy súvisiacej s meďou.
Konzumácia nadmerne veľkých dávok medi u človeka vedie k podráždeniu a erózii slizníc, rozsiahlemu poškodeniu kapilár, poškodeniu pečene a obličiek a podráždeniu centrálneho nervového systému. Denná potreba tohto prvku je asi 2 mg. Zdrojom medi sú potraviny ako pečeň, vaječný žĺtok, zelená zelenina.
jód. Jód je základným prvkom, ktorý sa podieľa na tvorbe hormónu tyroxínu. Pri nedostatku jódu vzniká struma – ochorenie štítnej žľazy.
Potreba jódu sa pohybuje od 100-150 mcg denne. Obsah jódu v potravinách je zvyčajne nízky (4-15 µg %). Morské plody sú najbohatšie na jód. Takže v morských rybách obsahuje asi 50 mcg / 100 g, v tresčej pečeni až 800, v morských riasach, v závislosti od typu a načasovania odberu - od 50 mcg do 70 000 mcg / 100 g produktu. Treba ale počítať s tým, že pri dlhodobom skladovaní a tepelnej úprave potravín sa značná časť jódu (od 20 do 60 %) stráca.
Obsah jódu v suchozemských rastlinných a živočíšnych produktoch je veľmi závislý od jeho množstva v pôde. V oblastiach, kde je v pôde málo jódu, môže byť jeho obsah v potravinách 10 až 100-krát nižší ako je priemer. Preto v týchto oblastiach na prevenciu strumy sa do kuchynskej soli pridáva malé množstvo jodičnanu draselného (25 mg na 1 kg soli). Skladovateľnosť takejto jodizovanej soli nie je dlhšia ako 6 mesiacov, pretože jód počas skladovania soli postupne mizne.
Fluór. Pri nedostatku tohto prvku vzniká zubný kaz (deštrukcia zubnej skloviny). Nadbytok fluóru má tiež negatívny vplyv na telo, pretože fluórové soli, ktoré sa hromadia v kostiach, spôsobujú zmenu farby a tvaru zubov, osteochondrózu, a po tomto zhrubnutí kĺbov a ich nehybnosti, kostných výrastkov. Rozdiel medzi užitočnými a škodlivými dávkami fluóru je taký malý, že mnohí výskumníci sú proti fluoridácii vody.
Fluór konzumovaný s vodou je takmer úplne absorbovaný, fluór obsiahnutý v potravinách je absorbovaný v menšej miere. Absorbovaný fluór je rovnomerne distribuovaný po celom tele. Zadržiava sa hlavne v kostre a malé množstvo sa ukladá v zubnom tkanive. Vo vysokých dávkach môže fluór spôsobiť narušenie metabolizmu uhľohydrátov, lipidov, bielkovín, ako aj metabolizmu vitamínov, enzýmov a minerálnych solí.
V rôznych krajinách sa robili odhady denného príjmu fluoridu z potravy; pre dospelých sa táto hodnota pohybuje od 0,2 do 3,1 mg pre deti veková skupina od 1 do 3 rokov sa príjem fluoridu odhadoval na 0,5 mg/deň.
Takmer všetky potravinárske výrobky obsahujú aspoň stopové množstvá tohto prvku. Všetky druhy vegetácie obsahujú určité množstvo fluóru, ktorý získavajú z pôdy a vody. Vysoké hladiny fluoridu sa našli v niektorých potravinách, najmä v rybách, niektorých druhoch zeleniny a čaji. Používanie fluoridovanej vody v závodoch na spracovanie potravín môže často zdvojnásobiť hladinu fluoridov v hotových výrobkoch.
Na prevenciu a liečbu zubného kazu, rôzne zubné pasty, prášky, elixíry, žuvačky a podobne, ktoré obsahujú pridaný fluór, hlavne v anorganickej forme. Tieto zlúčeniny sa bežne začleňujú do prostriedkov na čistenie zubov, typicky v koncentráciách približne 1 g/kg.
Chromium. Zdá sa, že tento prvok je nevyhnutný pre metabolizmus glukózy a lipidov a pre využitie aminokyselín niektorými systémami. Tiež má dôležitosti na prevenciu miernych foriem cukrovky a aterosklerózy u ľudí.
Chróm sa vstrebáva ako z gastrointestinálneho traktu, tak aj z dýchacieho traktu. Absorbované množstvo nie je pre každý z týchto systémov rovnaké a závisí od formy chrómu. Trojmocný chróm je pre človeka nevyhnutnou formou prvku, šesťmocný chróm je toxický. Chróm je distribuovaný v tkanivách ľudského tela v nerovnakých, ale zvyčajne nízkych koncentráciách. Hladiny chrómu vo všetkých tkanivách okrem pľúc s vekom klesajú. Najväčšie množstvo chrómu sa u ľudí hromadí v koži, svaloch a tukovom tkanive. Homeostatické mechanizmy, vrátane mechanizmov transportu v pečeni a črevách, zabraňujú nadmernej akumulácii trojmocného chrómu. Chróm sa pomaly vylučuje z tela, hlavne močom.
Dnes sa za normu považuje spotreba asi 150 mg chrómu denne. Je obzvlášť užitočný pre starších ľudí, ktorých telo neabsorbuje sacharidy dobre, a chróm podporuje metabolické procesy týchto konkrétnych zlúčenín. Anorganický chróm sa absorbuje zle, oveľa ľahšie - v organických zlúčeninách, teda vo forme, v akej sa nachádza v živých organizmoch.
Potravinárske výrobky sa značne líšia v hladinách chrómu, ktoré sa pohybujú od 20 do 550 µg/kg. Bohatým zdrojom chrómu sú pivovarské kvasnice, pečeň (10-80 mcg/100 g). V menšom množstve sa tento prvok nachádza v zemiakoch so šupkou, hovädzom mäse, čerstvej zelenine, celozrnnom pečive, syroch.
mangán. Mangán je nevyhnutný ako kofaktor v mnohých enzýmových systémoch; podieľa sa na správnom fungovaní flavoproteínov, pri syntéze sulfátovaných mukopolysacharidov, cholesterolu, hemoglobínu a v mnohých ďalších metabolických procesoch. Z požitého mangánu sa absorbujú len asi 3 %.
Vstrebávanie mangánu úzko súvisí so vstrebávaním železa. Potreba mangánu je 0,2-0,3 mg na 1 kg hmotnosti človeka denne. Najviac mangánu obsahujú brusnice a čaj, o niečo menej gaštany, kakao, zelenina, ovocie (100-200 mcg / 100 g).
^ Nikel. Nikel bol uznaný ako esenciálny stopový prvok relatívne nedávno. V súčasnosti je preukázaná jeho úloha ako koenzýmu v procesoch metabolizmu železa. Zároveň je zvýšený príjem železa v tele sprevádzaný zvýšením potreby potravinového niklu. Okrem toho nikel prispieva k absorpcii medi - ďalšieho prvku nevyhnutného pre hematopoézu. Význam potravinárskeho niklu alebo niklu izolovaného z prírodných produktov zvýrazňuje skutočnosť, že syntetické zlúčeniny tohto prvku sú karcinogénne.
Nikel je prítomný vo väčšine potravín, ale v koncentráciách nižších (a často oveľa nižších) ako 1 mg/kg. Uvádza sa, že príjem niklu v strave sa pohybuje od menej ako 200 do 900 µg/deň. Pri normálnej strave prichádza asi 400 mcg / deň. Ukázalo sa, že obsah niklu vo vínach a pive je 100 a 50 µg/l.
Zinok. Tento stopový prvok sa ako koenzým podieľa na širokom spektre reakcií biosyntézy bielkovín (viac ako 70) a metabolizmu nukleových kyselín (vrátane procesov replikácie a transkripcie DNA), ktoré zabezpečujú predovšetkým rast a dospievanie organizmu. Zároveň je zinok spolu s mangánom špecifickým stopovým prvkom, ktorý ovplyvňuje stav sexuálnej funkcie, a to aktivitu niektorých pohlavných hormónov, spermatogenézu, vývoj mužských pohlavných žliaz a sekundárne pohlavné znaky. Okrem toho sa v poslednej dobe uvažuje o úlohe zinku v prevencii hypertrofických procesov v prostatickej žľaze.
Zinok sa spolu so sírou podieľa na raste a obnove pokožky a vlasov. Spolu s mangánom a meďou sa zinok výrazne podieľa na vnímaní chuťových a čuchových vnemov. Zinok ako nenahraditeľná zložka je súčasťou molekuly inzulínu a u pacientov s diabetes mellitus je jeho hladina znížená. Je veľmi dôležité, že tento stopový prvok je koenzým alkoholdehydrogenázy, ktorý zabezpečuje metabolizmus etylalkoholu. Zároveň sa prudko znižuje úroveň absorpcie zinku pri chronickom alkoholizme. Takzvaná "nočná slepota" (t.j. zhoršené nočné videnie) sa môže vyvinúť nielen pri nedostatku vitamínu A, ale aj zinku. Zinok spolu s vitamínom B 6 zabezpečuje metabolizmus nenasýtených mastných kyselín a syntézu prostaglandínov.
Zinok je veľmi dôležitý pre trávenie a vstrebávanie živín. Zinok teda zabezpečuje syntézu najdôležitejších tráviacich enzýmov v pankrease a podieľa sa aj na tvorbe chylomikrónov – transportných častíc, v ktorých sa tuky z potravy môžu vstrebávať do krvi. Zinok je spolu s vitamínmi skupiny B dôležitým regulátorom funkcií nervového systému. V podmienkach nedostatku zinku môžu nastať emocionálne poruchy, emočná nestabilita, podráždenosť a vo veľmi ťažkých prípadoch môže dôjsť k dysfunkcii mozočka. Napokon sa hromadí stále viac údajov v prospech účasti zinku v procesoch dozrievania lymfocytov a reakciách bunkovej imunity.
Denná potreba zinku je 8000-22000 mcg%. S bežnou stravou je celkom spokojná. Priemerný denný príjem zinku len s pitnou vodou je asi 400 mcg. Obsah zinku v potravinárskych výrobkoch sa zvyčajne pohybuje od 150-25000 mcg%. V pečeni, mäse a strukovinách však dosahuje 3000 - 5000 mcg%. Niekedy môže nedostatok zinku pociťovať aj telo detí a dospievajúcich, ktorí nekonzumujú dostatok živočíšnych produktov.
^ Selén. Dokonca aj v polovici XX storočia. selén nielenže nutričná veda nepovažovala, ale bol dokonca považovaný za veľmi toxický prvok s karcinogénnymi vlastnosťami. Avšak už v 60. rokoch. zistilo sa, že pri nedostatku selénu trpí kardiovaskulárny systém, ktorý sa prejavuje progresívnou aterosklerózou a slabosťou srdcového svalu a pri stavoch chronického nedostatku selénu môže vzniknúť takmer neliečiteľná kardiomyopatia. V poslednej dobe na úrovni súčasný výskum nachádza potvrdenie jedného z dôležitých pozorovaní starovekej čínskej medicíny, čo naznačuje dostatočné zásobenie tela selénom pomáha spomaľovať proces starnutia a vedie k dlhovekosti . Zaujímavosťou je, že známe liečivé odrody zeleného čaju, dodávané s cieľom dosiahnuť zdravie a dlhovekosť v cisárskych palácoch v r. Staroveká Čína, boli pestované v tých horských provinciách, v ktorých pôdach je už pomocou moderných analytických metód stanovený vysoký obsah selénu.
Po objavení selénu sa zistilo, že vitamín E a selén pôsobia na rôzne časti toho istého procesu a navzájom sa striktne dopĺňajú, to znamená, že ich antioxidačná aktivita sa pri spoločnom použití dramaticky zvyšuje. Synergia oboch antioxidantov je obzvlášť zaujímavá v kontexte protirakovinovej aktivity. Ukázalo sa teda, že podávanie selénových prípravkov súčasne s vitamínom E výrazne zvýšilo antikarcinogénny účinok vo vzťahu k experimentálnym nádorom.
Príjem selénu potravou závisí od podmienok a charakteru príjmu potravy a od hladiny selénu v potravinách. Zelenina a ovocie sú vo všeobecnosti chudobným zdrojom selénu, na rozdiel od obilnín, obilných produktov, mäsa (najmä vedľajších produktov), morských plodov, ktoré obsahujú značné množstvo selénu, typicky vysoko nad 0,2 mg/kg vlhkej hmotnosti . Chemické zloženie Pôda a obsah selénu v nej výrazne ovplyvňuje množstvo selénu v zrne, pohybuje sa od 0,04 mg/kg do 21 mg/kg.
molybdén. Celkové množstvo molybdénu v tele dospelého človeka je asi 7 mg. Obsah molybdénu v krvi je asi 0,5 mikrogramu na 100 ml. Vyššie koncentrácie tohto prvku boli zistené u ľudí žijúcich v regiónoch, kde je pôda najbohatšia na zlúčeniny tohto kovu. V niektorých regiónoch Arménska boli teda zaznamenané časté prípady dny medzi obyvateľmi, ktorí jedia najmä miestne produkty, v ktorých sa zistilo extrémne vysoké množstvo molybdénu. Jeho obsah v strave obyvateľov tohto regiónu bol 10-15 mg. V iných oblastiach, kde boli prípady dny menej časté, dostávali ľudia z potravy len 1-2 mg molybdénu denne.
Molybdén je neoddeliteľnou súčasťou mnohých enzýmov, ako je xantínoxidáza, aldehydoxidáza, sulfátoxidáza. Je známe, že molybdén bráni vzniku zubného kazu.
Odhadovaná denná potreba molybdénu je 2 mcg na 1 kg telesnej hmotnosti. V Rusku je denný príjem molybdénu 0,27 mg.
najbohatší na molybdén rôzne druhy zelenina (napríklad strukoviny) a vnútorné orgány zvierat.
kobalt. Biologický účinok kobaltu je známy od roku 1948, keď vedci Rickes a Smith zistili, že atóm kobaltu je ústredným prvkom molekuly vitamínu B 12. Maximálna koncentrácia kobaltu v tkanivách je asi 100 μg / kg. Celkový obsah kobaltu v tele dospelého človeka je 5 mg. Človek s jedlom denne prijme 5,63 – 7,94 mikrogramov kobaltu, z čoho sa 73 – 97 % vstrebe.
Priemerná denná potreba kobaltu je 60 mcg na 1 kg telesnej hmotnosti. Predpokladá sa, že človek potrebuje kobalt iba vo forme kyanokobalamínu (vitamín B 12). V niektorých krajinách sa zlúčeniny kobaltu používali ako potravinová prísada do piva na stabilizáciu peny. Ukázalo sa však, že práve takáto prísada bola príčinou srdcových ochorení konzumentov piva. Preto sa teraz upustilo od používania zlúčenín kobaltu ako prídavnej látky v potravinách.
^
4 Vplyv spracovania na minerálne zloženie potravín
Pri spracovaní potravinárskych surovín spravidla dochádza k znižovaniu obsahu minerálnych látok (okrem Na, pridávaného vo forme potravinárskej soli). V rastlinnej potrave sa strácajú s odpadom. Pri výrobe obilnín a múky po spracovaní zrna sa teda znižuje obsah množstva makro- a najmä mikroprvkov, keďže týchto zložiek je v odstránených šupkách a klíčkoch viac ako v celom zrne. Porovnávacia analýza Minerálne zloženie v pšeničnej múke najvyššej kvality a celozrnnej múke je uvedené nižšie (obsah prvkov je uvedený v mg / 100 g výrobku):
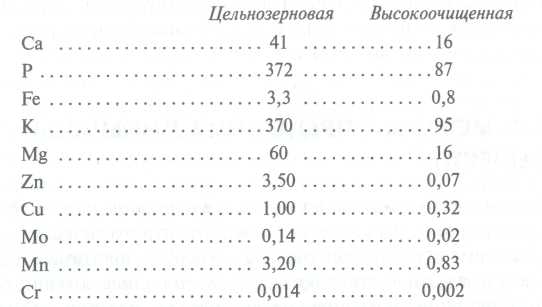
Napríklad zrno pšenice a raže obsahuje v priemere asi 1,7 % popola, zatiaľ čo v múke v závislosti od odrody od 0,5 (v najvyššej triede) do 1,5 % (v celozrnnej). Pri čistení zeleniny a zemiakov sa stráca 10 až 30 % minerálov. Ak sa podrobia tepelnému vareniu, potom sa v závislosti od technológie (varenie, vyprážanie, dusenie) stratí ďalších 5 až 30 %.
Mäso, rybie produkty a hydina väčšinou strácajú makroživiny, ako je vápnik a fosfor, keď sa dužina oddelí od kostí.
Pri tepelnej úprave (varenie, vyprážanie, dusenie) mäso stráca 5 až 50 % minerálov. Ak sa však spracovanie uskutočňuje za prítomnosti kostí obsahujúcich veľa vápnika, je možné zvýšiť obsah vápnika vo varených mäsových výrobkoch o 20%.
V technologickom procese môže v dôsledku nedostatočne kvalitného zariadenia prejsť do konečného produktu určité množstvo mikroelementov. Takže pri pečení chleba počas prípravy cesta v dôsledku kontaktu cesta so zariadením obsah železa možno zvýšiť o 30 %. Tento proces je nežiaduci, pretože spolu so železom môžu do produktu prechádzať aj toxické prvky obsiahnuté vo forme nečistôt v kove. Pri skladovaní konzervovaných potravín v prefabrikovaných plechovkách (teda spájkovaných) plechovkách s nekvalitnou spájkou alebo pri porušení ochrannej vrstvy laku môžu do výrobku preniknúť vysoko toxické prvky ako olovo, kadmium a cín.
Je potrebné vziať do úvahy, že množstvo kovov, ako je železo a meď, aj v malých koncentráciách, môže spôsobiť nežiaducu oxidáciu produktov. Ich katalytické oxidačné schopnosti sú obzvlášť výrazné vo vzťahu k tukom a tukovým produktom. Takže napríklad pri koncentrácii železa nad 1,5 mg/kg a medi 0,4 mg/kg pri dlhodobom skladovaní masla a margarínov tieto kovy spôsobujú žltnutie výrobkov. Pri skladovaní nápojov v prítomnosti železa nad 5 mg/l a medi 1 mg/l možno za určitých podmienok často pozorovať zakalenie nápojov.
^
5. Metódy stanovenia minerálnych látok
Na rozbor minerálnych látok sa využívajú najmä fyzikálno-chemické metódy - optické a elektrochemické.
Takmer všetky tieto metódy vyžadujú špeciálnu prípravu vzoriek na analýzu, ktorá spočíva v predbežnej mineralizácii predmetu štúdia. Mineralizácia môže byť vykonaná dvoma spôsobmi: "suchým" a "mokrým". „Suchá“ mineralizácia zahŕňa zuhoľnatenie, spálenie a kalcináciu testovanej vzorky za určitých podmienok. „Mokrá“ mineralizácia zabezpečuje aj spracovanie predmetu štúdia koncentrované kyseliny(najčastejšie HNO 3 a H 2 SO 4).
^ Spektrálne metódy analýzy.
Fotoelektrokolorimetria - analýza založená na meraní absorpcie farebných roztokov monochromatického žiarenia vo viditeľnej oblasti spektra. Merania sa vykonávajú pomocou fotoelektrických kolorimetrov vybavených úzkopásmovými filtrami. Ak testovaná látka nie je zafarbená, musí sa premeniť na farebnú zlúčeninu chemickou reakciou s určitými činidlami (fotometrická analytická reakcia).
Spektrofotometria je analytická metóda založená na meraní absorpcie monochromatického žiarenia v ultrafialovej, viditeľnej a infračervenej oblasti spektra. Takéto merania sa vykonávajú pomocou spektrofotometrov, kde sa ako monochromatizéry používajú disperzné hranoly a difrakčné mriežky.
Kvantitatívna analýza študovaného iónu sa zvyčajne vykonáva pomocou metódy kalibračnej krivky.
Emisná spektrálna analýza. Metódy emisnej spektrálnej analýzy sú založené na meraní vlnovej dĺžky, intenzity a iných charakteristík svetla emitovaného atómami a iónmi látky v plynnom stave. Emisná spektrálna analýza umožňuje určiť elementárne zloženie anorganických a organických látok.
Intenzita spektrálnej čiary je určená počtom excitovaných atómov v zdroji excitácie, ktorý závisí nielen od koncentrácie prvku vo vzorke, ale aj od podmienok excitácie. Pri stabilnej prevádzke budiaceho zdroja je vzťah medzi intenzitou spektrálnej čiary a koncentráciou prvku (ak je dostatočne malá) lineárny, t.j. tento prípad kvantitatívnu analýzu možno vykonať aj pomocou metódy kalibračnej krivky.
Najväčšie uplatnenie ako zdroj budenia dostal elektrický oblúk, iskra, plameň. Teplota oblúka dosahuje 5000 - 6000°C. V oblúku je možné získať spektrum takmer všetkých prvkov. Pri iskrovom výboji sa vyvinie teplota 7000 - 10000 °C a všetky prvky sú vzrušené. Plameň poskytuje dostatočne jasné a stabilné emisné spektrum. Metóda analýzy využívajúca plameň ako zdroj budenia sa nazýva analýza emisií plameňa. Táto metóda stanovuje viac ako štyridsať prvkov (alkalické a alkalické zeminy, Cu 2, Mn 2 atď.).
^ Atómová absorpčná spektroskopia . Metóda je založená na schopnosti voľných atómov prvkov v plameňových plynoch absorbovať svetelnú energiu pri vlnových dĺžkach charakteristických pre každý prvok.
V atómovej absorpčnej spektroskopii je takmer úplne vylúčená možnosť prekrývania spektrálnych čiar rôznych prvkov, pretože ich počet v spektre je oveľa menší ako v emisnej spektroskopii.
Pokles intenzity rezonančného žiarenia v podmienkach atómovej absorpčnej spektroskopie sa riadi exponenciálnym zákonom poklesu intenzity v závislosti od hrúbky vrstvy a koncentrácie látky, podobne ako Bouguer-Lambert-Beerov zákon.
Stálosť hrúbky vrstvy pohlcujúcej svetlo (plameň) sa dosahuje pomocou horákov špeciálnej konštrukcie. Metódy atómovej absorpčnej spektrálnej analýzy sa široko používajú na analýzu takmer akéhokoľvek technického alebo prírodného objektu, najmä v prípadoch, keď je potrebné určiť malé množstvá prvkov.
Metódy na stanovenie atómovej absorpcie boli vyvinuté pre viac ako 70 prvkov.
^ 2. Elektrochemické metódy analýzy.
Ionometria. Metóda sa používa na stanovenie K iónov , Na , Ca 2 , Mn 2 , F - , ja - , Сl - atď.
Metóda je založená na použití iónovo selektívnych elektród, ktorých membrána je priepustná pre určitý typ iónov (preto je spravidla vysoká selektivita metódy).
Kvantitatívny obsah stanovovaného iónu sa vykonáva buď pomocou kalibračného grafu, ktorý je vynesený v súradniciach E - pC, alebo metódou sčítania. Metóda štandardného pridávania sa odporúča na stanovenie iónov v komplexných systémoch obsahujúcich vysoké koncentrácie cudzorodých látok.
Polarografia. Metóda striedavej polarografie sa používa na stanovenie toxických prvkov (ortuť, kadmium, olovo, meď, železo).
Metóda je založená na štúdiu kriviek prúd-napätie získaných pri elektrolýze elektrooxidačnej alebo elektroredukčnej látky. Ako indikačná elektróda v polarografii sa najčastejšie používa ortuťová kvapková elektróda, niekedy pevné mikroelektródy - platina, grafit. Ako referenčná elektróda sa používa buď ortuť naliata na dno elektrolyzéra alebo nasýtený kalomelový poločlánok.
So zvyšujúcim sa napätím prichádza moment, kedy sa všetky ióny vstupujúce do elektródy v dôsledku difúzie okamžite vybijú a ich koncentrácia vo vrstve blízkej elektróde sa stáva konštantnou a prakticky nulovou. Prúd pretekajúci obvodom v tomto čase sa nazýva obmedzujúci difúzny prúd.
Kvantitatívna polarografická analýza je založená na použití priamej proporcionálna závislosť veľkosť difúzneho prúdu na koncentrácii určovaného prvku.
^ MINERÁLNE PRVKY
Minerálne (popolové) prvky sa v potravinách nachádzajú vo forme organických a anorganických zlúčenín. Nachádzajú sa v mnohých organických
látky rôznych tried - bielkoviny, tuky, glykozidy, enzýmy atď. Minerálne prvky sa zvyčajne stanovujú v popole po spálení potravinárskych výrobkov, pretože je pomerne ťažké presne určiť, ktoré látky a v akom množstve sú tieto prvky zahrnuté.
Úloha minerálnych prvkov v živote ľudí, zvierat a rastlín je obrovská: všetky fyziologické procesy v živých organizmoch prebiehajú za účasti týchto prvkov. Minerálne prvky sa teda v ľudskom a zvieracom organizme podieľajú na plastických procesoch, tvorbe a stavbe tkanív, na metabolizme vody, na udržiavaní osmotického tlaku krvi a iných telesných tekutín, na udržiavaní acidobázickej rovnováhy v organizme, na udržaní osmotického tlaku krvi a iných telesných tekutín. a sú zahrnuté v komplexe látok, ktoré tvoria živé bunky protoplazmy, v zložení niektorých žliaz s vnútornou sekréciou atď.
Minerálne zloženie organizmov sa mení s vekom; starnutím sa pozoruje mineralizácia organizmov. Takže novorodenci obsahujú okolo 34 g minerálov na 1 kg telesnej hmotnosti, u dospelého človeka obsah týchto látok stúpa na 43 g a viac.
V ľudskom a zvieracom tele sa našlo viac ako 70 minerálnych prvkov. Mnohé enzymatické procesy prebiehajúce v rôznych tkanivách tela vyžadujú účasť množstva minerálnych prvkov. Takže na premenu kyseliny pyrohroznovej na kyselinu octovú alebo glukózy na fruktózu alebo fosfoglycerol na glukózu-6-manóza-6- a fruktóza-6-fosfát je účasť horčíkových iónov povinná. Vápenaté ióny inhibujú vývoj tohto procesu.
Minerály sú v tkanivách ľudského tela nerovnomerne rozložené. V tvrdých tkanivách prevládajú dvojmocné prvky: vápnik (Ca) a horčík (Mg) a v mäkkých tkanivách monovalentné prvky: draslík (K) a sodík (Na). Okrem toho sa v tvrdých tkanivách hromadí veľa fosforu (P), hlavne vo forme fosfátových solí. Pri nedostatku minerálov v potrave sa tieto zlúčeniny vylučujú z tela a dochádza k narušeniu normálneho metabolizmu.
Minerálne látky rozpustené v krvnej plazme, medzibunkových a iných telesných tekutinách vytvárajú určitý osmotický tlak, ktorý závisí od molárnej koncentrácie látok rozpustených v tekutine. Soli zvyšujú osmotický tlak vo väčšej miere
stupňa ako neelektrolyty pri rovnakej molárnej koncentrácii, pretože soli disociujú za vzniku iónov. Osmotický tlak závisí od celkového počtu nedisociovaných molekúl a iónov. Osmotický tlak krvi, lymfy a medzibunkovej tekutiny ľudského a zvieracieho tela závisí najmä od chloridu sodného (NaCl), ktorý je v nich rozpustený.
Osmotický tlak v telesných tekutinách ovplyvňuje distribúciu vody a rozpustených látok v tkanivách. U vyšších zvierat je osmotický tlak konštantný a dosahuje 7,5 - 9,0 atm. Udržiavanie stáleho osmotického tlaku je zabezpečené činnosťou vylučovacích orgánov, hlavne obličiek a potných žliaz.
Vstupom minerálnych solí do krvi dochádza k vstupu medzibunkovej vody do krvi, a preto koncentrácia soli v krvi klesá. Prebytočnú vodu a soľ potom odstránia obličky. Pokles vody v tkanivách, reflexne pôsobiaci na nervové centrá, spôsobuje smäd.
Normálna životná aktivita ľudského tela môže prebiehať len s určitými vlastnosťami medzibunkových a intersticiálnych tekutín. V tejto stálosti prostredia zohráva dôležitú úlohu acidobázická rovnováha, pri ktorej je reakcia krvi, lymfy a iných telesných tekutín takmer neutrálna. Acidobázická rovnováha je udržiavaná o komplexný systém regulátory zjednotené do jednej centrály nervový systém. Takýmito regulátormi sú systémy vyrovnávania krvi, výmena kyslíka a oxidu uhličitého, oxidu uhličitého a chloridových solí, vylučovacie funkcie obličiek, pľúc, potných žliaz atď.
V procese komplexnej premeny potravín bohatých na vápnik, horčík, sodík alebo draslík v ľudskom tele môžu vznikať zásadité zlúčeniny. Medzi zdroje zásadotvorných prvkov patrí ovocie, zelenina, strukoviny, mlieko a mliečne výrobky.
Ostatné produkty, ako je mäso, ryby, vajcia, syr, chlieb, obilniny, cestoviny, v procese transformácie v ľudskom tele dávajú kyslé zlúčeniny.
Charakter výživy môže ovplyvniť posuny v acidobázickej rovnováhe v tkanivách ľudského tela. Acidobázická rovnováha sa často posúva na > stranu kyslosti. V dôsledku prudkého posunu
prípustné maximálne normy pre obsah popola a pri hodnotení takýchto produktov určujú jeho množstvo.
Zvyčajne sa rozlišujú dva pojmy - „celkový (surový) popol“ a „čistý popol“. Pojem „celkový popol" znamená súhrn minerálnych prvkov alebo ich oxidov, ktoré sú súčasťou chemickej štruktúry potravinárskych výrobkov, ako aj vložené do výrobku počas jeho výroby alebo „náhodne zachytené ako nečistoty. „Čistý popol" znamená súhrn minerálnych prvkov alebo ich oxidov bez nečistôt .
Obsah popola vo výrobku sa zisťuje spaľovaním. Na tento účel sa vzorka najskôr opatrne spáli a potom sa kalcinuje na konštantnú hmotnosť. Zvýšené množstvo popola oproti norme naznačuje kontamináciu produktu pieskom, kovovými časticami a zeminou.
Na stanovenie "čistého popola" sa výsledný popol spracuje s 10% kyselinou chlorovodíkovou. V tomto prípade sa „čistý popol“ rozpustí v kyseline chlorovodíkovej a zvyšok bude indikovať prítomnosť cudzích anorganických nečistôt v produkte. Takže v prípade zlého umývania paradajok pred spracovaním alebo v zemiakovom škrobe pri nedostatočnom umývaní hľúz dochádza k zvýšenému množstvu popola v dôsledku cudzích minerálnych nečistôt.
Vápnik v ľudskom tele sa nachádza v kostnom tkanive a zuboch - asi 99%. Zvyšok vápnika vstupuje do krvi vo forme iónov a v stave spojenom s proteínmi a inými zlúčeninami.
Denná potreba vápnika u dospelého človeka je 0,8-1,0 g Zvýšené množstvo vápnika potrebujú tehotné a dojčiace ženy, až 1,5-2 g denne, ako aj deti, v organizme ktorých sa vápnik intenzívne využíva na tvorbu kostí. Nedostatok vápnika spôsobuje v tele deformáciu kostry, krehkosť kostí a svalovú atrofiu. Vápnik sa vyznačuje tým, že aj pri jeho nedostatku v potrave sa naďalej vylučuje z tela vo významných množstvách.
Vápnik sa nachádza v potravinách vo forme fosfátových a oxalátových chloridových solí, ako aj v kombinácii s mastnými kyselinami, bielkovinami atď.
Všetky zlúčeniny vápnika, s výnimkou CaC! a, sú ťažko rozpustné vo vode, a preto sa zle vstrebávajú
ľudské telo. Nerozpustné zlúčeniny vápnika čiastočne prechádzajú z produktov do roztoku v žalúdku pôsobením kyseliny chlorovodíkovej tráviace šťavy. Absorpcia vápnika v potravinách ľudským telom závisí vo veľkej miere od prítomnosti fosfátov, tukov, zlúčenín horčíka atď.. Absorpcia vápnika je teda najvyššia, keď je pomer vápnika a fosforu I v potravinách ; 1,5 alebo 1: 2. Množstvo fosforu v potravinách zvýšené oproti uvedeným pomerom vedie k prudkému zníženiu absorpcie vápnika. Nadbytok horčíka má tiež nepriaznivý vplyv na vstrebávanie vápnika ľudským organizmom. Ostrý negatívny vplyv absorpciu vápnika zabezpečujú zlúčeniny vápnika s kyselinou inozitol-fosforečnou, ktorá sa vo významnom množstve nachádza v obilných zrnách a produktoch ich spracovania.
Veľmi dôležitú úlohu pri vstrebávaní vápnika zohráva vitamín D, ktorý podporuje prechod solí vápnika a fosforu z čriev do krvi a ukladanie v kostiach vo forme fosforečnanu vápenatého.
Obsah vápnika v niektorých potravinárskych výrobkoch je nasledovný (mg%): v chudom mäse - 7; vo vajciach - 54; v mlieku - 118; v syre - 930; v tvarohu - 140; v ovsených vločkách - 65; v pšeničnej múke - 15; v ryži - 9; v jablkách - 7; v pomarančoch - 45; vo vlašských orechoch -89; v repe - 29; v karfiole - 89; v bielej kapuste - 45; v mrkve - 56; v zemiakoch - 14. Z uvedených údajov je vidieť, že najvýznamnejším zdrojom vápnika pre človeka sú mliečne výrobky. Vápnik v mliečnych výrobkoch, ako aj v zelenine a ovocí, je ľahko stráviteľná zlúčenina.
Horčíka je v ľudskom tele 30-35-krát menej ako vápnika, no je veľmi dôležité. Väčšina horčíka sa nachádza v kostnom tkanive. Horčík hrá zvláštnu úlohu v rastlinách nesúcich chlorofyl, kde je súčasťou molekuly chlorofylu. Podobne ako vápnik aj horčík tvorí ťažko rozpustné zlúčeniny. Horčík je obzvlášť ťažké asimilovať v prítomnosti iónu LO$.
Obsah horčíka v niektorých potravinárskych výrobkoch je nasledovný (mg%): vo fazuli - 139; v ovsených vločkách - 133; v hrášku - 107; v prose - 87; v pšeničnom chlebe - 30; v zemiakoch - 28; v mrkve - 21; v bielej kapuste -! Anna - 12; v jablkách - 8; v citrónoch - 7; v hovädzom mäse - 15; vo vajciach - 11; v mlieku - 12. V dôsledku toho sa 2 * 35 horčíka nachádza v najväčšom množstve v obilninách a strukovinách.
Potreba horčíka pre dospelého človeka je 400 mg denne.
Sodík je široko obsiahnutý v potravinách, najmä v živočíšnych produktoch. Hlavným zdrojom sodíka pre ľudský organizmus je NaCt (obyčajná soľ). Sodík hrá dôležitú úlohu v procesoch intracelulárneho a medzitkanivového metabolizmu. Asi 90 % osmotického tlaku krvnej plazmy závisí od obsahu NaCl v nej. Typicky sa 3,3 g sodíka rozpustí v litri ľudskej krvnej plazmy. NaC! Tiež zohráva dôležitú úlohu pri regulácii vodného metabolizmu v tele. Sodné ióny spôsobujú opuch tkanivových koloidov a tým prispievajú k zadržiavaniu viazanej vody v tele. Z tela NaC! vylučuje hlavne močom a potom. Pri zvýšenej práci a konzumácii tekutín človek stratí až 3-5 litrov potu, čo je 99,5% vody. V sušine potu je hlavná časť NaGI.
Kuchynská soľ, ktorá sa dostáva do ľudského tela s potravou, doplňuje spotrebu NaCI v krvi a používa sa na tvorbu kyseliny chlorovodíkovej v žalúdočnej šťave, ako aj na syntézu NaHCO3 pankreasovou žľazou. Prítomnosť NaHCO3 vysvetľuje alkalickú reakciu pankreatickej šťavy, ktorá je nevyhnutná pre štiepenie potravinových bielkovín enzýmom trypsínom.
Denná potreba sodíka u dospelého človeka je 4-6 g, čo zodpovedá 10-15 g kuchynskej soli. Bežná strava obyvateľstva obsahuje dostatočné množstvo sodíka, keďže do jedla sa pridáva kuchynská soľ.
Draslík je neustále a vo významných množstvách prítomný v potravinách, najmä rastlinného pôvodu.V popole rastlín je obsah draslíka niekedy viac ako 50 % jeho hmotnosti.
V ľudskom tele sa draslík podieľa na enzymatických reakciách, tvorbe tlmivých systémov, ktoré zabraňujú posunom v reakcii prostredia. Draslík sa znižuje
vodu zadržiavajúcu schopnosť bielkovín, znižovanie ich hydro-schopnosti, a tým podporuje vylučovanie vody a sodíka z tela, preto možno draslík považovať za nejakého fyziologického antagonistu sodíka.
Denná potreba draslíka u dospelého človeka je 3-5 g.
Železo je v prírode široko rozšírené. Vo všeobecnosti takmer všetky prírodné potraviny obsahujú železo, ale v malom množstve.
V ľudskom a živočíšnom organizme je železo súčasťou najdôležitejších organických zlúčenín - hemoglobínu v krvi, myoglobínu, niektorých enzýmov - katalázy, peroxidázy, cytochrómoxidázy atď. Krvný hemoglobín obsahuje 2A, telesné železo. Významné množstvo železa sa nachádza v slezine a pečeni. Železo má schopnosť hromadiť sa v tele. Hemoglobín v krvi sa počas života ničí a železo uvoľnené v tomto prípade môže telo znovu využiť na tvorbu hemoglobínu.
Železo, ktoré je súčasťou ovocia a zeleniny, je ľudským telom dobre absorbované, pričom väčšina železa v obilných výrobkoch je pre telo v nestráviteľnej forme.
Denná potreba dospelej ľudskej žľazy je 15 mg.
l l o r je súčasťou prirodzenej potravy v malom množstve. Rastlinné produkty obsahujú málo chlóru, zatiaľ čo živočíšne produkty obsahujú o niečo viac. Takže obsah chlóru v hovädzom mäse je 76 mg%, v mlieku - 106, vo vajciach -
37106, v syre - 880, v prose - 19, v zemiakoch - 54, v jablkách - 5 mg%.
Významný je obsah chlóru v krvi a iných telesných tekutinách, ako aj v koži, pľúcach a obličkách. Chlór je v organizme v ionizovanom stave vo forme aniónov solí sodíka, draslíka, vápnika, horčíka, mangánu. Zlúčeniny chlóru v potravinách sú vysoko rozpustné a ľahko sa vstrebávajú v ľudskom čreve. Anióny chlóru spolu s katiónmi sodíka zohrávajú dôležitú úlohu pri vytváraní a regulácii osmotického tlaku krvi a iných telesných tekutín. Soli chlóru zabezpečujú tvorbu kyseliny chlorovodíkovej sliznicou žalúdka.
Hlavnú potrebu chlóru uspokojuje chlorid sodný, ktorý sa do potravín pridáva vo forme soli.
Celkové množstvo chloridu sodného v ľudskom tele je zvyčajne 10-15 g, ale pri konzumácii potravín bohatých na chlórové soli môže obsah chlóru v ľudskom organizme dosiahnuť vyššie množstvo. Denná ľudská potreba chlóru je 5-7 g.
Síra sa v najvyšších množstvách nachádza v obilných výrobkoch, strukovinách, mliečnych výrobkoch, mäse, rybách a najmä vajciach. Je súčasťou takmer všetkých bielkovín ľudského tela a hojne sa v ňom nachádzajú najmä aminokyseliny – cystín, metionín. Výmena síry v organizme je najmä jej premena na uvedené aminokyseliny. Podieľa sa aj na tvorbe vitamínu Bg (tiamín), inzulínu a niektorých ďalších zlúčenín. V proteinoidoch podporných tkanív je veľa síry, napríklad v keratíne vlasov, nechtov atď.
Pri oxidácii zlúčenín v tele sa významná časť síry vylučuje močom vo forme solí kyseliny sírovej.
Denná potreba dospelého človeka na síru pri miernej práci je asi 1 g.
Jód je obsiahnutý v tele zdravého človeka s hmotnosťou 70 kg v množstve približne 25 mg. Polovica tohto množstva je v štítnej žľaze a zvyšok je vo svalovom a kostnom tkanive a v krvi. Jód anorganických zlúčenín v štítnej žľaze je nahradený organickými zlúčeninami - tyroxínom, dijódtyroxínom, trijódtyroxínom. Jód je rýchlo absorbovaný štítnou žľazou a niekoľko hodín po vstupe do nej sa mení na organickú
spojenia. Tieto zlúčeniny stimulujú metabolické procesy v tele. Pri nedostatočnom množstve jódu, ktorý sa dostáva do tela s potravou, dochádza k narušeniu činnosti štítnej žľazy a vzniku závažného ochorenia nazývaného endemická struma.
Najväčšie množstvo jódu sa nachádza v rastlinných a živočíšnych produktoch pobrežných oblastí, kde sa koncentruje v morskej vode, vzduchu a pôde pobrežných oblastí. Málo jódu sa hromadí v rastlinách a živočíšnych organizmoch horských alebo vzdialených od morských pobrežných oblastí jódu.
Obsah jódu v obilných výrobkoch, zelenine, sladkovodných rybách nepresahuje 5-8 mcg na 100 g surového produktu. Vyšším obsahom jódu vyniká hovädzie mäso, vajcia, maslo, ovocie. morská kapusta, morské ryby a rybí olej obsahujú najvyššie množstvo jódu. Plody Feijoa rastúce na pobreží Čierneho mora v Gruzínsku akumulujú až 390 mikrogramov jódu na 100 g ovocnej hmoty, čo je oveľa viac ako obsah tohto prvku v inom ovocí a zelenine.
V oblastiach, kde potravinárske výrobky obsahujú nedostatočné množstvo jódu, sa do kuchynskej soli pridáva jodid draselný v množstve 25 g K1 na tonu kuchynskej soli. Pri bežnej strave človek prijme 200 mikrogramov jódu denne s jódovanou soľou. Pri skladovaní jodizovanej soli sa však jód postupne vytráca, preto sa jodidovaná soľ po 6 mesiacoch predáva ako obyčajná kuchynská soľ.
Denná ľudská potreba jódu je 100-260 mcg.
Fluór hrá dôležitú úlohu v plastických procesoch pri tvorbe kostného tkaniva a zubnej skloviny. Najväčšie množstvo fluóru sa koncentruje v kostiach - 200-490 mg/kg a zuboch - 240-560 mg/kg.
Zdá sa, že hlavným zdrojom fluoridu v ľudskom tele je voda, pričom fluorid Doda sa vstrebáva lepšie ako fluorid z potravy. Obsah fluóru v pitnej vode sa pohybuje od 1 do 1,5 mg/l. Nedostatok fluóru vo vode často ovplyvňuje
39nne k rozvoju ochorenia zubov, známeho ako kaz. Nadbytok fluóru vo vode spôsobuje fluorózu, pri ktorej je narušená normálna štruktúra zubov, na sklovine vznikajú škvrny a zvyšuje sa krehkosť zubov. Nedostatkom alebo nadbytkom fluóru trpia najmä deti.
Denná ľudská potreba fluóru ešte nebola stanovená. Predpokladá sa, že optimálne množstvo fluoridu v pitnej vode pre zdravie by malo byť 0,5-1,2 mg/l.
Meď v organizme zvierat spolu so železom zohráva dôležitú úlohu v procesoch krvotvorby, stimuluje oxidačné procesy a je tak spojená s metabolizmom železa. Je súčasťou enzýmov (laktáza, askorbátoxidáza, cytochrómoxidáza atď.) ako kovová zložka.
V rastlinách meď podporuje oxidačné procesy, urýchľuje rast a zvyšuje úrodu mnohých plodín.
V tých malých množstvách, v ktorých sa meď nachádza v prírodných produktoch, neškodí ľudskému telu. Ale zvýšené množstvo medi môže spôsobiť otravu. Takže súčasný príjem 77-120 mg medi môže spôsobiť nevoľnosť, vracanie a niekedy hnačku. Preto obsah medi v potravinárskych výrobkoch upravujú súčasné predpisy Ministerstva zdravotníctva ZSSR. Na 1 kg produktu je v závislosti od obsahu pevných látok v ňom povolených 5 až 30 mg medi. Takže v koncentrovanej paradajkovej paste by obsah medi nemal prekročiť 30 mg / kg, v paradajkovom pretlaku - 15-20, v konzervovanej zelenine - 10, v džeme a marmeláde - 10, v ovocných kompótoch - 5 mg / kg.
Meď sa môže dostať do potravinárskych produktov pri ich výrobe – z medených častí zariadení, keď sa vinohrady ošetrujú pesticídmi s obsahom medi atď.
Denná potreba medi u dospelého človeka je 2 mg.
Zinok sa nachádza vo všetkých tkanivách zvierat a rastlín. S nedostatkom zinku v organizme mladých žien,
U rastlín sa ich rast oneskoruje a pri jeho nedostatku v pôde dochádza k chorobám mnohých rastlín, čo často vedie k ich úhynu.
Zinok je súčasťou množstva enzýmov a dôležitá je najmä jeho úloha v molekule enzýmu karboanhydrázy, ktorá sa podieľa na väzbe a vylučovaní oxidu uhličitého z tela zvieraťa. Zinok je nevyhnutný pre normálnu funkciu hormónov hypofýzy, nadobličiek a pankreasu. Má tiež vplyv na metabolizmus tukov, zvyšuje odbúravanie tukov a zabraňuje stukovateniu pečene.
Zinok v potravinách vo vysokých množstvách môže spôsobiť otravu. Kyslé a mastné potraviny rozpúšťajú kovový zinok, a preto je varenie alebo skladovanie potravín v zinkových zariadeniach alebo nádobách neprijateľné. Otrava zinkom je podobná otrave meďou, je však výraznejšia a sprevádza ju pálenie a bolesť v ústach a žalúdku, vracanie, hnačka a srdcová slabosť. Zinkový riad je povolený len na skladovanie studenej pitnej vody, pretože v tomto prípade je rozpustnosť zinku zanedbateľná.
Denná potreba zinku u dospelého človeka je 10-15 mg. Zvýšená potreba zinku sa pozoruje počas rastu a puberty. Pri bežnej strave človek prijíma dostatočné množstvo zinku z potravy.
Olovo sa nachádza v živočíšnych a rastlinných produktoch vo veľmi malých množstvách. Takže v jablkách, hruškách, hrozne, jahodách je obsah olova asi 0,1 mg na 1 kg produktu, v mlieku - 0,8, v mäse - 0,05, v jeseterovi - 0,06 mg na 1 kg.
Olovo je pre človeka toxický kov, má schopnosť hromadiť sa v organizme, hlavne v pečeni, a spôsobovať ťažké chronické otravy.
Pri dennom príjme 2-4 mg olova s jedlom sa po niekoľkých mesiacoch môžu objaviť príznaky otravy olovom.
41 Kontaminácia potravín olovom môže pochádzať z riadu, spájok, glazúr, zariadení a insekticídov obsahujúcich olovo. Najčastejšie k otrave olovom dochádza pri skladovaní potravín v remeselnej kamenine, ktorá nie je dobre pokrytá olovenou glazúrou.
Kvôli vysokej toxicite nie je povolený obsah olova v potravinárskych výrobkoch.
Cín sa v potravinách nachádza v malom množstve. V pečeni býka a barana sa teda našlo 0,14 mg/kg cínu, v obličkách 0,003, v pľúcach 0,63 a v mozgu 0,019 mg/kg.
Cín nie je taký toxický kov ako olovo, zinok alebo meď, preto je povolený v obmedzenom množstve v zariadeniach potravinárskych podnikov, ako aj na pocínovanie povrchu cínu, z ktorého sa pripravujú plechovky, ktoré ho chránia pred koróziou. Často však pri dlhodobom skladovaní konzervovaných potravín v konzervách dochádza k interakcii hmoty výrobku s cínovým povlakom cínu, v dôsledku čoho vznikajú cínové soli organických kyselín. Tento proces je obzvlášť aktívny, keď sú v plechovke výrobky s vysokou kyslosťou - ovocie, konzervované ryby a zelenina paradajková omáčka a iné.Pri dlhodobom skladovaní sa môže výrazne zvýšiť obsah cínu v konzervách. Obsah cínu sa obzvlášť rýchlo zvyšuje vo výrobkoch, ktoré sú v otvorených kovových plechovkách potiahnutých cínom.
Na zvýšenie ochrany plechovky proti korózii sa na povrch plechovky dodatočne nanášajú špeciálne kyselinovzdorné laky alebo emaily, prípadne sa na povrchu plechovky vytvorí tenký film stabilných oxidov cínu.
Mangán je široko distribuovaný v živočíšnych a rastlinných produktoch. Aktívne sa podieľa na tvorbe mnohých enzýmov, tvorbe kostí, procesoch hematopoézy a stimuluje rast. V rastlinách mangán podporuje proces fotosyntézy a tvorbu kyseliny askorbovej.
Rastlinné produkty sú vo väčšine prípadov bohatšie na mangán ako živočíšne produkty. Takže obsah mangánu v obilných výrobkoch dosahuje 1-15 mg na 1 kg v liste
zelenina - 10-20, v ovocí - 0,5-1, v mlieku - 0,02-0,03, vo vajciach - 0,1-0,2, v pečeni zvierat - 2,65-2,98 mg na 1 kg.
Pri nedostatku mangánu v pôde rastliny ochorejú a zle sa vyvíjajú, úroda ovocia, zeleniny a iných plodín klesá. Pridávanie mikrohnojív s obsahom mangánu do pôdy pomáha zvýšiť úrodu.
Denná potreba dospelého človeka na mangán je 5-10 mg denne.
Rádioaktívne izotopy sú prítomné v ľudskom tele, neustále vstupujú a vystupujú z tela. Existuje rovnováha medzi príjmom rádioaktívnych zlúčenín do tela a ich odstránením z tela. Všetky potravinárske výrobky obsahujú rádioaktívne izotopy draslíka (K40), uhlíka (C14), vodíka (H3) a tiež rádia s jeho produktmi rozpadu.
Najvyššia koncentrácia pripadá na draslík (K40). Izotopy sa podieľajú na metabolizme spolu s nerádioaktívnymi.
Predpokladá sa, že počas nasledujúceho geologického obdobia nenastali na Zemi žiadne veľké zmeny v intenzite žiarenia, teda u zvierat a flóry vyvinul určitý druh imunity voči týmto úrovniam žiarenia. Ale živé organizmy sú veľmi citlivé na zvýšené koncentrácie. Malé koncentrácie zvyšujú rast živých organizmov, veľké koncentrácie spôsobujú výskyt aktívnych radikálov, v dôsledku čoho dochádza k narušeniu životnej činnosti jednotlivých orgánov a tkanív, ako aj celého organizmu.
o atómové výbuchy rádioaktívne izotopy dopadajú na zemský povrch a znečisťujú atmosféru, vodu, pôdu a rastliny. Prostredníctvom potravy, atmosféry a vody sa rádioaktívne izotopy dostávajú do ľudského tela.
Zistilo sa, že keď sú potravinárske výrobky ošetrené žiarením rádioaktívnych izotopov, ich skladovateľnosť sa zvyšuje a klíčenie zemiakov sa oneskoruje. Ale zvyčajne môže mať ožiarené jedlo špecifickú vôňu a chuť a je možné, že sa môžu vytvárať toxické látky. Na určenie bezpečnosti takýchto produktov sú potrebné dlhodobé experimenty.
testovacie otázky
Aké chemické prvky sú makroživiny?
Aké sú funkcie minerálov v ľudskom tele?
Aká je úloha vápnika v ľudskom tele?
Aké chemické prvky sú klasifikované ako stopové prvky a aké sú ich funkcie v ľudskom tele?
Akú úlohu hrá železo v ľudskom tele a v akých potravinách sa nachádza?
Aké sú dôsledky nedostatku jódu v tele a ako sa tomu dá vyhnúť?
Aké druhy technologického spracovania surovín a potravinárskych výrobkov prispievajú k úbytku minerálov?
Uveďte príklady vzájomného pôsobenia niektorých mikroelementov a vitamínov.
Aké metódy na stanovenie obsahu makro- a mikroprvkov poznáte?
Kukushkin ľan sa rozmnožuje: zoospórami;
semená za nepriaznivých podmienok;
spory; +
aplanospóry.
- listy jahôd:
nepárové perovité;
trojčlenný; +
trojlistový, jednolistový;
komplexná unifolia. Včely robotnice sú:
asexuálnych jedincov;
samice s nedostatočne vyvinutými reprodukčnými orgánmi; +
muži s nedostatočne vyvinutými reprodukčnými orgánmi;
samcov a samíc s normálne vyvinutými reprodukčnými orgánmi, ktoré sa však dočasne nerozmnožujú. Trávenie v koralových polypoch:
iba dutina;
iba intracelulárne;
brušné a intracelulárne; +
dutina, vnútrobunková a vonkajšia. Pteropódne mäkkýše, ktoré majú schopnosť svietiť v tme, môžu byť súčasťou:
bentos;
neuston;
fytoplanktón;
zooplanktón. + Vývojový cyklus muchy bol prvýkrát opísaný:
Anton Levenguk;
Francesco Redi; +
Henri Fabre;
Louis Pasteur. Húsenice motýľov majú:
tri páry prsných nôh;
tri páry hrudných nôh a päť párov ventrálnych falošných nôh; +
osem párov falošných nôh;
chýbajú končatiny. Obehový systém lanceletu:
OTVORENÉ;
uzavretý, existuje jeden kruh krvného obehu; +
uzavreté, existujú dva kruhy krvného obehu;
chýba. Vyberte správne vety:
- Vyberte správne vety:
- V cyklostómoch má tráviaci trakt:
tvar rovnej rúrky;
pečeňový výrastok;
pylorické výrastky;
špirálový ventil. + Z rýb rádu jesetera nie je prechádzajúci pohľad:
beluga;
hviezdicový jeseter;
sterlet; +
jeseter. Slinné žľazy počas evolúcie stavovcov sa prvýkrát objavujú v:
pľúcnik;
obojživelníky; +
plazy;
cicavcov. Z rýb radu treska žije a neresí sa iba v sladkej vode:
treska;
treska jednoškvrnná;
burbot; +
pollock. Pôvod vtáčieho krídla z voľnej prednej končatiny charakteristickej pre štvornohé stavovce názorne ilustruje príklad kurčiat:
pštros;
kiwi;
hoatzin; +
tučniak. O aerodynamických vlastnostiach vtáka počas letu neovplyvňovať perie:
zotrvačníky;
páperovité; +
riadenie;
obrys. Medzi vtákmi je stereoskopické videnie najrozvinutejšie u druhov:
hmyzožravce;
zrnožravé;
mäsožravé; +
planktožravý.
Glykokalyx živočíšnych buniek tvorí:
proteíny a lipidy;
proteíny a nukleotidy;
bielkoviny a sacharidy; +
sacharidy a nukleotidy.
Proces, ktorým améba s dysenterickou chorobou pohlcuje červené krvinky:
osmóza;
pinocytóza;
fagocytóza; +
uľahčená difúzia.
Pozostatky Pithecanthropus boli prvýkrát objavené v:
Južná Afrika;
Austrália;
Stredná Ázia;
Juhovýchodná Ázia. +
Najstarší z menovaných fosílnych predkov človeka je:
neandertálec;
Pithecanthropus;
Australopithecus; +
Cro-Magnon.
Organely nachádzajúce sa v bunkách prokaryotov aj eukaryotov:
endoplazmatické retikulum;
mitochondrie;
lyzozómy;
ribozómy. +
Hlavné zložky eukaryotického jadrového chromatínu sú:
DNA a RNA;
RNA a proteíny;
DNA a proteíny; +
DNA a lipidov. mikrotubuly neposkytujú:
udržiavanie tvaru bunky;
zmena tvaru bunky; +
pohyb organel;
pohyb chromozómov počas delenia buniek. Bunkové proteíny určené na sekréciu sa triedia a balia do:
lyzozómy;
endozómy;
endoplazmatické retikulum;
trans Golgiho siete. +
Umiestnenie enzýmu ATP syntetázy v mitochondriách je:
matrica;
medzimembránový priestor;
vonkajšia membrána;
vnútorná membrána. +
Oxidácia organických zlúčenín na CO2 v mitochondriách prebieha:
v matrici; +
v medzimembránovom priestore;
na vonkajšej membráne;
na vnútornej membráne.
Antikodón obsahuje:
jeden nukleotid;
dva nukleotidy;
tri nukleotidy; +
štyri nukleotidy.
Konečný akceptor elektrónov v bunkovom dýchaní je:
NADH;
voda;
kyslík; +
ATP.
Vlastnosť genetického kódu, ktorá zvyšuje spoľahlivosť uchovávania a prenosu genetickej informácie:
triplet;
univerzálnosť;
nadbytok; +
nedostatok interpunkčných znamienok.
Ióny horčíka sú súčasťou:
hemoglobín;
inzulín;
chlorofyl; +
tyroxínu. Molekuly RNA schopné vykazovať katalytickú aktivitu sa nazývajú:
ribonukleázy;
ribozómy;
ribozýmy; +
ribonukleotidy. Makroergické zlúčeniny sa nazývajú:
charakterizované prítomnosťou kovalentných väzieb s vysokou energiou;
pri deštrukcii určitých väzieb, v ktorých sa uvoľňuje veľké množstvo voľnej energie; +
ktorých syntéza nastáva s vynaložením veľkého množstva energie;
ktoré pri horení vydávajú veľa tepla.
V procese fotosyntézy je zdrojom kyslíka ako vedľajšieho produktu:
ribulóza bisfosfát;
glukóza;
voda; +
oxid uhličitý.
Vývoj nitrifikačných baktérií vedie k:
acidifikácia prostredia; +
alkalizácia prostredia;
neutralizácia životného prostredia;
neovplyvňuje pH média.
Acidophilus sa tvorí v dôsledku fermentácie mlieka:
baktérie mliečneho kvasenia; +
kvasnice;
zmiešaná kultúra baktérií mliečneho kvasenia a kvasiniek;
zmiešaná kultúra baktérií kyseliny mliečnej a kyseliny propiónovej.
Z týchto chorôb je spôsobená vírusom:
cholera;
kiahne; +
mor;
malária.
Zo zložiek rastlinných buniek vírus tabakovej mozaiky infikuje:
mitochondrie;
chloroplasty; +
jadro;
vakuoly.