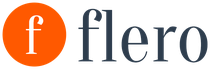Mineralne soli daju koštanog tkiva snaga, krutost. I povećani i smanjeni sadržaj mineralnih soli u koštanom tkivu umanjuje njegove karakteristike čvrstoće. U djece, nedovoljna mineralizacija koštanog tkiva otežava rast cjevastih kostiju, što dovodi do njihove zakrivljenosti. Nedovoljna mineralizacija ima negativan utjecaj na čvrstoću kostiju i u odrasloj dobi.
S prekomjernim sadržajem mineralnih soli, koštano tkivo postaje krhko, njegova snaga se značajno smanjuje.
Kiseline i soli topive u vodi nalaze se u tijelu u ioniziranom obliku. Od kationa najveći je sadržaj iona Na +, K+, Ca 2+, Mg 2+, Zn 2+, Fe 3+, Fe 2+. Zn 2+, Ni 2+, Cr 3+, Mn 2+, Cd 2+, Ba 2+, Cu 2+, Co 2+, Mo 2+ i neki drugi ioni metala sadržani su u znatno manjim količinama. Zbog niskog sadržaja u tijelu, ti se ioni nazivaju elementima u tragovima.
Od aniona najzastupljeniji su kiseli ostaci ugljične, klorovodične i fosforne kiseline. Anion sumporne kiseline sadržan je u znatno manjim količinama.
Ioni mogu biti i u slobodnom i u vezanom stanju u sastavu različitih spojeva tijela. Funkcije slobodnih i vezanih iona su različite. Ioni određuju osmotski tlak bioloških tekućina, stvaraju električni potencijal staničnih membrana, osiguravaju stvaranje i prijenos živčanih impulsa, djeluju kao aktivatori, kofaktori ili komponente enzima i drugih biološki aktivnih spojeva.
Zaustavimo se detaljnije na sadržaju i ulozi pojedinih iona u tijelu.
kalcijevi ioni. Kalcijevi ioni nalaze se i u krvi i u stanicama tijela. Sadržaj Ca 2+ u krvi je približno 5,7 mg% (5,7 mg na 100 ml krvi). Neravnomjerno je raspoređen između plazme i oblikovanih elemenata. Eritrociti ga sadrže oko 1,0 mg%, leukociti - oko 4,0-5,0 mg%. U krvnoj plazmi koncentracija kalcija je izrazito viša.
U stanicama tijela, kalcij je uglavnom lokaliziran u mitohondrijima, sarkoplazmatskom retikulumu i ribosomima.
Kalcijevi ioni aktiviraju fagocitnu funkciju leukocita, povećavaju otpornost organizma na infekcije i intoksikacije, smanjuju propusnost kapilara te tako djeluju protuupalno i antialergijsko. Oni normaliziraju ekscitabilnost perifernog živčanog sustava, potiču aktivnost simpatičkog živčanog sustava. Visoko važna uloga kalcijevi ioni igraju u konjugaciji ekscitacije s kontrakcijom u srčanim i skeletnim mišićima.
To nije ograničeno na ulogu kalcijevih iona u tijelu. Oni su dio staničnih membrana, osiguravajući njihovu stabilizaciju, sudjeluju u sinaptičkom prijenosu živčanih impulsa i regulatori su aktivnosti mnogih enzima. Kalcijevi ioni neophodni su za provođenje aktivnosti niza endokrinih žlijezda (hipofiza, nadbubrežne žlijezde), žlijezde probavni sustav. Oni aktivno sudjeluju u procesima zgrušavanja krvi.
Ioni Na + i K +. Vrijednost natrijevih iona u tijelu je izuzetno visoka. Na + ioni su glavni ioni u krvnoj plazmi i izvanstaničnoj tekućini. Oni igraju važnu ulogu u održavanju ravnoteže vode u ljudskom tijelu. Sadržaj natrijevih iona u tijelu određuje volumen tekućine (vode) i svako kršenje njezina metabolizma odmah dovodi do preraspodjele, zadržavanja ili gubitka vode.
Koncentracija natrijevih iona u tjelesnim tekućinama je čimbenik koji utječe na aktivnost određenih enzima, posebice enzima anaerobnih transformacija ugljikohidrata, kao i enzima koji osiguravaju skladištenje energije u makroergijskim fosfatnim spojevima.
Nedostatak natrija dovodi do niza poremećaja u tijelu: tkiva su dehidrirana, poremećena je cirkulacija krvi, gubi se apetit, smanjuju se mentalne sposobnosti. Svi ovi poremećaji u većini slučajeva nisu posljedica nedostatka soli (glavnog izvora natrija i klora za tijelo) u hrani, već njezinih velikih gubitaka u određenim stanjima i bolestima: povraćanje, proljev, pretjerano znojenje.
Natrijevi ioni obavljaju važne funkcije u održavanju acidobazne ravnoteže u tijelu. To se djelovanje očituje, posebice, u bubrezima. U bubrežnim tubulima, natrijevi ioni se reapsorbiraju u zamjenu za izlučene vodikove ione. Tako je osigurano očuvanje konstantnosti pH tijekom stvaranja kiselih metabolita i očuvanje natrijevih iona u tijelu. Ova sposobnost u bubrezima je toliko visoka da omjer koncentracija vodikovih iona u urinu i krvi može doseći i do 800:1.
Budući da je glavni izvor natrija za tijelo kuhinjska sol, obično se kaže da je potrebna kuhinjska sol, a ne natrij. Kod odrasle osobe, potreba za kuhinjskom soli je 4-5 g dnevno. Povećana potreba za kuhinjskom soli može biti povezana s određenim bolestima, kao i pojačano znojenje, u kojem se gube mnogi natrijevi ioni. To uzrokuje povećanu potrebu za soli kod sportaša. Osobito je velika potreba za soli kod ljudi koji se bave sportom u kojem su treninzi i natjecateljske aktivnosti povezane s obilnim znojenjem.
Za razliku od natrija, ioni kalija nalaze se uglavnom u stanicama organa i tkiva. Ukupna količina kalija u ljudskom tijelu težine 70 kg iznosi oko 140 g. Od ove količine samo je oko 25 g u izvanstaničnom prostoru. Najveći sadržaj kalijevih iona u eritrocitima, mišićnim vlaknima, stanicama jetre.
Većina intracelularnog kalija povezana je s proteinima, ugljikohidratima, fosfatima, kreatin fosfatom. Mnogi procesi sinteze u tijelu zahtijevaju prisutnost kalijevih iona. Dakle, kalij sudjeluje u sintezi glikogena. Uz povećanu glukoneogenezu u jetri i mišićima, uočava se smanjenje koncentracije slobodnih iona kalija. Naprotiv, s intenzivnom razgradnjom glikogena, na primjer, tijekom intenzivnog mišićnog rada, koncentracija slobodnih iona kalija značajno raste.
Vezanje kalijevih iona opaža se tijekom sinteze proteina, ATP-a, kreatin fosfata. Tako se tijekom sinteze svakih 2 g proteina veže približno 1 meq kalijevih iona. S nedostatkom kalija u tijelu, sinteza ovih spojeva je poremećena.
Kalij aktivno sudjeluje u prijenosu živčanih impulsa u sinaptičkim formacijama, sudjeluje u sintezi acetilkolina, posrednika živčane ekscitacije. Uz natrijeve ione, kalij sudjeluje u polarizaciji stanične membrane i pobuđivanju stanice, osiguravajući kontrakciju mišića.
Kalijevi ioni sudjeluju u regulaciji srčane aktivnosti. Srce je vrlo osjetljivo na fluktuacije koncentracije kalija u krvi. Također ima vazodilatacijski učinak.
Magnezijevi ioni. Ukupna količina magnezija u ljudskom tijelu težine 70 kg iznosi oko 14,4 g. Najveći sadržaj magnezija je u koštanom tkivu, gdje se nalazi u obliku fosfatnih, ugljičnih i fluoridnih soli. Koštani pepeo sadrži do 1,5% magnezija. Koštano tkivo sadrži određenu količinu magnezijevih soli topljivih u vodi, koje stvaraju svoju vrstu tjelesnog depoa. Nedostatak magnezijevih soli u koštanom tkivu uzrokuje kašnjenje u njihovom rastu u duljinu i debljinu.
Magnezij je dio krvi, mišića, jetre, bubrega i drugih organa i tkiva te u njima obavlja različite i važne funkcije. Aktivator je niza enzima: kolinesteraze, fosfoglukomutaze, pirofosfataze, arginaze, karboksilaze, intestinalne dipeptidaze. Magnezij je neophodan u sintezi acetilkolina, za nastanak glikolize, u sintezi proteina, stvaranju i razgradnji ATP-a. Sudjeluje u kontrakciji mišića, regulaciji srčane aktivnosti. Brojna istraživanja pokazala su obrnutu vezu između smrtnosti od srčanih bolesti i sadržaja ioniziranog magnezija u tijelu, kao i u vodi za piće kao glavnom izvoru magnezija za organizam.
Osim već spomenutih, magnezij obavlja i druge funkcije u ljudskom tijelu, a njegov nedostatak ili višak može uzrokovati ozbiljne poremećaje. Dakle, magnezij je neophodan za apsorpciju probavnih proizvoda u gastrointestinalnom traktu. Međutim, višak magnezija smanjuje brzinu apsorpcije nekih od njih, posebice masnih kiselina zbog stvaranja netopivih kompleksa s njima.
Nedostatak magnezija dovodi do značajne promjene mineralnog sastava stanica, do povećanja koncentracije triglicerida u krvi, masne jetre, kalcifikacije krvnih žila i smanjenja njihovog sadržaja elastina. Nedostatak magnezija uzrokuje nekrozu i žarišta kalcifikacije u miokardu, hiperemiju sluznice očiju, nosa, usta, gubitak kose, konvulzije i u konačnici može dovesti do smrti tijela.
Ioni klora. Sadržaj klora u ljudskom tijelu težine 70 kg iznosi oko 88,7 g. Ioni klora su glavni anioni u krvnoj plazmi, čine oko 75% ukupne količine aniona u krvi. Kao i natrijevi ioni, ioni klorida sudjeluju u održavanju osmotskog tlaka krvne plazme i drugih bioloških tekućina. S tim u vezi, sadržaj vode u tijelu i pojedinim organima i tkivima uvelike je određen koncentracijom kloridnih iona. Višak kloridnih iona popraćen je povećanim sadržajem vode, nedostatak dovodi do gubitka vode.
Ioni klora sudjeluju u detoksikaciji organizma vežući otrovne produkte metabolizma. Konkretno, oni sudjeluju u uklanjanju amonijaka i vodikovih iona iz tijela kroz bubrege. Dio amonijaka koji nastaje u tjelesnim stanicama u procesu deaminacije aminokiselina i drugih spojeva koji sadrže dušik isporučuju se u bubrege glutaminskom ili asparaginskom kiselinom. Tamo se cijepa od naznačenih aminokiselina i spaja s kloridnim i vodikovim ionima da nastane amonijev klorid (NH 4 Cl), koji se eliminira iz tijela mokraćom. Istodobno se ioni vodika vežu i uklanjaju iz tijela, što osigurava održavanje acidobazne ravnoteže tijela. Reakcija se odvija prema jednadžbi:
NH 3 + H + + Cl¯ → NH 4 Cl
Klor ulazi u tijelo uglavnom u kombinaciji s natrijem (kao dio kuhinjske soli). Prethodno spomenuta potreba za kuhinjskom soli zadovoljava potrebe ljudskog organizma i za natrijem i za klorom.
Mikroelementi. Osim navedenog, ljudsko tijelo sadrži niz iona u malim koncentracijama (ne većim od 0,001%) To uključuje: Fe 2+, Zn 2+, Mn 2+, Mo 2+, Co 2+, J‾ i neke druge. Zbog malog sadržaja u tijelu nazivaju se elementima u tragovima. Funkcije elemenata u tragovima u ljudskom tijelu su raznolike, iako uloga nekih od njih još nije dovoljno proučena. Zadržimo se na ulozi nekih elemenata u tragovima.
Ioni željeza dio su krvnog hemoglobina i mioglobina sadržanih u mišićnom tkivu, drugim tkivima i organima. Fe 2+ ioni sudjeluju u isporuci kisika u tkiva, osiguravajući njegov prijelaz iz krvi u tkiva i taloženje u njima. Osim toga, ion željeza je dio enzima aerobne oksidacije (citokromi), kao i katalaze, enzima koji razgrađuje vodikov peroksid nastao u procesima biološke oksidacije.
Intenzivna mišićna aktivnost popraćena je značajnim povećanjem energetskog metabolizma i, posljedično, povećanjem razgradnje spojeva koji sadrže željezo koji su uključeni u njegovu opskrbu, povećanje metabolizma željeza općenito. Istodobno, stupanj apsorpcije željeza iz hrane je vrlo nizak. Kao rezultat toga, tijekom razdoblja intenzivnog treninga može doći do stanja nedostatka željeza u tijelu i potrebe za korištenjem preparata koji sadrže spojeve željeza kao dodatne nutritivne čimbenike.
Cinkovi ioni dio su brojnih enzima koji sudjeluju u reakcijama sinteze i kataboličkim procesima. Neophodni su za procese prijenosa genetskih informacija u stanici, za sintezu hemoglobina. Ioni cinka sudjeluju u stabilizaciji strukture određenih makromolekula, procesa rasta tijela, aktivnosti imunološkog sustava, procesa zacjeljivanja rana, razvoja mozga u fetusa, te potiču hormonsku funkciju gušterače.
Ioni mangana sudjeluju u metabolizmu glukozaminoglikana, koji su dio vezivnog tkiva, glukoze, glikogena i lipida. Oni igraju posebno važnu ulogu u metabolizmu u mozgu. S nedostatkom mangana, metabolizam u vezivnom tkivu, mozak je poremećen, stopa sinteze glikogena se smanjuje.
Mehanizam djelovanja manganovih iona u mnogočemu još nije jasan, do sada je jasno prikazana samo njegova uloga kofaktora niza enzima, posebice glikoziltransferaza.
Kobalt je uključen u eritropoezu (sintezu hemoglobina) i regulaciju metabolizma željeza u tijelu. Ima važnu ulogu u regulaciji lipida u krvi i nekih metaboličkih reakcija koje se javljaju u srcu, živčanom tkivu i zidovima gastrointestinalnog trakta.
Ioni bakra, nikla, kroma i drugih elemenata u tragovima obavljaju važne funkcije u tijelu. Dakle, bakar sudjeluje u stvaranju flavoproteina i citokrom oksidaze - enzima energetskog metabolizma, ima aktivacijski učinak na glikolizu. Neki elementi u tragovima sastavni su dio ne samo enzima, već i hormona. Dakle, jod je strukturna komponenta hormona štitnjače: tiroksina i trijodtironina.
Magnezij je jedan od najvažnijih i nezamjenjivih elemenata u tragovima za ljudski organizam. A tijekom razdoblja rađanja djeteta, potreba za njim se povećava nekoliko puta. Važan je kako za normalno funkcioniranje majčinog tijela i uspješnu trudnoću, tako i za normalan rast i razvoj bebe.
Ovaj element u tragovima je uključen u mnoge metaboličke procese, doprinosi normalnom funkcioniranju mišićnog, koštanog, živčanog i imunološkog sustava. Zato njegov nedostatak za trudnicu može zaprijetiti ozbiljnim posljedicama.
Koja je uloga magnezija?
Magnezij je uključen u mnoge metaboličke procese u tijelu. Pomaže u normalizaciji procesa prijenosa živčanih impulsa u mišićnom tkivu, opušta mišiće, smanjuje njihov pretjerani tonus i smiruje živčani sustav.
Često se ženi u fazi pripreme za začeće propisuje dodatni unos magnezija. Dokazano je da magnezij potiče i regulira proces prijenosa genetskog materijala roditelja na dijete. Ion Mg 2+ sudjeluje u sintezi strukturnih komponenti DNK.
Također, ovaj mikroelement aktivno sudjeluje u sintezi proteina, koji su izravno građevinski materijal za unutarnje organe i sustave bebe.
Magnezij također sudjeluje u punom funkcioniranju posteljice tijekom cijele trudnoće, regulirajući putem njega metabolizam između organizama majke i djeteta.
Zašto je nedostatak magnezija opasan za trudnice?
Nedostatak magnezija (hipomagnezijemija) može izazvati nastanak nedostataka u mrvicama prenatalni razvoj mišićno-koštanog sustava ili srca. Nedostatak magnezija može dovesti do prijevremenog poroda ili prijetećeg pobačaja.
Na kasnijim datumima a u porodu je magnezij jednako važan za trudnicu kao i tijekom cijele trudnoće. Nedostatak ovog mikroelementa dovodi do smanjenja elastičnosti mišićnih vlakana i kršenja njihove kontraktilnosti, što može pridonijeti kršenju radne aktivnosti (slabost, neusklađena radna aktivnost). Kao rezultat toga, povećava se rizik od traume i rupture porođajnog kanala majke.
Potreba za magnezijem tijekom trudnoće povećava se za oko 30%. Uostalom, to sada trebaju dva organizma – majka i dijete.
Nadoknaditi nedostatak bilo kojih tvari potrebnih djetetu tijekom razdoblja trudnoća dolazi iz rezervi majčinog tijela. Stoga je jasno da buduća majka ponekad može imati očite znakove nedostatka elemenata u tragovima.
Ako s hranom u organizam ne ulazi dovoljno magnezija, tada ga tijelo uzima iz kostiju, zuba i endokrinih žlijezda. Tako pokušava nadoknaditi početno smanjenje razine magnezija u krvnoj plazmi.
Zato je to toliko važno trudnica spriječiti stanja s nedostatkom magnezija u bilo kojoj fazi – od planiranja trudnoće do samog poroda.
Kako odrediti nedostatak magnezija u tijelu?
Simptomi uočeni kod trudnica s nedostatkom magnezija:
S grč mišića
Često, s nedostatkom magnezija, buduća majka je zabrinuta zbog povlačenja bolova u donjem dijelu leđa i donjim ekstremitetima. Postoji ukočenost mišića i nelagoda u vratu.
Manjak magnezija očituje se i napetošću (kontrakcijom) mišića maternice. Žene opisuju ovo stanje kao “želudac se ukoči”, “želudac se nehotice napreže”. U tom slučaju dolazi do grčevite vučne boli u donjem dijelu trbuha. Takav povećani tonus maternice može dovesti do prekida trudnoće.
Još jedna manifestacija poremećene kontrakcije mišića u nedostatku magnezija su grčevi mišića potkoljenice. Oštra, uporna, vrlo bolna kontrakcija mišića lista javlja se uglavnom noću. Stanje je dosta neugodno, bolno.
Morate razumjeti da grčevi u donjim ekstremitetima mogu ukazivati ne samo na nedostatak magnezija, već i na nedostatak kalcija u tijelu trudnice.
Promjene u živčanom sustavu
Tijekom trudnoće, psihoemocionalno stanje svake žene se mijenja. Postoje brige za zdravlje bebe i vlastitu dobrobit. A s nedostatkom magnezija, ozbiljnost nervoze, nerazumne razdražljivosti, poremećaja spavanja, emocionalne labilnosti, plačljivosti i smanjene učinkovitosti značajno se povećava.
Promjene u kardiovaskularnom sustavu
Nedostatak magnezija očituje se povećanjem krvni tlak. Pritom se visokom tlaku pridružuju vrtoglavica i glavobolja. U pozadini povećanog tlaka, poremećen je venski odljev iz donjih ekstremiteta, što se očituje oticanjem nogu.
S izraženim nedostatkom magnezijevih iona može biti poremećena srčana vodljivost s razvojem aritmija i pojavom boli u predjelu srca.
Smanjenje razine magnezija u krvnom serumu ispod 0,7 mmol / l ukazuje na nedostatak ovog elementa u tragovima. U tom stanju poremećena je izmjena elektrolita (natrij, kalij, magnezij) tijekom kontrakcije srčanog mišića (miokarda).
S nedostatkom magnezija u tijelu poremećeno je i opuštanje mišićne stijenke žila. Kao rezultat toga, zbog stalnog umjerenog vazospazma, protok krvi u završne dijelove tijela je manji nego inače. Stoga osobe s nedostatkom magnezija postaju osjetljivije na hladnoću, prohladne čak i ljeti.
Promjene u probavnom sustavu
Nedostatak magnezija izaziva kršenje kontraktilnosti crijeva, odnosno njegove peristaltike. Stoga su zatvor i nadutost česti pratitelji takvog deficitarnog stanja.
Značajke prehrane s nedostatkom magnezija
Magnezij se iz hrane apsorbira u crijevima, uglavnom u tankom, ali djelomično u debelom dijelu. Ali, nažalost, samo 35% magnezija se apsorbira iz hrane kroz probavni trakt.
Što se može učiniti da se apsorbira više od 35% magnezija? Njegovu apsorpciju poboljšavaju vitamin B 6 i neke organske kiseline (mliječna, limunska, asparaginska).
Također je važno u kojem obliku magnezij ulazi u tijelo. Dakle, njegovi organski spojevi, na primjer, magnezijev citrat (spoj magnezija s limunskom kiselinom), magnezijev laktat (spoj magnezija s mliječnom kiselinom), dobro se apsorbiraju kroz crijeva. ALI anorganske soli praktički se ne apsorbira, na primjer, magnezijev sulfat.
Kako bi se spriječio nedostatak magnezija kod trudnice, potrebno je u prehranu uključiti namirnice bogate magnezijem. Tu spadaju: peršin, kopar, orasi, mahunarke, riba i plodovi mora, zobene pahuljice i heljda, lubenica, žumanjak, soja, mekinje, banane, komorač, kruh od cjelovitih žitarica.

Puno magnezija nalazi se u svim zelenim biljnim namirnicama. Zelena boja Daje biljkama klorofil. Ovo je posebna tvar, složena bjelančevina, zahvaljujući kojoj biljke provode vrlo važan proces fotosinteze.
Kemijska struktura klorofila slična je hemoglobinu proteina ljudske krvi. Samo hemoglobin sadrži ione željeza, a klorofil sadrži ione magnezija. Stoga jedite više zelenog povrća i voća. Ovo su najvažniji izvori magnezija za ljudski organizam.
No, najbogatije magnezijem ipak nisu zelene namirnice. Ispod je tablica prehrambenih lidera po sadržaju magnezija na 100 g proizvoda. Pogledajte koji vam je od ovih proizvoda najprikladniji za nadopunu zaliha magnezija u vašem tijelu.
| Naziv proizvoda | Sadržaj magnezija, mg/100 g jestivog dijela proizvoda |
|---|---|
| Sjemenke bundeve | 534 |
| pšenične mekinje | 448 |
| kakao 20% | 442 |
| sezam (pržene sjemenke) | 356 |
| indijski orah (sirov) | 292 |
| bademi (pečeni) | 286 |
| Pinjoli | 251 |
| soja (suhi grah) | 240 |
| Pšenične klice, sirove | 239 |
| heljda (sirova) | 231 |
| Lubenica | 224 |
| Kukuruzne pahuljice | 214 |
| Zobene pahuljice | 130 |
| suncokretove sjemenke (pečene) | 129 |
| Grašak oguljen | 128 |
| šipak (suhi) | 120 |
| orah | 100 |
Sada pogledajte koji čimbenici ometaju apsorpciju magnezija ili pridonose iscrpljivanju njegovih rezervi u tijelu.
- pića s kofeinom;
- monotona prehrana s viškom lako probavljivih ugljikohidrata i slatkiša;
- slatke gazirane pića;
- alkohol, pušenje;
- kronična bol ili stres;
- endokrine bolesti: hipotireoza, dijabetes melitus;
- bolesti praćene povećanim znojenjem;
- uzimanje određenih lijekova (diuretici, antikonvulzivi, kalcijeve soli).
Dnevne potrebe za magnezijem tijekom trudnoće i dojenja
Podaci o dnevnim potrebama za magnezijem za trudnice i dojilje u razni izvori su različiti. Nutricionisti i znanstvenici još nisu došli do konsenzusa.
Ispod je usporedna tablica povećanje potrebe za magnezijem, uzimajući u obzir dob žene. To su brojke kojih se drži najveći broj stručnjaka.
Kada se magnezij propisuje trudnici?
Nedostatak magnezija može se otkriti biokemijskim testom krvi.
- s umjereno teškim nedostatkom magnezija: 12 - 17 mg / l (0,5 - 0,7 mmol / l);
- s teškim nedostatkom magnezija: ispod 12 mg / l (0,5 mmol / l).
Pripravci magnezija indicirani su za nedostatak magnezija utvrđen kliničkim ispitivanjima, kao i za pojavu gore opisanih znakova nedostatka magnezija (razdražljivost, plačljivost, loš san, umor, grčevi mišića i dr.).
Dodatni unos magnezijevih pripravaka izravno je indiciran za hipertonus maternice. Ovo stanje se često razvija u prvom tromjesečju trudnoće i povećava rizik od pobačaja u ranim fazama.Događa se da se liječenje propisuje za cijelo razdoblje rađanja djeteta.
Pripravke magnezija liječnik može propisati kako u fazi planiranja trudnoće, tako i tijekom trudnoće u različito vrijeme.
Odabir pripravka magnezija, određivanje njegove doze, oblika doziranja i trajanja liječenja provodi samo liječnik pojedinačno u svakom slučaju.
Najčešće liječnik trudnicama propisuje magnezij u obliku lijeka Magne B 6. Ispod je opis ovog lijeka.
Primjena Magne B 6 u trudnica
Aktivni sastojci Magne B 6 su magnezijev laktat dihidrat i piridoksin hidroklorid (aktivni oblik vitamina B 6). Piridoksin poboljšava apsorpciju magnezija, potiče njegov ulazak u stanice tijela.
Proizvode se dvije verzije lijeka: Magne B 6 i Magne B 6 forte. Tijekom trudnoće dopušteno je uzimati bilo koji od ovih oblika. Razlika između njih leži u koncentraciji aktivnih tvari.
U Magna B 6 forte količina djelatne tvari je udvostručena. Također, zbog sadržaja raznih pomoćnih tvari, postignuta je visoka bioraspoloživost (sposobnost apsorpcije u tijelu). Stupanj apsorpcije Magne B 6 forte je oko 90%, dok je bioraspoloživost Magne B6 blizu 50%.
Postoje različiti oblici oslobađanja lijeka: obložene tablete bijela boja, ampule s otopinom za oralnu primjenu i ampule za injekcije (otopina za intramuskularnu ili intravensku primjenu). Otopina je dostupna u ampulama zatamnjenog stakla. U pakiranju od 10 ampula. Samo rješenje ima smeđa boja i miris karamele.
Dodijeljen Magne B 6th 6-8 tableta u danu. U pravilu se preporuča uzimati 2 tablete tri puta dnevno uz obrok. Lijek u ampulama za oralnu primjenu uzima se 2-4 ampule / dan. Ovaj oblik zahtijeva prethodno razrjeđivanje lijeka u 200 mililitara vode.
Kontraindikacije i nuspojave Magne B 6
Magne B 6 je kontraindiciran u:
- Preosjetljivost na lijek i njegove komponente.
- Zatajenje bubrega.
- Intolerancija fruktoze, malapsorpcija glukoze i galaktoze.
- Fenilketonurija, kada je poremećen metabolizam određenih aminokiselina.
- Djeca mlađa od 1 godine.
- Dojenje.
Magne B 6 se općenito dobro podnosi. Ali upute za lijek uključuju sljedeće moguće nuspojave:
- bol u trbuhu;
- poremećaji stolice u obliku proljeva;
- alergijske reakcije u obliku urtikarije, Quinckeovog edema.
Ako se ovi simptomi pojave tijekom uzimanja lijeka, odmah se obratite liječniku.
Je li dugotrajna suplementacija magnezijem sigurna?
Dugi tečaj u terapijskim dozama koje je propisao liječnik, uz normalnu funkciju bubrega, ne može dovesti do predoziranja lijekom. Apsorpcija magnezija i njegov ulazak u krv događa se postupno. Lijek se izlučuje putem bubrega. Stoga se zdravi bubrezi mogu nositi s metaboličkim proizvodima lijeka i njegovim viškom.
Pripravci magnezija prodiru u majčino mlijeko. Stoga se dojiljama ne preporučuje uzimanje ovog lijeka.
Kada propisujete suplemente magnezija, svakako obavijestite svog liječnika o uzimanju dodatnih multivitaminskih kompleksa ili drugih lijekova (kalcij, željezo). Liječnik mora izračunati potrebnu dozu magnezija, uzimajući u obzir sadržaj ovog elementa u tragovima u vašem kompleksu.
To je također važno jer su magnezij i kalcij antagonisti (konkurenti) u tijelu i međusobno ometaju apsorpciju. Njihov prijem treba podijeliti po vremenu. Također, ne možete uzimati magnezij i željezo u isto vrijeme, jer to smanjuje apsorpciju svakog od njih.
Unatoč činjenici da se pripravci magnezija smatraju sigurnima, nikada ih ne smijete sami prepisivati. Samo liječnik može izračunati dozu lijeka i tijek liječenja koji vam je potreban.
Uloga u životu biljaka
Sadržaj magnezija u biljkama je u prosjeku 0,07% (težinski). On sudjeluje u grandioznom djelu - akumulaciji sunčeve energije u procesu fotosinteze, budući da je središnji atom u molekuli klorofila. Klorofil apsorbira sunčevu energiju i uz njegovu pomoć pretvara ugljični dioksid i vodu u složene organske tvari: šećere, škrob itd. Magnezij je bitna komponenta ribosoma: uz njegovo sudjelovanje (zajedno s ATP) aminokiseline se vežu na tRNA tijekom biosinteze proteina . Magnezijevi ioni Mg 2+ „poprečno povezuju“ proteinske molekule u glomerule, održavajući strukturu proteinskih molekula. Magnezij katalizira sintezu ATP-a iz nukleozid-difosfata, aktivira enzimske sustave za pretvaranje jabučne kiseline u limunsku kiselinu, a oksalne kiseline u mravlju kiselinu i ugljični dioksid.
S nedostatkom magnezija smanjuje se prinos kultiviranih biljaka, poremećeno je stvaranje kloroplasta i klorofila: listovi (prije svega donji) postaju "mramorirani": blijede između žila i ostaju zeleni duž vena. Tkiva između žila mogu dobiti različitu boju - žutu, narančastu, crvenu, ljubičastu, zatim odumiru, počevši od rubova lišća: listovi se uvijaju i postupno otpadaju. Kod bora se opaža žutilo vrhova iglica.
Biljka-indikator visokog sadržaja magnezija je kostenets.
Životinjsko tijelo sadrži približno 0,03–0,07% magnezija (po masi), dio je kostiju i zuba, nalazi se u jetri, krvi, živčanom tkivu i mozgu te je uključen u metabolizam proteina i ugljikohidrata. S osobom od 70 kg, tijelo sadrži 19-20 g magnezija. Ima antiseptički i vazodilatacijski učinak, snižava krvni tlak i kolesterol u krvi, pojačava procese inhibicije u moždanoj kori, djeluje umirujuće (sedativno) na živčani sustav, ima važnu ulogu u aktiviranju obrambene snage tijelo u borbi protiv raka. Magnezij jača imunološki sustav, djeluje antiaritmično, potiče oporavak nakon fizičkog napora.

S nedostatkom Mg povećava se osjetljivost na srčani udar. To su pokazali eksperimenti mađarskih znanstvenika provedeni u 20. stoljeću. na životinjama (kod životinja se ova bolest naziva biljna tetanija). Neki psi su dobivali hranu bogatu magnezijevim solima, drugi - siromašnu. Do kraja pokusa, oni psi čija je prehrana bila siromašna magnezijem "zaradili" su infarkt miokarda.
Magnezij se iz organizma izlučuje urinom, izmetom i znojem.
Proizvodi od povrća: voće, orašasti plodovi (bademi, kikiriki, orasi), povrće (rajčica, krumpir, bundeva, grah, zelena salata), menta, radič, masline, peršin, cjelovita pšenica, zob, heljda; raženi kruh, proso, mekinje. Proizvodi životinjskog podrijetla: jetra, žumanjak.

MgSO 4- magnezijev sulfat, gorka ili Epsom sol.
MgCO 3– magnezijev karbonat, magnezit.
MgO- magnezijev oksid, spaljena magnezija.
Magnezijevi silikati: talk 3 MgO x 4 SiO 2 x H 2 O i azbest CaO x 3 MgO x 4 SiO 2.
Klorofil.
Znaš li to…
Magnezij je prvi 1808. godine dobio engleski kemičar G. Davy iz vlažnog oksida MgO. Naziv dolazi od lat. magnezija alba(bijeli magnezij), prema mineralu hidromagnezitu, koji sadrži ovaj metal, a pronašli su ga stari Grci u blizini grada Magnezije.

Broj atoma magnezija u ljudskom tijelu je 8,7 x 10 23, au jednoj stanici - 8,7 x 10 9.
Ukupna količina magnezija u klorofilu svih biljaka na Zemlji iznosi oko 100 milijardi tona.
Dnevni unos magnezija hranom u organizam trebao bi biti 240-720 mg.
Magnezijev sulfat MgSO 4 (gorka, ili Epsom sol) se u medicini koristi kao laksativ, koleretik i analgetik.
Ioni magnezija ne samo da morskoj vodi daju slan okus, već je čine i nepitkom, uzrokujući jak proljev i povraćanje.
Postoji nekoliko vrsta klorofila (klorofil a, b, c, d), koji se razlikuju po svojoj strukturi i spektru apsorpcije. Više biljke i alge sadrže klorofil kao glavni pigment. a, a kao dodatni - klorofil b, dijatomeje i smeđe alge - samo klorofil c, a crvene alge - klorofil d.
Željezo

Uloga u životu biljaka i mikroorganizama
Njegovim nedostatkom usporava se stvaranje klorofila. Možda pojava kloroze (žuta boja) na prvom mjestu mladog lišća, njihov gubitak boje. S dugotrajnim nedostatkom željeza u zeljastim biljkama, tkivo odumire uz rubove lisne ploče, izdanci odumiru na stablima, a ukupna produktivnost i otpornost biljaka na bolesti se smanjuje.
Pelin i neke druge biljke pokazatelj su visokog sadržaja željeza u tlu. Istodobno, lišće pelina postaje svijetlo žuto, a cvjetovi nekih biljaka, poput hortenzija, poprimaju neobičnu plavu boju.
U prirodi postoje takozvane željezne bakterije. U procesu kemosinteze oksidiraju fero željezo u feri željezo, koje se taloži na površini stanice. Nastali željezov (III) hidroksid taloži se i tvori takozvanu močvarnu rudu:
4FeCO 3 + O 2 + 6H 2 O ––> 4Fe(OH) 3 + 4CO 2 + energija
Kemosintetske bakterije koje oksidiraju spojeve željeza i mangana otkrio je akademik S.N. Vinogradsky. Izuzetno su rasprostranjeni i u slatkim i u morskim vodama. Zahvaljujući njihovoj vitalnoj aktivnosti, na dnu močvara i mora stvara se ogromna količina naslaga željeza i mangana. U I. Vernadsky, utemeljitelj biogeokemije, govorio je o naslagama takvih ruda kao rezultat vitalne aktivnosti bakterija u drevnim geološkim razdobljima.
Uloga u životu životinja i ljudi
Tijelo životinje sadrži približno 0,01% željeza (po masi). Željezo je neophodno u procesima hematopoeze i unutarstaničnog metabolizma. Otprilike 55% željeza je dio hemoglobina eritrocita, oko 24% je uključeno u stvaranje bojene tvari mišića (mioglobin), otprilike 21% se taloži "u rezervi" u jetri i slezeni.

Željezo je ono što određuje boju krvi, kao i njezinu sposobnost vezanja i oslobađanja kisika. Crvene krvne stanice prenose kisik iz pluća po cijelom tijelu i uklanjaju ugljični dioksid. Kisik je jako oksidacijsko sredstvo, ali hemoglobin, zahvaljujući željezu koje sadrži, može prenositi kisik. Ljudsko tijelo sadrži enzime koji sadrže željezo. Tu je i proteinski kompleks feritina, iz kojeg nastaju sve ostale tvari koje sadrže željezo potrebne za tijelo. Ioni željeza u tijelu se prenose pomoću kompleksnog proteina transferina (koji se nalazi u krvnoj plazmi, mlijeku, bjelanjku). Željezo ima važnu ulogu u procesima oslobađanja energije, u enzimskim reakcijama, u osiguravanju imunoloških funkcija, u metabolizmu kolesterola.
S osobom od 70 kg, tijelo sadrži 4,2-5 g željeza. Dnevna potreba odrasle zdrave osobe za željezom je 10-20 mg i nadopunjuje se normalnom uravnoteženom prehranom.
Sa smanjenjem količine željeza u krvi dolazi do anemije. Najčešća je anemija zbog nedostatka željeza ili, kako se već dugo naziva, anemija.

Željezo se iz tijela izlučuje urinom, izmetom i znojem.
Glavni izvori ulaska u tijelo
Zeleno povrće: luk, vrhovi mlade repe, rotkvice, senf, mrkva, potočarka, kiseljak, zeleni grašak, rajčica (samo sirova), kupus, češnjak, leća, hren, krastavci. Voće i bobičasto voće: jabuke, šipak, maline, jagode, trešnje, kruške, grožđe, lubenica, bilo koje suho voće. Proizvodi životinjskog podrijetla: jetra, bubrezi, žumanjak.
Najčešće veze
Hemoglobin.
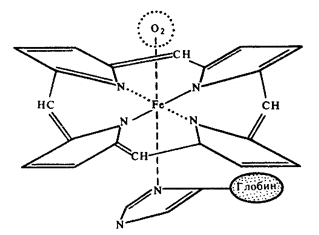
Shematski dijagram veze hem-globin u molekuli hemoglobina
Znaš li to…
O poznavanju starog čovjeka sa željezom kozmičkog porijekla svjedoči činjenica da su stanovnici Grenlanda, koji nisu imali pojma o željeznoj rudi, imali željezne proizvode. Mnogi meteoriti sastoje se od prirodnog željeza s primjesom nikla do 5,5%. Alkemičari su željezo označavali u obliku koplja i štita - karakteristične osobine boga rata Marsa. Otuda i njegovo ime od lat. fero- mač.
Broj atoma željeza u ljudskom tijelu je 4,5 x 10 22, au jednoj stanici - 4,5 x 10 8.
100 ml ljudske krvi sadrži 13-16 g hemoglobina.
Za “sastavljanje” molekule hemoglobina u ljudskom tijelu potrebno je oko 90 sekundi, a svake sekunde nastaje 650 x 10 12 molekula hemoglobina.
Mnoge žive objekte karakterizira fenomen biomagnetizma. Njihova orijentacija u magnetskom polju Zemlje provodi se uz pomoć željeznog oksida, koji se nalazi u posebnim formacijama - magnetosomima, formiranim u obliku lanaca od 10-25 kristala ukupne duljine oko 50 nm.
Za nadoknadu nedostatka željeza, u liječenju anemije, koriste se soli fero i feri željeza.
Utvrđena je korelacija između povećanog sadržaja željeza u tijelu i rani razvoj ateroskleroza, ishemijska bolest, tumori.

Željezni vitriol FeSO 4 x 7H 2 O (željezo (II) kristalni hidrat) koristi se za suzbijanje biljnih štetnika i za pripremu mineralnih boja. Željezni klorid (III) FeCl 3 koristi se kao jedkasto sredstvo za bojenje tkanina.
Cinkov

Uloga u životu biljaka, gljiva
Cink je važan mikroelement čiji je sadržaj u biljkama u prosjeku 0,003% (težinski). Aktivira 30 enzimskih sustava u stanici. Gljive (osobito otrovne), lišajevi, četinjača bogati su cinkom. U biljkama, uz sudjelovanje u disanju, metabolizmu bjelančevina i nukleika, cink regulira rast, utječe na stvaranje aminokiseline triptofana i povećava sadržaj giberelina. Cink je neophodan za razvoj jajeta i fetusa. Povećava otpornost biljaka na sušu, toplinu i hladnoću.
Njegov nedostatak dovodi do poremećaja diobe stanica (pjegavost lista u agrumima), na biljkama se stvaraju uski spiralno uvijeni listovi. Tkivo između vena postaje obezbojeno, a ističu se prozirnom zelenom mrežicom.
Višak cinka štetan je za biljke, jer. može uzrokovati deformaciju organa: u maku cvjetovi postaju dvostruki, a u yarutki latice postaju vrlo velike. U drugim biljkama moguća je kloroza lista koja se širi od vrha do baze lista. Biljke-indikatori povećanog sadržaja cinka u tlu su trobojna ljubičica, preslica, maćuhice.
Uloga u životu životinja i ljudi
Sadržaj cinka u životinjskom tijelu je približno 0,01% (težinski). Neke morske životinje beskralježnjaka, kao što su kamenice, sadrže 0,4% cinka (težinski). Dosta cinka u zmijskom otrovu (za zaštitu od djelovanja vlastitog otrova). U životinja, Zn, osim što sudjeluje u disanju i metabolizmu nukleika, povećava aktivnost spolnih žlijezda, utječe na formiranje skeleta fetusa. S nedostatkom cinka smanjuje se sadržaj RNA i smanjuje se sinteza proteina u mozgu, usporava se razvoj mozga.
S osobom od 70 kg, tijelo sadrži do 3 g cinka. Dio je najvažnijih enzima: karboanhidraze (ubrzava oslobađanje ugljičnog dioksida u plućima), raznih dehidrogenaza, fosfataza (povezanih s disanjem i drugim fiziološkim procesima), proteaza i peptidaza uključenih u metabolizam proteina, enzima nukleinskog metabolizma ( RNA i DNA polimeraze). Cink igra bitnu ulogu u sintezi mRNA molekula na odgovarajućim dijelovima DNA (transkripcija), u stabilizaciji struktura ribosoma i biopolimera (RNA, DNA, neki proteini). Cink je bitan dio enzima krvi. Neophodan je za održavanje normalnog rasta kože, kose i noktiju te zacjeljivanje rana, jer sudjeluje u sintezi proteina. Cink je dio inzulina, hormona gušterače koji regulira razinu šećera u krvi, i hormona timusa. Cink ima važnu ulogu u preradi alkohola u tijelu, pa nedostatak cinka može povećati predispoziciju za alkoholizam (osobito kod djece i adolescenata). Za bolju apsorpciju cinka u tijelu potrebni su vitamini A i B6.

Nedostatak Zn dovodi do patuljastosti, odgođenog spolnog razvoja.
Višak cinka negativno utječe na funkcije srca i krvi. Nije slučajno da je sadržaj cinka u namirnicama reguliran prema MPC: dječja i dijetalna hrana - 5,0 mg/kg; biljno ulje - 10,0 mg / kg; protein soje - 60,0 mg / kg.
U stanicama i pojedinim organima tijekom njihove maligne transformacije povećava se sadržaj određenih metalnih iona. Koncentracija cinka se povećava nekoliko puta. Razlozi još nisu poznati, ali se nagađa da bi to moglo poslužiti rana dijagnoza Rak.
Cink se iz tijela izlučuje urinom, izmetom, znojem.

Glavni izvori ulaska u tijelo
Proizvodi od povrća: povrće, kukuruz, orašasti plodovi, pekarski proizvodi. Gljive. Proizvodi životinjskog podrijetla: govedina, jetra, meso, mlijeko; plodovi mora (kamenice, školjke, haringa).
Najčešće veze
ZnS- cink sulfid, cink blende.
ZnSO 4 x 7H 2 O- cink hidrosulfat, cink vitriol.
ZnCl 2- cink klorid.
Znaš li to...
Vjeruje se da su rude cinka ljudima poznate od davnina. U II stoljeću pr. Grci su već znali topiti mjed – leguru cinka i bakra. u Indiji u 12. stoljeću. postojala je proizvodnja metalnog cinka, ali se u Europi pojavila mnogo kasnije. Saksonski metalurg I. Genkel opisao je cink kao metal, a 1746. godine njemački kemičar A. Marggraf razvio je metode za dobivanje cinka iz minerala kalamina i sfalerita ZnS (cinkova mješavina). Ime dolazi od njega. cinkov- bijeli metal.
Broj atoma cinka u ljudskom tijelu je 2,2 x 10 22, au jednoj stanici - 2,2 x 10 8.
Dnevni unos cinka u organizam hranom iznosi 13 mg.
Postoji više od 200 enzima koji sadrže cink.
Suspenzija, koja uključuje inzulin, protamin i cink klorid, učinkovit je antidijabetički agens koji djeluje bolje od čistog inzulina.
U suvremenoj medicini spojevi cinka se koriste u liječenju raznih imunodeficijencija, neplodnosti, bolesti kože, kose, noktiju i jetre. U obliku otopine, cink klorid ZnCl 2 koristi se kao sredstvo za kauterizaciju, cinkova mast ZnO kao sredstvo za sušenje, adstringens i dezinficijens za kožne bolesti, cink vitriol ZnSO 4 x 7H 2 O je dio kapi za oči.
Spojevi cinka doprinose prevenciji prehlade kod djece, poboljšavaju apetit, rast, razvoj, povećavaju koncentraciju.
Nastavit će se
Sve je počelo fotosintezom. Zanimljivo je primijetiti da su se važnost magnezija za naš organizam i posljedice njegovog nedostatka počeli procjenjivati u isto vrijeme kada su otkrivene tajne fotosinteze biljaka – prije samo nekoliko desetljeća.
Proces kontinuiranog stvaranja organske tvari započeo je prije više milijardi godina, kada su se na Zemlji pojavili pigmenti koji su upijajući sunčevu svjetlost uzrokovali kemijske reakcije. Odlučujuću ulogu u tome imale su "fotoosjetljive" tvari iz skupine nastalih od jednostavnih spojeva - i glicerola. Međutim, tek pojavom magnezijevog derivata porfirina u obliku klorofila prirodna povijest viši oblici organskog života. Klorofil ima sposobnost provesti nepovratnu fotokemijsku reakciju čija se energija akumulira u stabilnim biokemijskim spojevima.
Proces fotosinteze nastao je, vjerojatno, na kraju pretkambrija (prije oko 1000 milijuna godina). Struktura klorofila vrlo je bliska strukturi hema, glavne komponente krvnog pigmenta. Razlika je u tome što klorofil sadrži magnezij (magnezijev ion), a hem, hemoglobin - (ion željeza). Ovo otkriće profesora Jagelonskog sveučilišta Leona Marklevskog potvrdilo je vezu između evolucije flore i faune.
Možemo reći da se i čovjeku događa isto, iako je... sve je puno kompliciranije. Čovjek ne može biti zdrav ako u hrani nema dovoljno magnezija. Do ovog su zaključka došli sudionici prvog Kongresa o bolestima uzrokovanim nedostatkom magnezija. Kongres je održan u svibnju 1971. u Vittelu. Magnezijev ion ima posebnu ulogu u gotovo svim procesima koji se odvijaju u tijelu. Dakle, u imunološkim procesima djeluje antistresno, antitoksično, antialergijsko, antianafilaktično (vrsta osjetljivosti), protuupalno, štiti od ionizirajućeg zračenja, regulira temperaturu, potiče i sudjeluje u stvaranju antitijela. Magnezij djeluje opuštajuće i smanjuje osjetljivost tijela. Tada je, na kongresu u Vittelu, profesor Dürlach rekao: "Znak modernog civiliziranog svijeta je sve niža razina magnezijevog iona."
Čini se da su civilizacijske bolesti velikim dijelom uzrokovane nedostatkom magnezija u ljudskom tijelu. Stoga je vrijedno pobliže pogledati magnezij.
Magnezij dobivamo iz tla – putem biljne hrane i hrane dobivene od životinja koje se hrane biljkama. Dakle, u naše tijelo ulazi onoliko magnezija koliko ga ima u tlu.
U međuvremenu, u tlu je malo magnezija. Nedostatak magnezija zabilježen je u 40% poljskih zemalja, prosječan sadržaj u 34% zemalja, a dovoljan ili visok sadržaj u manje od 26%. Umjetna gnojiva ili uopće ne obogaćuju tlo magnezijem, ili ga ono prima premalo. Primjerice, 1971.-1975. Prosječna količina magnezija dodanog poljskom zemljištu bila je 10-12 kg magnezijevog oksida (MgO) po 1 ha obrađene zemlje. Je li to puno ili malo? Pšenica s prinosom od 40 q/ha trebala bi dobiti iz tla oko 17 kg s 1 ha MgO, a šećerna repa s prinosom od samo 350 q/ha - oko 66 kg.
Naravno, potrebna količina magnezijskog gnojiva ovisi o sadržaju magnezija u tlu i vrsti usjeva koji se uzgaja. Obično je to od 130 do 260 kg/ha. Od ove količine kieserita (magnezijevog gnojiva) u tlo prelazi 30-60 kg magnezijevog oksida i uz to 15-31 kg kalijevog oksida. Stajnjak sadrži 0,18% magnezija, što znači da ako na 1 ha unesemo 300 kg stajskog gnoja, dobijemo oko 54 kg Mg. Ovo definitivno nije dovoljno.
Klorofil sadrži 2,7% magnezija. Ioni magnezija reguliraju stupanj hidratacije stanica. Uz nedostatak magnezija u biljkama, proces isparavanja vode je ograničen, a s viškom, biljka intenzivno upija vodu, tako da se tlo suši unutar korijenskog sustava.
Za zainteresirane, evo tablice.
Mineralni elementi.doc
Minerali1. Uloga mineralnih elemenata u ljudskom tijelu 1
2. Makronutrijenti, njihove karakteristike
3. Elementi u tragovima, njihove karakteristike
4. Utjecaj tehnološke obrade
O mineralnom sastavu prehrambenih proizvoda
5. Metode za određivanje mineralnih tvari
1. Uloga mineralnih elemenata u ljudskom tijelu
Mnogi elementi u obliku mineralnih soli, iona, složenih spojeva i organska tvar dio su žive tvari i bitne su hranjive tvari koje se moraju svakodnevno unositi hranom. Sadržaj minerala u glavnim namirnicama dat je u tablici. 5.1.
Prema preporuci Dijetetskog odbora Nacionalna akademija SAD, dnevni unos kemijskih elemenata hranom trebao bi biti na određenoj razini (tablica 5.2). Isti broj kemijskih elemenata mora se dnevno izlučivati iz tijela, budući da je njihov sadržaj u njemu relativno konstantan.
Uloga minerala u ljudskom tijelu iznimno je raznolika, unatoč tome što nisu bitna komponenta prehrane. Mineralne tvari sadržane su u protoplazmi i biološkim tekućinama, igraju veliku ulogu u osiguravanju postojanosti osmotskog tlaka, što je neophodan uvjet za normalno funkcioniranje stanica i tkiva. Dio su složenih organskih spojeva (npr. hemoglobin, hormoni, enzimi), plastični su materijal za izgradnju koštanog i zubnog tkiva. U obliku iona, mineralne tvari sudjeluju u prijenosu živčanih impulsa, osiguravaju zgrušavanje krvi i druge fiziološke procese u tijelu.
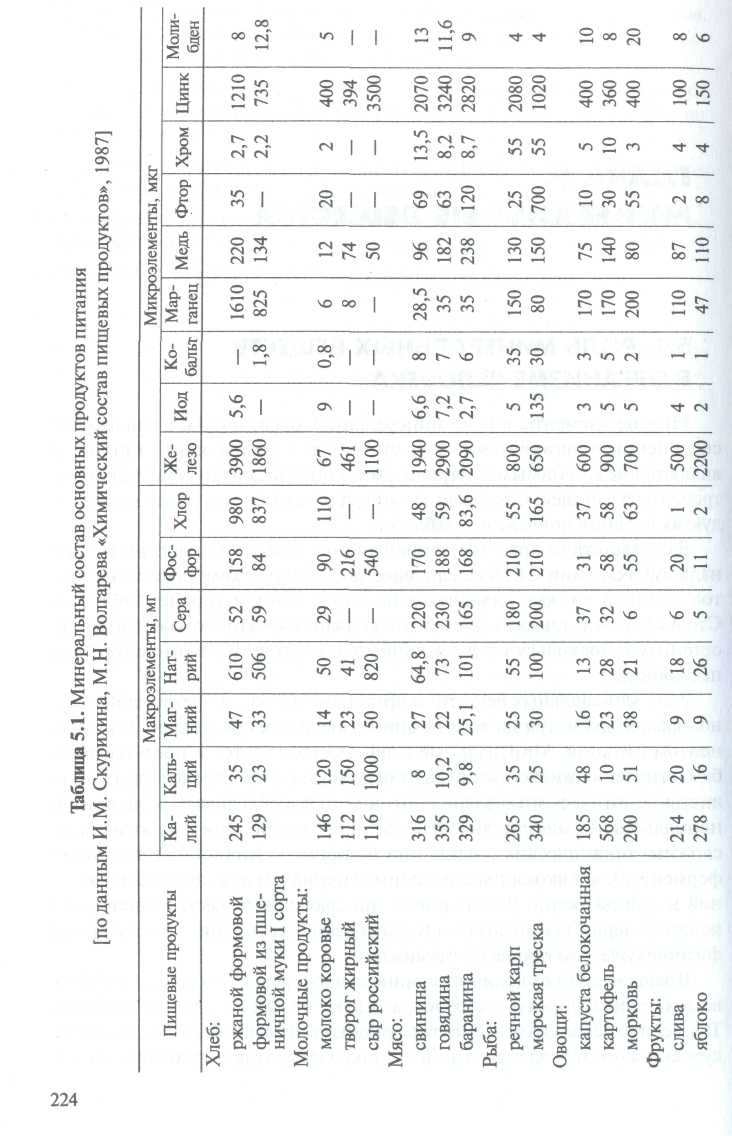 |
Ovisno o količini minerala u ljudskom tijelu i prehrambenim proizvodima, dijele se na makro- i elementi u tragovima. Dakle, ako maseni udio elementa u tijelu prelazi 10 -2%, onda ga treba smatrati makroelementom. Udio elemenata u tragovima u tijelu je 10 -3 -10 -5%. Ako je sadržaj elementa ispod 10 -5%, smatra se ultramikroelementom. Makronutrijenti uključuju kalij, natrij, kalcij, magnezij, fosfor, klor i sumpor. Sadrže se u količinama koje se mjere u stotinama i desecima miligrama na 100 g tkiva ili hrane. Elementi u tragovima dio su tkiva tijela u koncentracijama izraženim u desetinkama, stotinkama i tisućinkama miligrama i neophodni su za njegovo normalno funkcioniranje. Elementi u tragovima se uvjetno dijele u dvije skupine: apsolutno ili vitalne (kobalt, željezo, bakar, cink, mangan, jod, brom, fluor) i tzv. vjerojatno potrebne (aluminij, stroncij, molibden, selen, nikal, vanadij i neke druge ). Elementi u tragovima nazivaju se vitalnim ako je u njihovoj odsutnosti ili nedostatku normalno funkcioniranje tijela poremećeno.
Raspodjela elemenata u tragovima u tijelu ovisi o njihovoj kemijska svojstva i vrlo raznolika. Željezo je, na primjer, sastavni dio hemoglobina, mioglobina i drugih dišnih pigmenata, odnosno tvari koje sudjeluju u apsorpciji i transportu kisika do svih tkiva u tijelu; atomi bakra uključeni su u aktivno središte brojnih enzima itd.
Djelovanje mikroelemenata može biti i neizravno – kroz utjecaj na intenzitet ili prirodu metabolizma. Dakle, neki mikroelementi (npr. mangan, cink, jod) utječu na rast, a njihov nedovoljan unos hranom inhibira normalno tjelesnog razvoja dijete. Ostali elementi u tragovima (na primjer, molibden, bakar, mangan) uključeni su u reproduktivnu funkciju, a njihov nedostatak u tijelu negativno utječe na ovu stranu ljudskog života.
Najdeficitarnijim mineralima u prehrani modernog čovjeka uključuju kalcij i željezo, višak - natrij i fosfor.
Nedostatak ili višak u prehrani bilo koje mineralne tvari uzrokuje kršenje metabolizma proteina, masti, ugljikohidrata, vitamina, što dovodi do razvoja niza bolesti. Ispod su karakteristični (tipični) simptomi manjka raznih kemijskih elemenata u ljudskom tijelu: Najčešća posljedica neusklađenosti količine kalcija i fosfora u prehrani je zubni karijes, stanjivanje kostiju. Nedostatak fluora u vodi za piće uništava se zubna caklina, nedostatak joda u hrani i vodi dovodi do bolesti štitnjače. Dakle, minerali su vrlo važni za eliminaciju i prevenciju niza bolesti.


Navodimo uzroke metaboličkih poremećaja mineralnih tvari koji se mogu javiti i uz njihovu dovoljnu količinu u hrani:
A) neuravnotežena prehrana (nedovoljne ili prekomjerne količine bjelančevina, masti, ugljikohidrata, vitamina itd.);
B) korištenje metoda kulinarske obrade hrane, koje uzrokuju gubitak minerala, na primjer, tijekom odmrzavanja (u Vruća voda) meso, riba ili kod uklanjanja dekocija od povrća i voća, gdje prolaze topljive soli;
C) nedostatak pravovremene korekcije sastava prehrane kada se tjelesna potreba za mineralima povezana s fiziološkim razlozima mijenja. Na primjer, ljudi koji rade u uvjetima povišena temperatura vanjsko okruženje povećava se potreba za kalijem, natrijem, klorom i drugim mineralima zbog činjenice da se većina njih izlučuje iz tijela znojem;
D) kršenje procesa apsorpcije minerala u gastrointestinalnom traktu ili povećan gubitak tekućine (na primjer, gubitak krvi).
^
2. Makronutrijenti, njihove karakteristike
Kalcij. Glavna je strukturna komponenta kostiju i zuba; dio je jezgri stanica, staničnih i tkivnih tekućina, neophodan je za zgrušavanje krvi. Kalcij tvori spojeve s proteinima, fosfolipidima, organskim kiselinama; sudjeluje u regulaciji propusnosti staničnih membrana, u prijenosu živčanih impulsa, u molekularnom mehanizmu mišićnih kontrakcija, kontrolira aktivnost niza enzima. Dakle, kalcij obavlja ne samo plastične funkcije, već utječe i na mnoge biokemijske i fiziološke procese u tijelu.
Kalcij je teško probavljiv element. Spojevi kalcija koji ulaze u ljudsko tijelo s hranom praktički su netopivi u vodi. Alkalna okolina tankog crijeva potiče stvaranje neprobavljivih spojeva kalcija, a samo djelovanje žučnih kiselina osigurava njegovu apsorpciju.
Asimilacija kalcija u tkivima ne ovisi samo o njegovom sadržaju u hrani, već io njegovom omjeru s ostalim sastojcima hrane i prije svega s mastima, magnezijem, fosforom i bjelančevinama. Uz višak masnoće dolazi do konkurencije žučnim kiselinama i znatan dio kalcija se izlučuje iz organizma kroz debelo crijevo. Na apsorpciju kalcija negativno utječe višak magnezija; preporučeni omjer ovih elemenata je 1:0,5. Ako količina fosfora premašuje razinu kalcija u hrani za više od 2 puta, tada nastaju topljive soli koje se krvlju izvlače iz koštanog tkiva. Kalcij ulazi u stijenke krvnih žila, što uzrokuje njihovu krhkost, kao i u tkiva bubrega, što može doprinijeti nastanku bubrežnih kamenaca. Za odrasle je preporučeni omjer kalcija i fosfora u hrani 1:1,5. Poteškoće u održavanju ovog omjera nastaju zbog činjenice da je najčešće konzumirana hrana puno bogatija fosforom nego kalcijem. Fitin i oksalna kiselina, sadržani u brojnim biljnim proizvodima, negativno utječu na apsorpciju kalcija. Ovi spojevi tvore netopive soli s kalcijem.
Dnevna potreba za kalcijem kod odrasle osobe je 800 mg, a kod djece i adolescenata - 1000 mg ili više.
S nedovoljnim unosom kalcija ili kršenjem njegove apsorpcije u tijelu (s nedostatkom vitamina D), razvija se stanje nedostatka kalcija. Dolazi do pojačanog izlučivanja iz kostiju i zuba. U odraslih se razvija osteoporoza - demineralizacija koštanog tkiva, kod djece je poremećeno formiranje kostura, razvija se rahitis.
Najbolji izvori kalcija su mlijeko i mliječni proizvodi, razni sirevi i svježi sir (100-1000 mg/100 g proizvoda), zeleni luk, peršin, grah. Značajno manje kalcija nalazi se u jajima, mesu, ribi, povrću, voću, bobičastom voću (20-40 mg / 100 g proizvoda).
Magnezij. Ovaj element je potreban za djelovanje niza ključnih enzima. za tjelesni metabolizam. Magnezij je uključen u održavanje normalne funkcije živčanog sustava i srčanih mišića; ima vazodilatacijski učinak; potiče izlučivanje žuči; podiže motorička aktivnost crijeva, što pomaže u uklanjanju toksina iz tijela (uključujući kolesterol).
Apsorpciju magnezija ometa prisutnost fitina te višak masnoće i kalcija u hrani. Dnevne potrebe za magnezijem nisu precizno definirane; vjeruje se, međutim, da doza od 200-300 mg / dan sprječava pojavu nedostatka (pretpostavlja se da se apsorbira oko 30% magnezija).
S nedostatkom magnezija, apsorpcija hrane je poremećena, rast je odgođen, kalcij se taloži u stijenkama krvnih žila, a razvijaju se i brojne druge patološke pojave. Kod ljudi je nedostatak magnezijevih iona, zbog prirode prehrane, krajnje malo vjerojatan. Međutim, kod proljeva može doći do velikih gubitaka ovog elementa; njihove se posljedice osjećaju ako se u organizam unose tekućine koje ne sadrže magnezij. Kada koncentracija magnezija u serumu padne na oko 0,1 mmol/l, može se javiti sindrom nalik delirium tremens: osoba ima polukomatozno stanje, drhtanje mišića, grčeve mišića u zapešću i stopalu, povećanu neuromuskularnu ekscitabilnost kao odgovor na zvuk, mehanički i vizualni podražaji. Uvođenje magnezija uzrokuje brzo poboljšanje stanja.
Magnezijem je bogata uglavnom biljna hrana. Velika količina sadrži pšenične mekinje, razne žitarice (40 - 200 mg / 100 g proizvoda), mahunarke, marelice, suhe marelice, suhe šljive. Malo magnezija ima u mliječnim proizvodima, mesu, ribi, tjestenini, većini povrća i voća (20 - 40 mg / 100 g).
Kalij. Oko 90% kalija nalazi se unutar stanica. On, zajedno s drugim solima, osigurava osmotski tlak; sudjeluje u prijenosu živčanih impulsa; regulacija metabolizma vode i soli; potiče uklanjanje vode, a time i toksina iz tijela; održava kiselo-baznu ravnotežu unutarnjeg okoliša tijela; sudjeluje u regulaciji aktivnosti srca i drugih organa; neophodna za funkcioniranje niza enzima.
Kalij se dobro apsorbira iz crijeva, a njegov višak se brzo uklanja iz tijela urinom. Dnevna potreba za kalijem kod odrasle osobe je 2000-4000 mg. Povećava se kod obilnog znojenja, uz korištenje diuretika, bolesti srca i jetre. Kalij nije manjkav nutrijent u prehrani, a uz raznovrsnu prehranu ne dolazi do manjka kalija. Nedostatak kalija u tijelu nastaje kada je poremećena funkcija živčano-mišićnog i kardiovaskularnog sustava, pospanost, sniženje krvnog tlaka i srčane aritmije. U takvim slučajevima propisana je dijeta s kalijem.
Većina kalija dolazi iz biljne hrane. Njegovi bogati izvori su marelice, suhe šljive, grožđice, špinat, morske alge, grah, grašak, krumpir, ostalo povrće i voće (100 - 600 mg / 100 g proizvoda). Manje kalija ima u kiselom vrhnju, riži, kruhu od vrhunskog brašna (100 - 200 mg / 100 g).
Natrij. Natrij se nalazi u svim tkivima i tjelesnim tekućinama. On je uključen u održavanje osmotskog tlaka u tkivnim tekućinama i krvi; u prijenosu živčanih impulsa; regulacija acidobazne ravnoteže, metabolizma vode i soli; povećava aktivnost probavnih enzima.
Metabolizam natrija je opsežno proučavan zbog njegovih fizioloških svojstava i važnosti za tijelo. Ovaj nutrijent se lako apsorbira iz crijeva. Natrijevi ioni uzrokuju oticanje koloida tkiva, što uzrokuje zadržavanje vode u tijelu i sprječava njezino oslobađanje. Ukupna količina natrija u izvanstaničnoj tekućini tako određuje volumen tih tekućina. Povećanje koncentracije natrija u plazmi dovodi do osjećaja žeđi. U vrućoj klimi i tijekom teškog fizičkog rada dolazi do značajnog gubitka natrija uz znoj te je potrebno unositi sol u organizam kako bi se nadoknadilo izgubljeno.
Uglavnom, natrijevi ioni ulaze u tijelo na račun kuhinjske soli – NaCl. Prekomjernom konzumacijom natrijevog klorida pogoršava se uklanjanje krajnjih produkata metabolizma topljivih u vodi kroz bubrege, kožu i druge organe za izlučivanje. Zadržavanje vode u tijelu otežava aktivnost kardiovaskularnog sustava, povećava krvni tlak. Stoga je konzumacija soli kod relevantnih bolesti u prehrani ograničena. Međutim, pri radu u vrućim trgovinama ili vrućoj klimi povećava se količina natrija (u obliku kuhinjske soli) unesenog izvana kako bi se nadoknadio njegov gubitak znojem i smanjilo znojenje koje opterećuje rad srca.
Natrij je prirodno prisutan u svim namirnicama. Način dobivanja prehrambenih proizvoda uvelike određuje konačni sadržaj natrija u njemu. Na primjer, smrznuti zeleni grašak sadrži mnogo više natrija od svježeg. Svježe povrće i voće sadrže manje od 10 mg/kg do 1 g/kg, za razliku od žitarica i sira koji mogu sadržavati natrij u količinama od 10-20 g/kg.
Procjena prosječnog dnevnog unosa natrija iz hrane je teška jer koncentracija natrija u hrani uvelike varira, a osim toga, ljudi su navikli dodavati sol u hranu. Odrasla osoba dnevno unese do 15 g kuhinjske soli, a istu količinu izluči iz organizma. Ova količina je mnogo veća od fiziološki potrebne a određuje ga prvenstveno okus natrijevog klorida, navika slane hrane. Sadržaj kuhinjske soli u ljudskoj hrani može se smanjiti na 5 g dnevno bez štete po zdravlje. Na oslobađanje natrijevog klorida iz tijela, a time i na potrebu za njim, utječe količina kalijevih soli koje tijelo prima. Biljna hrana, posebice krumpir, bogata je kalijem i povećava izlučivanje natrijevog klorida u mokraći, a samim time i povećava potrebu za njim.
Fosfor. Fosfor se nalazi u svim tkivima tijela, posebno u mišićima i mozgu. Ovaj element je uključen u sve životne procese tijela. : sinteza i razgradnja tvari u stanicama; regulacija metabolizma; dio je nukleinskih kiselina i niza enzima; potrebno za stvaranje ATP-a.
Fosfor se nalazi u tjelesnim tkivima i prehrambenim proizvodima u obliku fosforne kiseline i njezinih organskih spojeva (fosfata). Njegova glavna masa je u koštanom tkivu u obliku kalcijevog fosfata, ostatak fosfora je dio mekih tkiva i tekućina. U mišićima dolazi do najintenzivnije izmjene fosfornih spojeva. Fosforna kiselina sudjeluje u izgradnji molekula mnogih enzima, nukleinskih kiselina itd.
Uz dugotrajan nedostatak fosfora u prehrani, tijelo koristi vlastiti fosfor iz koštanog tkiva. To dovodi do demineralizacije kostiju i kršenja njihove strukture - razrjeđivanja. Kada je tijelo iscrpljeno fosforom, mentalna i tjelesna učinkovitost se smanjuje, bilježi se gubitak apetita, apatija.
Dnevna potreba za fosforom za odrasle je 1200 mg. Povećava se kod velikog fizičkog ili psihičkog stresa, kod određenih bolesti.
Velika količina fosfora se nalazi u proizvodima životinjskog podrijetla, osobito u jetri, kavijaru, kao i u žitaricama i mahunarkama. Njegov sadržaj u ovim proizvodima kreće se od 100 do 500 mg na 100 g proizvoda. Bogat izvor fosfora su žitarice (zobene pahuljice, biserni ječam), sadrže 300-350 mg fosfora / 100 g. Međutim, spojevi fosfora se apsorbiraju iz biljnih proizvoda lošije nego kada jedu hranu životinjskog podrijetla.
Sumpor. Važnost ovog elementa u prehrani određena je, prije svega, činjenicom da je dio proteina u obliku aminokiselina koje sadrže sumpor. (metionin i cistin), a također je sastavni dio nekih hormona i vitamina.
Kao sastavni dio aminokiselina koje sadrže sumpor, sumpor je uključen u procese metabolizma proteina, a potreba za njim dramatično raste tijekom trudnoće i rasta tijela, praćena aktivnim uključivanjem proteina u nastala tkiva, kao i tijekom upalnih procesa. procesa. Aminokiseline koje sadrže sumpor, osobito u kombinaciji s vitaminima C i E, imaju izražen antioksidativni učinak. Uz cink i silicij, sumpor određuje funkcionalno stanje kose i kože.
Klor. Ovaj element sudjeluje u stvaranju želučanog soka, formiranju plazme, aktivira niz enzima. Ova se hranjiva tvar lako apsorbira iz crijeva u krv. Zanimljiva je sposobnost klora da se taloži u koži, da se prekomjernim unosom zadržava u tijelu, te da se u značajnim količinama izlučuje znojem. Izlučivanje klora iz tijela događa se uglavnom mokraćom (90%) i znojem.
Povrede u razmjeni klora dovode do razvoja edema, nedovoljnog izlučivanja želučanog soka itd. Oštar pad sadržaja klora u tijelu može dovesti do ozbiljnog stanja, čak i smrti. Povećanje njegove koncentracije u krvi javlja se s dehidracijom tijela, kao i s kršenjem funkcije izlučivanja bubrega.
Dnevna potreba za klorom je približno 5000 mg. Klor ulazi u ljudsko tijelo uglavnom u obliku natrijevog klorida kada se doda hrani.
^
3. Elementi u tragovima, njihove karakteristike
Željezo. Ovaj element je neophodan za biosintezu spojeva koji osiguravaju disanje, hematopoezu; sudjeluje u imunobiološkim i redoks reakcijama; dio je citoplazme, staničnih jezgri i brojnih enzima.
Asimilaciju željeza sprječavaju oksalna kiselina i fitin. Za asimilaciju ove hranjive tvari potreban je vitamin B 12. Askorbinska kiselina također doprinosi apsorpciji željeza, budući da se željezo apsorbira u obliku dvovalentnog iona.
^ Nedostatak željeza u tijelu može dovesti do razvoja anemije, razmjene plinova, staničnog disanja, odnosno poremećeni su temeljni procesi koji osiguravaju život. Razvoj stanja nedostatka željeza olakšava: nedovoljan unos željeza u tijelo u asimiliranom obliku, smanjenje sekretorne aktivnosti želuca, nedostatak vitamina (osobito B 12 , folna i askorbinska kiselina) i niz bolesti koje uzrokuju gubitak krvi.
Potrebe za željezom odrasle osobe (14 mg/dan) suvišno su zadovoljene normalnom prehranom. Međutim, kada se u ishrani koristi kruh od finog brašna koji sadrži malo željeza, kod gradskih stanovnika vrlo se često opaža nedostatak željeza. Istodobno, treba uzeti u obzir da proizvodi od žitarica bogati fosfatima i fitinom tvore teško topive spojeve sa željezom i smanjuju njegovu asimilaciju u tijelu.
Željezo je rasprostranjen element. Nalazi se u iznutricama, mesu, jajima, grahu, povrću, bobičastom voću. Međutim, u lako probavljivom obliku, željezo se nalazi samo u mesnim proizvodima, jetri (do 2000 mg / 100 g proizvoda), žumanjku.
Bakar. Bakar je bitan element u ljudskom metabolizmu, igra ulogu u stvaranju crvenih krvnih stanica, oslobađanju željeza iz tkiva i razvoju kostura, središnjeg živčanog sustava i vezivnog tkiva.
Budući da je bakar široko rasprostranjen u hrani, malo je vjerojatno da će ljudi, s mogućim izuzetkom dojenčadi, na isključivo mliječnoj prehrani, ikada razviti oblik pothranjenosti povezane s bakrom.
Konzumacija pretjerano velikih doza bakra od strane osobe dovodi do iritacije i erozije sluznice, širokog oštećenja kapilara, oštećenja jetre i bubrega te iritacije središnjeg živčanog sustava. Dnevna potreba za ovim elementom je oko 2 mg. Izvori bakra su namirnice kao što su jetra, žumanjak, zeleno povrće.
Jod. Jod je esencijalni element uključen u stvaranje hormona tiroksina. S nedostatkom joda razvija se gušavost - bolest štitnjače.
Potreba za jodom kreće se od 100-150 mcg dnevno. Sadržaj joda u namirnicama obično je nizak (4-15 µg%). Plodovi mora su najbogatiji jodom. Dakle, u morskoj ribi sadrži oko 50 mcg / 100 g, u jetri bakalara do 800, u morskim algama, ovisno o vrsti i vremenu sakupljanja - od 50 mcg do 70 000 mcg / 100 g proizvoda. Ali mora se uzeti u obzir da se tijekom dugotrajnog skladištenja i toplinske obrade hrane gubi značajan dio joda (od 20 do 60%).
Sadržaj joda u kopnenim biljnim i životinjskim proizvodima uvelike ovisi o njegovoj količini u tlu. U područjima gdje ima malo joda u tlu, njegov sadržaj u prehrambenim proizvodima može biti 10 do 100 puta manji od prosjeka. Stoga na ovim prostorima za prevenciju gušavosti kuhinjskoj soli se dodaje mala količina kalijevog jodata (25 mg na 1 kg soli). Rok trajanja takve jodirane soli nije duži od 6 mjeseci, budući da jod postupno nestaje tijekom skladištenja soli.
Fluor. S nedostatkom ovog elementa razvija se zubni karijes (uništenje zubne cakline). Višak fluora također negativno utječe na tijelo, jer soli fluora, nakupljajući se u kostima, uzrokuju promjenu boje i oblika zuba, osteohondrozu, a nakon toga grubost zglobova i njihova nepokretnost koštane izrasline. Razlika između korisnih i štetnih doza fluora toliko je mala da se mnogi istraživači protive fluoriranju vode.
Fluor koji se konzumira s vodom gotovo se potpuno apsorbira, a fluor sadržan u hrani apsorbira se u manjoj mjeri. Apsorbirani fluor je ravnomjerno raspoređen po cijelom tijelu. Zadržava se uglavnom u kosturu, a mala količina se taloži u zubnom tkivu. U visokim dozama, fluor može uzrokovati kršenje metabolizma ugljikohidrata, lipida, proteina, kao i metabolizam vitamina, enzima i mineralnih soli.
Procjene dnevnog unosa fluora iz hrane napravljene su u raznim zemljama; za odrasle, ova vrijednost varira od 0,2 do 3,1 mg, za djecu dobna skupina od 1 do 3 godine, unos fluorida procijenjen je na 0,5 mg/dan.
Gotovo svi prehrambeni proizvodi sadrže najmanje količine ovog elementa u tragovima. Sve vrste vegetacije sadrže određenu količinu fluora koji dobivaju iz tla i vode. Visoke razine fluorida pronađene su u određenim namirnicama, osobito ribi, nekom povrću i čaju. Upotreba fluorirane vode u postrojenjima za preradu hrane često može udvostručiti razinu fluora u gotovim proizvodima.
Za prevenciju i liječenje karijesa, razne paste za zube, puderi, eliksiri, žvakaće gume i slično, koji sadrže dodan fluor, uglavnom u anorganskom obliku. Ovi spojevi se obično ugrađuju u paste za zube, obično u koncentracijama od oko 1 g/kg.
Krom. Čini se da je ovaj element bitan za metabolizam glukoze i lipida te za korištenje aminokiselina u nekim sustavima. On također ima važnost za prevenciju blagih oblika dijabetesa i ateroskleroze u ljudi.
Krom se apsorbira i iz gastrointestinalnog trakta i iz respiratornog trakta. Apsorbirana količina nije ista za svaki od ovih sustava i ovisi o obliku kroma. Trovalentni krom je esencijalni oblik elementa za ljude, heksavalentni krom je otrovan. Krom se distribuira po tkivima ljudskog tijela u nejednakim, ali obično niskim koncentracijama. Razina kroma u svim tkivima osim u plućima smanjuje se s godinama. Najveće količine kroma kod ljudi se nakupljaju u koži, mišićima i masnom tkivu. Homeostatski mehanizmi, uključujući mehanizme transporta u jetri i crijevima, sprječavaju prekomjerno nakupljanje trovalentnog kroma. Krom se polako izlučuje iz tijela, uglavnom mokraćom.
Danas se smatra normom konzumacije oko 150 mg kroma dnevno. Posebno je koristan za starije osobe čije tijelo slabo apsorbira ugljikohidrate, a krom pospješuje metaboličke procese tih spojeva. Anorganski krom se slabo, puno lakše apsorbira - u organskim spojevima, odnosno u obliku u kojem se nalazi u živim organizmima.
Prehrambeni proizvodi značajno variraju u razinama kroma, koje se kreću od 20 do 550 µg/kg. Bogati izvori kroma su pivski kvasac, jetra (10-80 mcg/100 g). U manjim količinama ovaj element ima u krumpiru s ljuskom, govedini, svježem povrću, integralnom kruhu, siru.
Mangan. Mangan je neophodan kao kofaktor u brojnim enzimskim sustavima; igra ulogu u pravilnom funkcioniranju flavoproteina, u sintezi sulfatiranih mukopolisaharida, kolesterola, hemoglobina i u mnogim drugim metaboličkim procesima. Od unesenog mangana apsorbira se samo oko 3%.
Apsorpcija mangana usko je povezana s apsorpcijom željeza. Potreba za manganom je 0,2-0,3 mg na 1 kg ljudske težine dnevno. Najviše mangana ima u brusnicama i čaju, nešto manje u kestenima, kakau, povrću, voću (100-200 mcg/100 g).
^ Nikal. Nikal je relativno nedavno prepoznat kao esencijalni element u tragovima. Trenutno je utvrđena njegova uloga kao koenzima u procesima metabolizma željeza. Istodobno, povećanje unosa željeza u tijelo popraćeno je povećanjem potrebe za prehrambenim niklom. Osim toga, nikal doprinosi apsorpciji bakra - još jednog elementa neophodnog za hematopoezu. Važnost prehrambenog nikla ili nikla izoliranog iz prirodnih proizvoda naglašena je činjenicom da su sintetski spojevi ovog elementa kancerogeni.
Nikal je prisutan u većini namirnica, ali u koncentracijama ispod (a često i znatno ispod) 1 mg/kg. Prijavljeno je da se prehrambeni unos nikla kreće od manje od 200 do 900 µg/dan. Uz normalnu prehranu dolazi oko 400 mcg / dan. Pokazalo se da je udio nikla u vinima 100 odnosno 50 µg/L u pivu.
Cinkov. Ovaj element u tragovima kao koenzim sudjeluje u širokom spektru reakcija biosinteze proteina (više od 70) i metabolizma nukleinskih kiselina (uključujući procese replikacije i transkripcije DNA), koje prvenstveno osiguravaju rast i pubertet tijela. Istovremeno, cink je, uz mangan, specifičan element u tragovima koji utječe na stanje spolne funkcije, odnosno na aktivnost nekih spolnih hormona, spermatogenezu, razvoj muških spolnih žlijezda i sekundarne spolne karakteristike. Osim toga, nedavno se razmatra uloga cinka u prevenciji hipertrofičnih procesa u prostati.
Cink, zajedno sa sumporom, sudjeluje u rastu i obnovi kože i kose. Uz mangan i bakar, cink značajno pridonosi percepciji osjeta okusa i mirisa. Cink kao neizostavan sastojak dio je molekule inzulina, a njegova je razina smanjena u bolesnika sa šećernom bolešću. Vrlo je važno da je ovaj element u tragovima koenzim alkohol dehidrogenaze, koji osigurava metabolizam etilnog alkohola. Istodobno, razina apsorpcije cinka kod kroničnog alkoholizma naglo je smanjena. Takozvano "noćno sljepilo" (tj. oštećenje noćnog vida) može se razviti ne samo u nedostatku vitamina A, već i cinka. Cink, zajedno s vitaminom B 6, osigurava metabolizam nezasićenih masnih kiselina i sintezu prostaglandina.
Cink je vrlo važan za probavu i apsorpciju hranjivih tvari. Dakle, cink osigurava sintezu najvažnijih probavnih enzima u gušterači, a također sudjeluje u stvaranju hilomikrona - transportnih čestica, u kojima se prehrambene masti mogu apsorbirati u krv. Cink je, uz vitamine B, važan regulator funkcija živčanog sustava. U uvjetima manjka cinka mogu nastati emocionalni poremećaji, emocionalna nestabilnost, razdražljivost, au vrlo teškim slučajevima i disfunkcija malog mozga. Konačno, skuplja se sve više podataka u prilog sudjelovanju cinka u procesima sazrijevanja limfocita i reakcijama stanične imunosti.
Dnevna potreba za cinkom je 8000-22000 mcg%. Sasvim je zadovoljna uobičajenom prehranom. Prosječan dnevni unos cinka samo s pitkom vodom je oko 400 mcg. Sadržaj cinka u prehrambenim proizvodima obično se kreće od 150-25000 mcg%. Međutim, u jetri, mesu i mahunarkama doseže 3000 - 5000 mcg%. Ponekad, nedostatak cinka može iskusiti organizam djece i adolescenata koji ne konzumiraju dovoljno životinjskih proizvoda.
^ Selen. Čak i sredinom XX. stoljeća. selen ne samo da nije uzet u obzir od strane nutricionističke znanosti, već se čak smatrao vrlo otrovnim elementom s kancerogenim svojstvima. Međutim, već 60-ih godina. ustanovljeno je da s nedostatkom selena, kardiovaskularni sustav pati, što se očituje progresivnom aterosklerozom i slabošću srčanog mišića, a u stanjima kroničnog manjka selena može se razviti gotovo neizlječiva kardiomiopatija. U posljednje vrijeme na razini suvremena istraživanja nalazi potvrdu jednog od važnih zapažanja drevne kineske medicine, što ukazuje na to odgovarajuća opskrba tijela selenom pomaže u usporavanju procesa starenja i vodi do dugovječnosti . Zanimljivo je napomenuti da su poznate ljekovite sorte zelenog čaja, opskrbljivane s ciljem postizanja zdravlja i dugovječnosti u carskim palačama u Drevna Kina, uzgajane su u onim planinskim pokrajinama u čijim se tlima već suvremenim analitičkim metodama utvrđuje visok sadržaj selena.
Nakon otkrića selena, ustanovljeno je da vitamin E i selen djeluju na različite dijelove istog procesa i da su međusobno striktno komplementarni, odnosno njihovo antioksidativno djelovanje dramatično raste kada se koriste zajedno. Sinergija oba antioksidansa od posebnog je interesa u kontekstu antikancerogenog djelovanja. Tako se pokazalo da primjena pripravaka selena istodobno s vitaminom E značajno povećava antikarcinogeni učinak u odnosu na eksperimentalne tumore.
Unos selena hranom ovisi o uvjetima i prirodi unosa hrane te o razini selena u prehrambenim proizvodima. Povrće i voće općenito su loš izvor selena, za razliku od žitarica, proizvoda od žitarica, mesa (osobito nusproizvoda), morskih plodova koji sadrže značajne količine selena, tipično preko 0,2 mg/kg mokre težine . Kemijski sastav Tlo i sadržaj selena u njemu značajno utječu na količinu selena u zrnu, varirajući od 0,04 mg/kg do 21 mg/kg.
Molibden. Ukupna količina molibdena u tijelu odrasle osobe je oko 7 mg. Sadržaj molibdena u krvi je oko 0,5 mikrograma na 100 ml. Veće koncentracije ovog elementa pronađene su kod ljudi koji žive u regijama gdje je tlo najbogatije spojevima ovog metala. Tako su u nekim regijama Armenije zabilježeni česti slučajevi gihta među stanovnicima koji jedu uglavnom lokalne proizvode, u kojima je pronađena izrazito visoka razina molibdena. Njegov sadržaj u prehrani stanovnika ove regije bio je 10-15 mg. U drugim područjima gdje su slučajevi gihta bili rjeđi, ljudi su dobivali samo 1-2 mg molibdena dnevno iz hrane.
Molibden je sastavni dio niza enzima, kao što su ksantin oksidaza, aldehid oksidaza, sulfat oksidaza. Poznato je da molibden inhibira razvoj karijesa.
Procijenjena dnevna potreba za molibdenom je 2 mcg po 1 kg tjelesne težine. U Rusiji je dnevni unos molibdena 0,27 mg.
najbogatiji molibdenom različite vrste povrće (kao što su mahunarke) i unutarnji organi životinja.
Kobalt. Biološki učinak kobalta poznat je od 1948. godine, kada su znanstvenici Rickes i Smith otkrili da je atom kobalta središnji u molekuli vitamina B 12. Maksimalna koncentracija kobalta u tkivima je oko 100 μg/kg. Ukupni sadržaj kobalta u tijelu odrasle osobe je 5 mg. Osoba s hranom dnevno prima 5,63 -7,94 mikrograma kobalta, od čega se 73 - 97% apsorbira.
Prosječna dnevna potreba za kobaltom je 60 mcg po 1 kg tjelesne težine. Vjeruje se da je osobi potreban kobalt samo u obliku cijanokobalamina (vitamin B 12). U nekim zemljama, spojevi kobalta korišteni su kao aditivi za hranu pivu za stabilizaciju pjene. Međutim, pokazalo se da je takav aditiv uzrok srčanih bolesti kod konzumenata piva. Stoga je upotreba spojeva kobalta kao aditiva za hranu sada napuštena.
^
4 Utjecaj prerade na mineralni sastav namirnica
Pri preradi prehrambenih sirovina u pravilu dolazi do smanjenja sadržaja mineralnih tvari (osim Na, dodanog u obliku prehrambene soli). U biljnoj hrani se gube s otpadom. Tako se smanjuje sadržaj niza makro-, a posebno mikroelemenata tijekom proizvodnje žitarica i brašna nakon prerade zrna, budući da je tih komponenti više u odstranjenim ljuskama i klicama nego u cijelom zrnu. Komparativna analiza mineralni sastav u pšeničnom brašnu najvišeg stupnja i brašnu od cjelovitih žitarica dat je u nastavku (sadržaj elemenata je naveden u mg/100 g proizvoda):
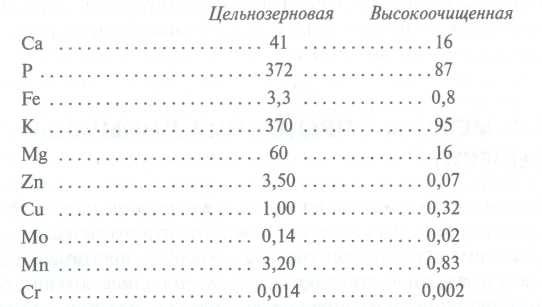
Primjerice, zrno pšenice i raži u prosjeku sadrži oko 1,7% elemenata pepela, dok u brašnu, ovisno o sorti, od 0,5 (u najvišem razredu) do 1,5% (u cjelovitom zrnu). Prilikom čišćenja povrća i krumpira gubi se 10 do 30% minerala. Ako se podvrgnu toplinskom kuhanju, tada se, ovisno o tehnologiji (kuhanje, prženje, pirjanje), gubi još 5 do 30%.
Meso, riblji proizvodi i perad uglavnom gube makronutrijente kao što su kalcij i fosfor tijekom odvajanja pulpe od kostiju.
Tijekom termičkog kuhanja (kuhanje, prženje, dinstanje) meso gubi od 5 do 50% minerala. Međutim, ako se obrada provodi u prisutnosti kostiju koje sadrže mnogo kalcija, moguće je povećati udio kalcija u kuhanim mesnim proizvodima za 20%.
U tehnološkom procesu, zbog nedovoljno kvalitetne opreme, određena količina mikroelemenata može prijeći u konačni proizvod. Dakle, pri izradi kruha tijekom pripreme tijesta kao rezultat kontakta tijesta s opremom sadržaj željeza može se povećati za 30%. Ovaj proces je nepoželjan, jer toksični elementi sadržani u obliku nečistoća u metalu također mogu proći u proizvod zajedno sa željezom. Kada se konzervirana hrana skladišti u gotovim limenkama (odnosno zalemljenim) konzervama s nekvalitetnim lemom ili ako je zaštitni sloj laka slomljen, vrlo otrovni elementi poput olova, kadmija i kositra mogu proći u proizvod.
Treba uzeti u obzir da brojni metali, poput željeza i bakra, čak i u malim koncentracijama, mogu uzrokovati neželjenu oksidaciju proizvoda. Njihove katalitičke oksidacijske sposobnosti posebno su izražene u odnosu na masti i masne proizvode. Tako, primjerice, pri koncentraciji željeza iznad 1,5 mg/kg i bakra od 0,4 mg/kg tijekom dugotrajnog skladištenja maslaca i margarina, ti metali uzrokuju užeglost proizvoda. Pri skladištenju pića u prisutnosti željeza iznad 5 mg/l i bakra 1 mg/l, pod određenim uvjetima, često se može uočiti zamućenje pića.
^
5. Metode za određivanje mineralnih tvari
Za analizu mineralnih tvari uglavnom se koriste fizikalno-kemijske metode – optičke i elektrokemijske.
Gotovo sve ove metode zahtijevaju posebnu pripremu uzoraka za analizu, koja se sastoji u preliminarnoj mineralizaciji predmeta proučavanja. Mineralizacija se može provesti na dva načina: "suho" i "mokro". "Suha" mineralizacija uključuje pougljenje, spaljivanje i kalciniranje ispitnog uzorka pod određenim uvjetima. "Mokra" mineralizacija također omogućuje obradu predmeta proučavanja koncentrirane kiseline(najčešće HNO 3 i H 2 SO 4).
^ Spektralne metode analize.
Fotoelektrokolorimetrija - analiza koja se temelji na mjerenju apsorpcije obojenih otopina monokromatskog zračenja u vidljivom području spektra. Mjerenja se provode pomoću fotoelektričnih kolorimetara opremljenih uskopojasnim filterima. Ako ispitivana tvar nije obojena, mora se kemijskom reakcijom s određenim reagensima pretvoriti u obojeni spoj (fotometrijska analitička reakcija).
Spektrofotometrija je metoda analize koja se temelji na mjerenju apsorpcije monokromatskog zračenja u ultraljubičastom, vidljivom i infracrvenom području spektra. Takva se mjerenja provode pomoću spektrofotometara, gdje se kao monokromatizatori koriste disperzivne prizme i difrakcijske rešetke.
Kvantitativna analiza iona koji se proučava obično se provodi metodom kalibracijske krivulje.
Emisiona spektralna analiza. Metode spektralne analize emisije temelje se na mjerenju valne duljine, intenziteta i drugih karakteristika svjetlosti koju emitiraju atomi i ioni tvari u plinovitom stanju. Emisiona spektralna analiza omogućuje određivanje elementarnog sastava anorganskih i organskih tvari.
Intenzitet spektralne linije određen je brojem pobuđenih atoma u izvoru uzbude, koji ne ovisi samo o koncentraciji elementa u uzorku, već i o uvjetima pobude. Uz stabilan rad izvora uzbude, odnos između intenziteta spektralne linije i koncentracije elementa (ako je dovoljno mala) je linearan, tj. ovaj slučaj kvantitativna analiza može se provesti i metodom kalibracijske krivulje.
Najveću primjenu kao izvor uzbude dobio je električni luk, iskra, plamen. Temperatura luka doseže 5000 - 6000°C. U luku je moguće dobiti spektar gotovo svih elemenata. S iskričnim pražnjenjem razvija se temperatura od 7000 - 10000 ° C i svi elementi se pobuđuju. Plamen daje dovoljno svijetao i stabilan emisijski spektar. Metoda analize koja koristi plamen kao izvor uzbude naziva se analiza emisije plamena. Ovom metodom se utvrđuje više od četrdeset elemenata (zemnoalkalna i zemnoalkalna, Cu 2 , Mn 2 itd.).
^ Atomska apsorpcijska spektroskopija . Metoda se temelji na sposobnosti slobodnih atoma elemenata u plamenim plinovima da apsorbiraju svjetlosnu energiju na valnim duljinama karakterističnim za svaki element.
U atomskoj apsorpcijskoj spektroskopiji gotovo je potpuno isključena mogućnost preklapanja spektralnih linija različitih elemenata, jer je njihov broj u spektru znatno manji nego u emisijskoj spektroskopiji.
Smanjenje intenziteta rezonantnog zračenja u uvjetima atomske apsorpcijske spektroskopije podliježe eksponencijalnom zakonu smanjenja intenziteta ovisno o debljini sloja i koncentraciji tvari, slično Bouguer-Lambert-Beerovom zakonu
Konstantnost debljine sloja koji apsorbira svjetlost (plamen) postiže se pomoću plamenika posebnog dizajna. Metode atomske apsorpcijske spektralne analize naširoko se koriste za analizu gotovo svakog tehničkog ili prirodnog objekta, posebno u slučajevima kada je potrebno odrediti male količine elemenata.
Metode za određivanje atomske apsorpcije razvijene su za više od 70 elemenata.
^ 2. Elektrokemijske metode analize.
Ionometrija. Metoda se koristi za određivanje K iona , Na , ca 2 , Mn 2 , F - , ja - , Sl - itd.
Metoda se temelji na korištenju ionsko-selektivnih elektroda čija je membrana propusna za određenu vrstu iona (dakle, u pravilu, visoka selektivnost metode).
Kvantitativni sadržaj iona koji se utvrđuje provodi se ili pomoću kalibracijskog grafa, koji je ucrtan u koordinatama E - pC, ili metodom zbrajanja. Standardna metoda adicije preporučuje se za određivanje iona u složenim sustavima koji sadrže visoke koncentracije stranih tvari.
polarografija. Metoda polarografije izmjenične struje koristi se za određivanje toksičnih elemenata (živa, kadmij, olovo, bakar, željezo).
Metoda se temelji na proučavanju strujno-naponskih krivulja dobivenih tijekom elektrolize elektrooksidirajuće ili elektroreducirajuće tvari. Kao indikatorska elektroda u polarografiji najčešće se koristi živina kap elektroda, ponekad čvrste mikroelektrode - platina, grafit. Kao referentna elektroda koristi se ili živa izlivena na dno elektrolizera ili zasićena kalomelna polućelija.
Kako napon raste, dolazi trenutak kada se svi ioni koji zbog difuzije ulaze u elektrodu odmah isprazne i njihova koncentracija u sloju blizu elektrode postaje konstantna i praktički jednaka nuli. Struja koja teče u strujnom krugu u tom trenutku naziva se struja granične difuzije.
Kvantitativna polarografska analiza temelji se na korištenju izravne proporcionalna ovisnost veličina difuzijske struje na koncentraciju elementa koji se utvrđuje.
^ MINERALNI ELEMENTI
Mineralni (pepeo) elementi nalaze se u prehrambenim proizvodima u obliku organskih i anorganskih spojeva. Ima ih u mnogim organskim
tvari različitih klasa - bjelančevine, masti, glikozidi, enzimi itd. Obično se mineralni elementi određuju u pepelu nakon izgaranja prehrambenih proizvoda, budući da je prilično teško točno odrediti koje su tvari iu kojoj količini ti elementi uključeni.
Uloga mineralnih elemenata u životu ljudi, životinja i biljaka je ogromna: svi fiziološki procesi u živim organizmima odvijaju se uz sudjelovanje tih elemenata. Dakle, u ljudskom i životinjskom tijelu mineralni elementi sudjeluju u plastičnim procesima, formiranju i izgradnji tkiva, u metabolizmu vode, u održavanju osmotskog tlaka krvi i drugih tjelesnih tekućina, u održavanju acidobazne ravnoteže u tijelu, i uključeni su u kompleks tvari koje čine žive stanice protoplazme, u sastav nekih endokrinih žlijezda itd.
Mineralni sastav organizama mijenja se s godinama; starenjem se uočava mineralizacija organizama. Dakle, novorođena djeca sadrže oko 34 g minerala na 1 kg tjelesne težine, a kod odrasle osobe sadržaj tih tvari raste na 43 g ili više.
U ljudskom i životinjskom tijelu pronađeno je više od 70 mineralnih elemenata. Mnogi enzimski procesi koji se odvijaju u različitim tkivima tijela zahtijevaju sudjelovanje brojnih mineralnih elemenata. Dakle, za pretvorbu pirogrožđane kiseline u octenu kiselinu ili glukoze u fruktozu ili fosfoglicerola u glukozu-6-manozu-6- i fruktozo-6-fosfat potrebno je sudjelovanje magnezijevih iona. Kalcijevi ioni inhibiraju razvoj ovog procesa.
Minerali su neravnomjerno raspoređeni u tkivima ljudskog tijela. U tvrdim tkivima prevladavaju dvovalentni elementi: kalcij (Ca) i magnezij (Mg), a u mekim tkivima - jednovalentni elementi: kalij (K) i natrij (Na). Osim toga, puno fosfora (P) nakuplja se u tvrdim tkivima, uglavnom u obliku fosfatnih soli. S nedostatkom minerala u hrani, ti spojevi se izlučuju iz organizma i poremeti normalan metabolizam.
Mineralne tvari otopljene u krvnoj plazmi, međustaničnim i drugim tjelesnim tekućinama stvaraju određeni osmotski tlak, koji ovisi o molarnoj koncentraciji tvari otopljenih u tekućini. Soli u većoj mjeri povećavaju osmotski tlak
stupnju nego neelektroliti pri istoj molarnoj koncentraciji, budući da se soli disociraju u ione. Osmotski tlak ovisi o ukupnom broju nedisociranih molekula i iona. Osmotski tlak krvi, limfe i međustanične tekućine ljudskog i životinjskog tijela ovisi uglavnom o natrijevom kloridu (NaCl) otopljenom u njima.
Osmotski tlak u tjelesnim tekućinama utječe na raspodjelu vode i otopljenih tvari u tkivima. U viših životinja osmotski tlak je konstantan i iznosi 7,5 - 9,0 atm. Održavanje konstantnog osmotskog tlaka osigurava se djelovanjem organa za izlučivanje, uglavnom bubrega i znojnih žlijezda.
Ulazak mineralnih soli u krv dovodi do ulaska međustanične vode u krv, pa se stoga koncentracija soli u krvi smanjuje. Višak vode i soli tada se uklanjaju bubrezima. Smanjenje količine vode u tkivima, refleksno djelujući na živčane centre, uzrokuje žeđ.
Normalna vitalna aktivnost ljudskog tijela može se odvijati samo s određenim svojstvima međustaničnih i međustaničnih tekućina. U toj postojanosti okoliša važnu ulogu igra kiselinsko-bazna ravnoteža u kojoj je reakcija krvi, limfe i drugih tjelesnih tekućina bliska neutralnoj. Kiselinsko-baznu ravnotežu održava složeni sustav regulatori ujedinjeni u jednu središnju živčani sustav. Takvi regulatori su sustavi pufera krvi, izmjena kisika i ugljičnog dioksida, soli ugljičnog dioksida i klorida, funkcije izlučivanja bubrega, pluća, znojnih žlijezda itd.
U procesu složene transformacije u ljudskom tijelu hrane bogate kalcijem, magnezijem, natrijem ili kalijem mogu nastati alkalni spojevi. Izvori elemenata koji tvore lužine uključuju voće, povrće, mahunarke, mlijeko i mliječne proizvode.
Ostali proizvodi, kao što su meso, riba, jaja, sir, kruh, žitarice, tjestenina, u procesu transformacije u ljudskom tijelu daju kisele spojeve.
Priroda prehrane može utjecati na promjene kiselinsko-bazne ravnoteže u tkivima ljudskog tijela. Kiselinsko-bazna ravnoteža često pomiče > stranu kiselosti. Kao rezultat oštrog pomaka
dopuštene maksimalne norme za sadržaj pepela, a pri ocjenjivanju takvih proizvoda određuju njegovu količinu.
Obično se razlikuju dva koncepta - "ukupni (sirovi) pepeo" i "čisti pepeo". Pojam "ukupni pepeo" označava zbroj mineralnih elemenata ili njihovih oksida koji su dio kemijske strukture prehrambenih proizvoda, kao i uneseni u proizvod tijekom njegove proizvodnje ili "slučajno uhvaćeni kao nečistoće". "Čisti pepeo" označava zbroj mineralnih elemenata ili njihovih oksida bez primjesa .
Sadržaj pepela u proizvodu određuje se spaljivanjem. Da biste to učinili, uzorak se najprije pažljivo spali, a zatim kalcinira do konstantne težine. Povećana količina pepela u odnosu na normu ukazuje na kontaminaciju proizvoda pijeskom, metalnim česticama i zemljom.
Za određivanje "čistog pepela" dobiveni pepeo se tretira s 10% klorovodičnom kiselinom. U ovom slučaju, "čisti pepeo" se otapa u klorovodičnoj kiselini, a ostatak će ukazivati na prisutnost stranih anorganskih nečistoća u proizvodu. Dakle, u slučaju lošeg pranja rajčice prije prerade, odnosno u krumpirovom škrobu, uz nedovoljno pranje gomolja, dolazi do povećane količine pepela zbog stranih mineralnih nečistoća.
Kalcij u ljudskom tijelu nalazi se u koštanom tkivu i zubima - oko 99%. Ostatak kalcija ulazi u krv u obliku iona iu stanju povezanom s proteinima i drugim spojevima.
Dnevna potreba odrasle osobe za kalcijem je 0,8-1,0 g. Trudnice i dojilje trebaju povećane količine kalcija, do 1,5-2 g dnevno, kao i djeca u čijim se tijelima kalcij intenzivno koristi za formiranje kostiju. Nedostatak kalcija uzrokuje deformitet skeleta, krhkost kostiju i atrofiju mišića u tijelu. Kalcij karakterizira značajka da se čak i uz nedostatak u hrani nastavlja izlučivati iz tijela u značajnim količinama.
Kalcij se nalazi u prehrambenim proizvodima u obliku fosfatnih i oksalat kloridnih soli, kao iu kombinaciji s masnim kiselinama, bjelančevinama itd.
Svi kalcijevi spojevi, s izuzetkom CaC!a, teško su topljivi u vodi, te se stoga slabo apsorbiraju
ljudsko tijelo. Netopljivi kalcijevi spojevi djelomično prelaze iz proizvoda u otopinu u želucu pod djelovanjem klorovodične kiselineželučana kiselina. Apsorpcija kalcija iz prehrambenih proizvoda od strane ljudskog organizma u velikoj mjeri ovisi o prisutnosti fosfata, masti, magnezijevih spojeva itd. u hrani. Dakle, apsorpcija kalcija je najveća kada je omjer kalcija i fosfora I u hrani ; 1,5 ili 1:2. Povećana količina fosfora u hrani u odnosu na navedene omjere dovodi do naglog smanjenja apsorpcije kalcija. Višak magnezija također negativno utječe na apsorpciju kalcija u ljudskom tijelu. Oštro negativan učinak na apsorpciju kalcija imaju spojevi kalcija s inozitol-fosfornom kiselinom, koja se u značajnim količinama nalazi u zrnu žitarica i proizvodima njegove prerade.
Vitamin D ima vrlo važnu ulogu u apsorpciji kalcija, koji potiče prijelaz soli kalcija i fosfora iz crijeva u krv i taloženje u kostima u obliku kalcijevog fosfata.
Sadržaj kalcija u nekim prehrambenim proizvodima je sljedeći (mg%): u nemasnom mesu - 7; u jajima - 54; u mlijeku - 118; u siru - 930; u svježem siru - 140; u zobenim pahuljicama - 65; u pšeničnom brašnu - 15; u riži - 9; u jabukama - 7; u narančama - 45; u orasima -89; u repi - 29; u karfiolu - 89; u bijelom kupusu - 45; u mrkvi - 56; u krumpiru - 14. Iz navedenih podataka vidljivo je da su za čovjeka najvažniji izvor kalcija mliječni proizvodi. Kalcij u mliječnim proizvodima, kao i povrću i voću, lako je probavljiv spoj.
Magnezija je u ljudskom tijelu 30-35 puta manje od kalcija, ali je vrlo važan. Najviše magnezija nalazi se u koštanom tkivu. Magnezij ima posebnu ulogu u biljkama koje nose klorofil, gdje je dio molekule klorofila. Kao i kalcij, magnezij stvara teško topive spojeve. Magnezij je posebno teško asimilirati u prisutnosti LO$ iona.
Sadržaj magnezija u nekim prehrambenim proizvodima je sljedeći (mg%): u grahu - 139; u zobenim pahuljicama - 133; u grašku - 107; u prosu - 87; u pšeničnom kruhu - 30; u krumpiru - 28; u mrkvi - 21; u bijelom kupusu -!Ana - 12; u jabukama - 8; u limunu - 7; u govedini - 15; u jajima - 11; u mlijeku - 12. Posljedično, 2 * 35 magnezija nalazi se u najvećim količinama u žitaricama i mahunarkama.
Potreba za magnezijem za odraslu osobu je 400 mg dnevno.
Natrij se široko nalazi u hrani, posebno u proizvodima životinjskog podrijetla. Glavni izvor natrija za ljudsko tijelo je NaCt (obična sol). Natrij ima važnu ulogu u procesima unutarstaničnog i međutkivnog metabolizma. Oko 90% osmotskog tlaka krvne plazme ovisi o sadržaju NaCl u njoj. Obično se 3,3 g natrija otopi u litri ljudske krvne plazme. NaC! Također igra važnu ulogu u reguliranju metabolizma vode u tijelu. Natrijevi ioni uzrokuju oticanje koloida tkiva i time doprinose zadržavanju vezane vode u tijelu. Iz tijela NaC! izlučuje se uglavnom mokraćom i znojem. Pojačanim radom i potrošnjom tekućine čovjek izgubi i do 3-5 litara znoja, što je 99,5% vode. U suhoj tvari znoja glavni dio je NaGI.
Kuhinjska sol, koja s hranom ulazi u ljudski organizam, nadoknađuje potrošnju NaCI u krvi i koristi se za stvaranje klorovodične kiseline u želučanom soku, kao i za sintetiziranje NaHCO3 u žlijezdi gušterače. Prisutnost NaHCO3 objašnjava alkalnu reakciju soka gušterače, koja je neophodna za razgradnju proteina hrane enzimom tripsinom.
Dnevna potreba odrasle osobe za natrijem je 4-6 g, što odgovara 10-15 g kuhinjske soli. Uobičajena prehrana stanovništva sadrži dovoljne količine natrija, jer se u hranu dodaje kuhinjska sol.
Kalij je stalno iu značajnim količinama prisutan u prehrambenim proizvodima, posebice biljnog podrijetla.U pepelu biljaka sadržaj kalija ponekad iznosi i više od 50% njegove mase.
U ljudskom tijelu kalij je uključen u enzimske reakcije, stvaranje puferskih sustava koji sprječavaju pomake u reakciji okoline. Kalij smanjuje
sposobnost zadržavanja vode bjelančevina, smanjujući njihovu hidro-(sposobnost), a time pospješuju izlučivanje vode i natrija iz tijela, pa se kalij može smatrati nekim fiziološkim antagonistom natrija.
Dnevna potreba odrasle osobe za kalijem je 3-5 g.
Željezo je široko rasprostranjeno u prirodi. Općenito, gotovo sva prirodna hrana sadrži željezo, ali u malim količinama.
U ljudskim i životinjskim organizmima željezo je dio najvažnijih organskih spojeva – hemoglobina u krvi, mioglobina, nekih enzima – katalaze, peroksidaze, citokrom oksidaze itd. Hemoglobin u krvi sadrži 2A, željezo u tijelu. Značajna količina željeza nalazi se u slezeni i jetri. Željezo ima sposobnost nakupljanja u tijelu. Hemoglobin u krvi uništava se tijekom života, a željezo oslobođeno u ovom slučaju tijelo može ponovno iskoristiti za stvaranje hemoglobina.
Željezo, koje je dio voća i povrća, ljudski organizam dobro apsorbira, dok je većina željeza u proizvodima od žitarica u neprobavljivom obliku za tijelo.
Dnevna potreba žlijezde odraslog čovjeka je 15 mg.
l l o r je dio prirodne hrane u malim količinama. Biljni proizvodi sadrže malo klora, dok proizvodi životinjskog porijekla sadrže nešto više. Dakle, sadržaj klora u govedini je 76 mg%, u mlijeku - 106, u jajima -
37106, u siru - 880, u prosu - 19, u krumpiru - 54, u jabukama - 5 mg%.
Sadržaj klora značajan je u krvi i drugim tjelesnim tekućinama, kao iu koži, plućima i bubrezima. Klor je u tijelu u ioniziranom stanju u obliku aniona soli natrija, kalija, kalcija, magnezija, mangana. Spojevi klora u prehrambenim proizvodima vrlo su topljivi i lako se apsorbiraju u ljudskom crijevu. Anioni klora, zajedno s kationima natrija, igraju važnu ulogu u stvaranju i regulaciji osmotskog tlaka krvi i drugih tjelesnih tekućina. Klorne soli osiguravaju stvaranje klorovodične kiseline u želučanoj sluznici.
Glavnu potrebu za klorom podmiruje natrijev klorid koji se hrani dodaje u obliku soli.
Ukupna količina natrijevog klorida u ljudskom organizmu je obično 10-15 g, ali pri jedenju hrane bogate klorovim solima sadržaj klora u ljudskom tijelu može doseći i veću količinu. Dnevna ljudska potreba za klorom je 5-7 g.
Sumpora se u najvećim količinama nalazi u proizvodima od žitarica, mahunarkama, mliječnim proizvodima, mesu, ribi, a posebno u jajima. Dio je gotovo svih proteina ljudskog tijela, a posebno je bogat aminokiselinama - cistinom, metioninom. Izmjena sumpora u tijelu je uglavnom njegova transformacija u naznačene aminokiseline. Također sudjeluje u stvaranju vitamina Bg (tiamina), inzulina i nekih drugih spojeva. Mnogo je sumpora u proteinoidima potpornih tkiva, na primjer, u keratinu kose, noktiju itd.
Kada se spojevi oksidiraju u tijelu, značajan dio sumpora se izlučuje mokraćom u obliku soli sumporne kiseline.
Dnevna potreba odrasle osobe za sumporom uz umjereni rad je oko 1 g.
Jod se nalazi u tijelu zdrave osobe težine 70 kg u količini od približno 25 mg. Polovica te količine nalazi se u štitnjači, a ostatak u mišićnom i koštanom tkivu te u krvi. Zamijenjeni su anorganski spojevi joda u štitnjači organski spojevi- tiroksin, di-jodtiroksin, trijodtiroksin. Jod se brzo apsorbira u štitnjači i nekoliko sati nakon ulaska u nju pretvara se u organski
veze. Ovi spojevi potiču metaboličke procese u tijelu. Kada s hranom u organizam uđe nedovoljna količina joda, poremeti se aktivnost štitnjače i nastaje ozbiljna bolest koja se zove endemska gušavost.
Najveća količina joda nalazi se u biljnim i životinjskim proizvodima obalnih područja, gdje je koncentriran u morskoj vodi, zraku i tlu obalnih područja. Malo joda nakuplja se u biljkama i životinjskim organizmima planinskih ili udaljenih od morskih obala područja joda.
Sadržaj joda u proizvodima od žitarica, povrću, slatkovodnoj ribi ne prelazi 5-8 mcg na 100 g sirovog proizvoda. Govedina, jaja, maslac, voće odlikuju se većim sadržajem joda. morski kelj, morska riba i riblje ulje sadrže najveću količinu joda. Plodovi feijoe koji rastu na crnomorskoj obali Gruzije akumuliraju do 390 mikrograma joda na 100 g voćne mase, što je mnogo više od sadržaja ovog elementa u drugom voću i povrću.
U područjima gdje prehrambeni proizvodi sadrže nedovoljne količine joda, kuhinjskoj soli se dodaje kalijev jodid u količini od 25 g K1 po toni kuhinjske soli. Uz normalnu prehranu, osoba dnevno konzumira 200 mikrograma joda s jodiranom soli. Međutim, pri skladištenju jodirane soli jod postupno nestaje, pa se nakon 6 mjeseci jodirana sol prodaje kao obična kuhinjska sol.
Dnevna ljudska potreba za jodom je 100-260 mcg.
Fluor igra važnu ulogu u plastičnim procesima tijekom formiranja koštanog tkiva i zubne cakline. Najveća količina fluora koncentrirana je u kostima - 200-490 mg/kg i zubima - 240-560 mg/kg.
Čini se da je voda glavni izvor fluorida u ljudskom tijelu, pri čemu se Dodin fluorid bolje apsorbira od fluorida iz hrane. Sadržaj fluora u vodi za piće kreće se od 1 do 1,5 mg/l. Nedostatak fluora u vodi često utječe
39nne do razvoja bolesti zuba, poznate kao karijes. Višak fluora u vodi uzrokuje fluorozu u kojoj se narušava normalna struktura zuba, pojavljuju se mrlje na caklini i povećava se krhkost zuba. Djeca posebno pate od nedostatka ili viška fluora.
Dnevna ljudska potreba za fluorom još nije utvrđena. Smatra se da bi optimalna količina fluora u vodi za piće za zdravlje trebala biti 0,5-1,2 mg/l.
Bakar u životinjskom tijelu, uz željezo, igra važnu ulogu u procesima hematopoeze, potiče oksidativne procese te je stoga povezan s metabolizmom željeza. Dio je enzima (laktaza, askorbat oksidaza, citokrom oksidaza itd.) kao metalna komponenta.
U biljkama bakar pojačava oksidativne procese, ubrzava rast i povećava prinos mnogih usjeva.
U onim malim količinama u kojima se bakar nalazi u prirodnim proizvodima, ne šteti ljudskom tijelu. Ali povišene količine bakra mogu uzrokovati trovanje. Dakle, istovremeni unos 77-120 mg bakra može uzrokovati mučninu, povraćanje, a ponekad i proljev. Stoga je sadržaj bakra u prehrambenim proizvodima reguliran važećim propisima Ministarstva zdravstva SSSR-a. Na 1 kg proizvoda, ovisno o sadržaju krutih tvari u njemu, dopušteno je od 5 do 30 mg bakra. Dakle, u koncentriranoj pasti od rajčice, sadržaj bakra ne smije biti veći od 30 mg / kg, u pireu od rajčice - 15-20, u konzerviranom povrću - 10, u pekmezu i marmeladi - 10, u voćnim kompotima - 5 mg / kg.
Bakar može dospjeti u prehrambene proizvode tijekom njihove proizvodnje - iz bakrenih dijelova opreme, pri tretiranju vinograda pesticidima koji sadrže bakar itd.
Dnevna potreba odrasle osobe za bakrom je 2 mg.
Cink se nalazi u svim tkivima životinja i biljaka. Uz nedostatak cinka u organizmima mladih žena,
Kod biljaka je njihov rast odgođen, a njegovim nedostatkom u tlu nastaju bolesti mnogih biljaka što često dovodi do njihove smrti.
Cink je dio niza enzima, a posebno je važna njegova uloga u molekuli enzima karboanhidraze, koja sudjeluje u vezivanju i izlučivanju ugljičnog dioksida iz životinjskog tijela. Cink je neophodan za normalnu funkciju hormona hipofize, nadbubrežne žlijezde i gušterače. Također utječe na metabolizam masti, povećava razgradnju masti i sprječava masnu jetru.
Cink u hrani u velikim količinama može uzrokovati trovanje. Kisela i masna hrana otapa metalni cink, te je stoga kuhanje ili pohranjivanje hrane u opremi ili posuđu od cinka neprihvatljivo. Trovanje cinkom slično je trovanju bakrom, ali je izraženije i praćeno pečenjem i bolovima u ustima i želucu, povraćanjem, proljevom i slabošću srca. Posuđe od cinka dopušteno je samo za spremanje hladne pitke vode, jer je u tom slučaju topljivost cinka zanemariva.
Dnevna potreba odrasle osobe za cinkom je 10-15 mg. Povećana potreba za cinkom uočava se tijekom rasta i puberteta. Uz normalnu prehranu, osoba dobiva dovoljnu količinu cinka iz hrane.
Olovo se u životinjskim i biljnim proizvodima nalazi u vrlo malim količinama. Dakle, u jabukama, kruškama, grožđu, jagodama sadržaj olova je oko 0,1 mg po 1 kg proizvoda, u mlijeku - 0,8, u mesu - 0,05, u jesetri - 0,06 mg na 1 kg proizvoda.
Olovo je otrovan metal za ljude, ima sposobnost nakupljanja u tijelu, uglavnom u jetri, te uzrokovati teška kronična trovanja.
Uz svakodnevnu upotrebu 2-4 mg olova s hranom, znak trovanja olovom može se otkriti nakon nekoliko mjeseci.
41 Kontaminacija hrane olovom može biti od pribora, lemova, glazura, opreme i insekticida koji sadrže olovo. Najčešće se trovanje olovom događa kada se hrana pohranjuje u zanatskoj zemljanoj posudi koja nije dobro prekrivena olovnom glazurom.
Zbog visoke toksičnosti sadržaj olova u prehrambenim proizvodima nije dopušten.
Kositar se u prehrambenim proizvodima nalazi u malim količinama. Tako je u jetri bika i ovna pronađeno 0,14 mg/kg kositra, u bubrezima 0,003, u plućima 0,63, a u mozgu 0,019 mg/kg.
Kositar nije tako otrovan metal kao olovo, cink ili bakar, stoga je dopušten u ograničenim količinama u opremi prehrambenih poduzeća, kao i za kalajisanje površine kositra, od koje se pripremaju limenke, štiteći je od korozije. Međutim, često tijekom dugotrajnog skladištenja konzervirane hrane u limenkama, masa proizvoda stupa u interakciju s kositrenim premazom kositra, zbog čega nastaju kositrene soli organskih kiselina. Ovaj proces je posebno aktivan kada se u limenci nalaze proizvodi s visokom kiselošću - voće, riblje konzerve i povrće u umak od rajčice i dr. Tijekom dugotrajnog skladištenja sadržaj kositra u konzerviranoj hrani može značajno porasti. Sadržaj kositra posebno se brzo povećava u proizvodima koji se nalaze u otvorenim metalnim limenkama obloženim kositrom.
Za pojačanu zaštitu limenke od korozije, na površinu lima se dodatno nanose posebni kiselootporni lakovi ili emajl ili se na površini lima stvara tanak sloj stabilnih kositrenih oksida.
Mangan je široko rasprostranjen u životinjskim i biljnim proizvodima. Aktivno sudjeluje u stvaranju mnogih enzima, formiranju kostiju, procesima hematopoeze i potiče rast. U biljkama mangan pospješuje proces fotosinteze i stvaranje askorbinske kiseline.
Biljni proizvodi su u većini slučajeva bogatiji manganom od životinjskih proizvoda. Dakle, sadržaj mangana u proizvodima od žitarica doseže 1-15 mg po 1 kg, u listu
povrće - 10-20, u voću - 0,5-1, u mlijeku - 0,02-0,03, u jajima - 0,1-0,2, u jetri životinja - 2,65-2,98 mg po 1 kg.
Uz nedostatak mangana u tlu, biljke obolijevaju i slabo se razvijaju, smanjuje se prinos voća, povrća i drugih usjeva. Dodatak tlu mikrognojiva koja sadrže mangan pomaže u povećanju prinosa.
Dnevna potreba odrasle osobe za manganom je 5-10 mg dnevno.
Radioaktivni izotopi su prisutni u ljudskom tijelu, kontinuirano ulaze i izlaze iz tijela. Postoji ravnoteža između unosa radioaktivnih spojeva u tijelo i njihovog uklanjanja iz tijela. Svi prehrambeni proizvodi sadrže radioaktivne izotope kalija (K40), ugljika (C14), vodika (H3), a također i radija s njegovim produktima raspadanja.
Najveća koncentracija pada na kalij (K40). Izotopi sudjeluju u metabolizmu zajedno s neradioaktivnim.
Vjeruje se da tijekom sljedećeg geološkog vremena nije došlo do velikih promjena u intenzitetu zračenja na Zemlji, dakle, u životinjskom i Flora razvila svojevrsnu imunost na te razine zračenja. Ali živi organizmi su vrlo osjetljivi na povišene koncentracije. Male koncentracije povećavaju rast živih organizama, velike koncentracije uzrokuju pojavu aktivnih radikala, zbog čega dolazi do kršenja vitalne aktivnosti pojedinih organa i tkiva, kao i cijelog organizma.
Na atomske eksplozije radioaktivni izotopi padaju na površinu Zemlje, zagađujući atmosferu, vodu, tlo i biljke. Putem hrane, atmosfere i vode radioaktivni izotopi ulaze u ljudski organizam.
Utvrđeno je da kada se prehrambeni proizvodi tretiraju zračenjem radioaktivnih izotopa, njihov rok trajanja se povećava, a klijanje krumpira odgađa. Ali obično, ozračena hrana može imati specifičan miris i okus, a moguće je i stvaranje otrovnih tvari. Za utvrđivanje sigurnosti takvih proizvoda potrebni su dugoročni eksperimenti.
test pitanja
Koji su kemijski elementi makronutrijenti?
Koje su funkcije minerala u ljudskom tijelu?
Koja je uloga kalcija u ljudskom tijelu?
Koji se kemijski elementi klasificiraju kao elementi u tragovima i koje su njihove funkcije u ljudskom tijelu?
Kakvu ulogu ima željezo u ljudskom tijelu i u kojoj se hrani nalazi?
Koje su posljedice nedostatka joda u tijelu i kako se to može izbjeći?
Koje vrste tehnološke obrade sirovina i prehrambenih proizvoda pridonose gubitku minerala?
Navedite primjere interakcije nekih mikroelemenata i vitamina.
Koje metode za određivanje sadržaja makro- i mikroelemenata poznajete?