Elementy mineralne.doc
Minerały1. Rola pierwiastków mineralnych w organizmie człowieka 1
2. Makroelementy, ich charakterystyka
3. Pierwiastki śladowe, ich charakterystyka
4. Wpływ obróbki technologicznej
O składzie mineralnym produktów spożywczych
5. Metody oznaczania substancji mineralnych
1. Rola pierwiastków mineralnych w organizmie człowieka
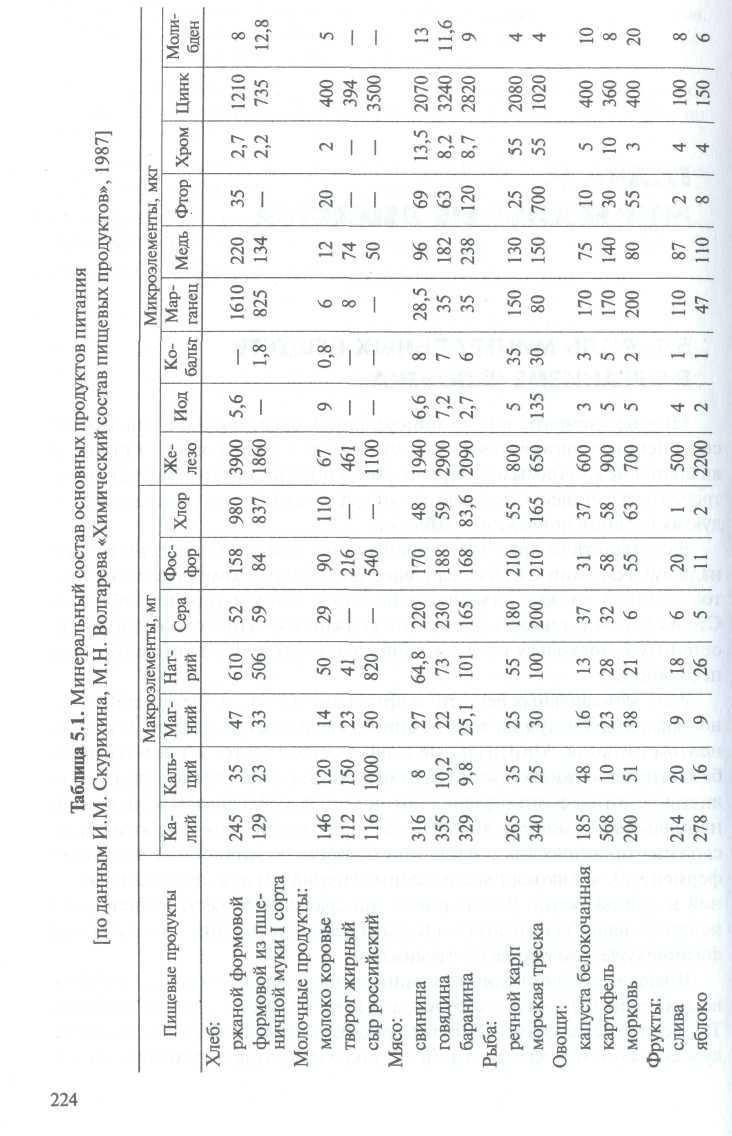
Wiele pierwiastków w postaci soli mineralnych, jonów, związków kompleksowych i materia organiczna są częścią żywej materii i są niezbędnymi składnikami odżywczymi, które muszą być spożywane codziennie z pożywieniem. Zawartość składników mineralnych w głównych produktach spożywczych podana jest w tabeli. 5.1.
Jak określić brak magnezu w organizmie?
Pierwszą oznaką obecności niezbędnych metali jest odwrócenie objawów i przywrócenie optymalnego wzrostu u bydła. Z biegiem czasu badania biochemiczne doprowadziły do wyizolowania enzymów, które wymagały działania jonów metali, a wkrótce potem te specyficzne enzymy mogły być związane z objawami niedoboru.
Zmiany w układzie pokarmowym
Oddziaływania jonów metali uznano za szkodliwe i cenne dla systemu. Na przykład wczesne badania wykazały, że miedź wzmacnia działanie żelaza w łagodzeniu anemii u szczurów laboratoryjnych karmionych dietą na bazie mleka; ta obserwacja została powtórzona u kurcząt i świń i wkrótce przyciągnęła uwagę klinicystów, którzy przyjęli podobny bimetaliczny protokół leczenia ludzi z anemią. Wraz z pojawieniem się w tym samym czasie diet półoczyszczonych, nauka o żywieniu była u progu ważnych odkryć na temat roli niezbędnych składników mineralnych.
Zgodnie z zaleceniami Rady Dietetycznej Akademia Narodowa W USA dzienne spożycie pierwiastków chemicznych z pożywieniem powinno być na pewnym poziomie (tab. 5.2). Ta sama liczba pierwiastków chemicznych musi być codziennie wydalana z organizmu, ponieważ ich zawartość w nim jest stosunkowo stała.
Kofaktory mineralne zawierają duża grupa substancje nieorganiczne z większością jonów metali. Domena jonów metali obejmuje makrometale, jony metali śladowych i metaloidy. Szukając przyczyny ich konieczności, musimy zrozumieć, że jony metali nadają się do przeprowadzania niebezpiecznych reakcji chemicznych na powierzchniach enzymatycznych, reakcji, które mogą uszkodzić bardziej wrażliwe łańcuchy boczne aminokwasów organicznych w enzymie. Na przykład metale redoks, takie jak żelazo, mangan i miedź, mogą przyjmować elektrony w swojej strukturze, tymczasowo je zatrzymując, a następnie przenosić je do tlenu, tworząc wodę, aby bezpiecznie usunąć elektron.
Rola minerałów w organizmie człowieka jest niezwykle zróżnicowana, mimo że nie są one niezbędnym składnikiem pożywienia. Substancje mineralne zawarte w protoplazmie i płynach biologicznych odgrywają główną rolę w zapewnieniu stałości ciśnienia osmotycznego, które jest niezbędnym warunkiem prawidłowego funkcjonowania komórek i tkanek. Są częścią kompleksu związki organiczne(np. hemoglobina, hormony, enzymy) to tworzywo sztuczne do budowy tkanki kostnej i zębowej. W postaci jonów substancje mineralne biorą udział w przekazywaniu impulsów nerwowych, zapewniają krzepnięcie krwi i inne procesy fizjologiczne organizmu.
W istocie należy wziąć pod uwagę, że kofaktor metaliczny rozszerza repertuar dostępnych funkcji katalitycznych i jest wykonywany przez enzymy. Enzymy, które zależą od jonów metali jako kofaktorów, dzielą się na 2 kategorie: enzymy aktywowane metalami i metaloenzymy. Jak sama nazwa wskazuje, enzymy aktywowane metalami są pobudzane do wyższej aktywności katalitycznej dzięki obecności jedno- lub dwuwartościowego jonu metalu na zewnątrz białka. Metal może aktywować substrat, bezpośrednio wiązać enzym lub osiągnąć równowagę z enzymem przy użyciu jego ładunku jonowego, aby uzyskać korzystniejsze wiązanie z substratem lub lepsze środowisko katalityczne.
 |
W zależności od ilości minerałów w organizmie człowieka i produktach spożywczych dzieli się je na: makro- oraz pierwiastki śladowe. Tak więc, jeśli ułamek masowy pierwiastka w ciele przekracza 10 -2%, należy go uznać za makroelement. Proporcja pierwiastków śladowych w organizmie wynosi 10 -3 -10 -5%. Jeśli zawartość pierwiastka jest poniżej 10 -5%, uważa się go za ultramikroelement. Makroelementy obejmują potas, sód, wapń, magnez, fosfor, chlor i siarkę. Są one zawarte w ilościach mierzonych w setkach i dziesiątkach miligramów na 100 g tkanki lub pożywienia. Pierwiastki śladowe wchodzą w skład tkanek organizmu w stężeniach wyrażonych w dziesiątych, setnych i tysięcznych miligrama i są niezbędne do jego normalnego funkcjonowania. Pierwiastki śladowe są warunkowo podzielone na dwie grupy: absolutnie lub witalną (kobalt, żelazo, miedź, cynk, mangan, jod, brom, fluor) i tzw. prawdopodobnie niezbędne (glin, stront, molibden, selen, nikiel, wanad i kilka innych ). Pierwiastki śladowe nazywane są niezbędnymi, jeśli ich brak lub niedobór zaburza normalne funkcjonowanie organizmu.
Rozkład pierwiastków śladowych w organizmie zależy od ich właściwości chemicznych i jest bardzo zróżnicowany. Na przykład żelazo jest integralną częścią hemoglobiny, mioglobiny i innych pigmentów oddechowych, czyli substancji zaangażowanych w wchłanianie i transport tlenu do wszystkich tkanek organizmu; atomy miedzi są zawarte w aktywnym centrum wielu enzymów itp.
Dlatego enzymy aktywowane metalem wymagają obecności metalu w nadmiarze, być może 2-10-krotnym stężeniem enzymu. Ponieważ metal nie może wiązać się w bardziej trwały sposób, enzymy aktywowane metalem zazwyczaj tracą aktywność podczas oczyszczania.
W przeciwieństwie do tego, enzymy metaliczne mają kofaktor metalowy ściśle związany z określonym regionem na powierzchni białka. Z nielicznymi wyjątkami metale śladowe pojawiają się jako kofaktory dla enzymów metali. Silne połączenie uniemożliwia utratę jonu metalu przez dializę lub przez słabe czynniki dysocjacyjne. Enzymy metali mogą jednak utracić swój kofaktor metali i stać się nieaktywne, gdy zostaną potraktowane chelatorami metali, które mają silniejsze powinowactwo wiązania niż enzym i pokonują białko enzymu przez jon metalu.
Działanie mikroelementów może być również pośrednie – poprzez wpływ na intensywność lub charakter metabolizmu. Tak więc niektóre mikroelementy (na przykład mangan, cynk, jod) wpływają na wzrost, a ich niewystarczające spożycie z pokarmem hamuje normalne rozwój fizyczny dziecko. Inne pierwiastki śladowe (np. molibden, miedź, mangan) biorą udział w funkcji rozrodczej, a ich niedobór w organizmie negatywnie wpływa na tę stronę życia człowieka.
Jako grupy prostetyczne metale w metaloenzymach mają stosunek stechiometryczny reprezentowany przez pełny integrator. Metaloenzymy rzadko są przygotowywane do zwiększenia aktywności poprzez dodanie ich sprzężonego jonu metalu do enzymu. Problemem jest również geometria przestrzenna: metale w pierwszej serii stanów nieustalonych muszą mieć ściśle określone konfiguracje geometryczne wokół miejsca wiązania metalu.
Z wyjątkiem tych z cynkiem, enzymy z metalami z pierwszej serii przejściowej wydają się być bardzo jasne; na przykład czerwony kolor hemoglobiny lub Kolor niebieski ceruloplazmina związana z miedzią. Większość enzymów łączy żelazo z żelazem w postaci hemu lub jako specjalny układ żelaza z grupami siarki, znany jako centra żelazowo-siarkowe. Żelazo w hemie wykazuje silne powinowactwo do jonów magnezu w chlorofilu. Hem, który jest zasadniczo porfirynowym układem pierścieniowym z żelazem zlokalizowanym w centrum, jest najliczniejszą formą żelaza w białkach biologicznych.
Do najbardziej ubogich minerałów w diecie nowoczesny mężczyzna obejmują wapń i żelazo, nadmiar - sód i fosfor.
Brak lub nadmiar w diecie jakichkolwiek substancji mineralnych powoduje naruszenie metabolizmu białek, tłuszczów, węglowodanów, witamin, co prowadzi do rozwoju wielu chorób. Poniżej znajdują się charakterystyczne (typowe) objawy niedoboru różnych pierwiastków chemicznych w organizmie człowieka: Najczęstszą konsekwencją rozbieżności w ilości wapnia i fosforu w diecie jest próchnica zębów, przerzedzenie kości. Przy braku fluoru w wodzie pitnej szkliwo zębów ulega zniszczeniu, niedobór jodu w pożywieniu i wodzie prowadzi do chorób tarczycy. Dlatego minerały są bardzo ważne w eliminacji i zapobieganiu wielu chorobom.
Najpopularniejsze połączenia
Jako składnik centrów żelazowo-siarkowych, żelazo wchodzi w kilka schematów grupowych z pozostałościami cysteiny w enzymach, które pozwalają na bardziej bezpośredni kontakt z białkiem. Żelazo w tych centrach wiąże się z substratami, jak również przenosi elektrony i uczestniczy w reakcjach, które obejmują odwodnienie i przegrupowanie. Enzymy z centrami żelazowo-siarkowe obejmują oksydazę ksantynową, dehydrogenazę bursztynianową, akonitazę i kwas azotowy.
Taki układ pozwala enzymowi na usunięcie atomu wodoru z bardzo stabilnej Połączenia S-N. Niemetal może zastąpić żelazo w tych kompleksach. Enzymy z grupą hemową mają zwykle czerwono-brązowy kolor. Kolor motywował początkowe zainteresowanie tymi białkami i był czynnikiem motywującym do oznaczania białek hemu w mitochondriach jako „cytochromów”.


Wymieniamy przyczyny zaburzeń metabolicznych substancji mineralnych, które mogą wystąpić nawet przy ich wystarczającej ilości w pożywieniu:
A) niezrównoważone odżywianie (niewystarczająca lub nadmierna ilość białek, tłuszczów, węglowodanów, witamin itp.);
Chociaż tylko kilka rozpuszczalnych enzymów ma żelazo jako kofaktor, żelazo jest szczególnie widoczne w białkach związanych z błoną, które zawierają szlaki transportu elektronów. Właściwość redoks żelaza odgrywa dużą rolę w jego chemii jako kofaktor. Żelazo prawie zawsze bierze udział w przenoszeniu elektronów i często przekazuje elektrony cząsteczce tlenu.
Zarówno katalaza, jak i peroksydaza, dwa enzymy hemu, wykorzystują żelazo do interakcji z niebezpiecznymi utleniaczami. Oba enzymy znajdują się w cytozolu i peroksysomach, gdzie podczas normalnych procesów metabolicznych zachodzą szkodliwe reakcje utleniania. Być może najbardziej znanym enzymem zawierającym żelazo jest oksydaza cytochromu c, końcowy akceptor elektronów w mitochondrialnym łańcuchu transportu elektronów i enzym zdolny do rozszczepiania cząsteczki tlenu z wytworzeniem wody.
B) stosowanie metod kulinarnego przetwarzania żywności, powodujących utratę składników mineralnych np. podczas rozmrażania (w gorąca woda) mięso, ryby lub przy usuwaniu wywarów z warzyw i owoców, gdzie przechodzą sole rozpuszczalne;
C) brak terminowej korekty składu diety, gdy zmienia się zapotrzebowanie organizmu na składniki mineralne związane z przyczynami fizjologicznymi. Na przykład osoby pracujące w warunkach podniesiona temperaturaśrodowisko zewnętrzne wzrasta zapotrzebowanie na potas, sód, chlor i inne minerały, ponieważ większość z nich jest wydalana z organizmu wraz z potem;
Rola magnezu w organizmie człowieka
Cynk jest prawdopodobnie najbardziej rozpowszechnionym i wszechstronnym ze wszystkich metalowych kofaktorów. Ponad 300 enzymów ma kofaktor cynkowy. Około 3% genomu ssaków koduje białka palca cynkowego. Jako kofaktor cynk może pełnić zarówno funkcje strukturalne, jak i katalityczne. Te przykłady ilustrują, dlaczego cynk jest ważnym towarzyszem enzymów i białek.
Cynk jest uważany za miękki metal, ponieważ zachowuje się jak kation dwuwartościowy bez większych preferencji geometrycznych. Być może ta miękkość pozwala cynkowi przystosować się do wielu różnych środowisk fermentacji. Z tego powodu kompleksy cynkowe są bezbarwne, a sam cynk zachowuje się przede wszystkim jak kation. Innym przykładem jest zastosowanie cynku do polaryzacji wiązania estrowego lub amidowego, ułatwiając w ten sposób nukleofilowy atak wody na związek, jak w reakcjach katalizowanych przez karboksypeptydazę i aminopeptydazę.
D) naruszenie procesu wchłaniania minerałów w przewodzie pokarmowym lub zwiększona utrata płynów (na przykład utrata krwi).
^
2. Makroelementy, ich charakterystyka
Wapń. Jest głównym składnikiem strukturalnym kości i zębów; wchodzi w skład jąder komórkowych, płynów komórkowych i tkankowych, jest niezbędny do krzepnięcia krwi. Wapń tworzy związki z białkami, fosfolipidami, kwasami organicznymi; uczestniczy w regulacji przepuszczalności błon komórkowych, w przekazywaniu impulsów nerwowych, w molekularnym mechanizmie skurczów mięśni, kontroluje aktywność szeregu enzymów. Więc wapń pełni nie tylko funkcje plastyczne, ale także wpływa na wiele procesów biochemicznych i fizjologicznych w organizmie.
Miedź, podobnie jak żelazo, jest metalem redoks. Enzymy miedzi, choć nie tak liczne jak enzymy cynku, pełnią ważne funkcje biologiczne, głównie w cytozolu. Najbardziej złożone enzymy obejmują oksydazy multicorex, które mogą mieć od 4 do 8 atomów miedzi na enzym. Miedź w tych enzymach występuje w trzech różnych środowiskach chemicznych, znanych jako plastry typu 1, typu 2 i typu miedzi. Miejsce miedzi typu 1 nadaje niebieski kolor ceruloplazminie i innym niebieskim białkom z miedzią.
Miejsca wiązania miedzi w oksydazie politlenkowej tworzą triadę składającą się z miedzi typu 3 2 i miedzi typu 3 ułożonych w trójkąt równoramienny. Tlen wiąże się z tymi dwoma medykami typu 3 u podstawy trójkąta. Ze względu na skłonność do przyjmowania elektronów miedź jest silnym utleniaczem w układach biologicznych. Ta reakcja łączy metabolizm żelaza z miedzią i może wyjaśniać, w jaki sposób brak miedzi w żelazie zapobiega przenoszeniu żelaza i powoduje anemię u ludzi. Rzadko miedź odgrywa jedynie rolę strukturalną, a wiele enzymów, które mają miedź jako kofaktor, wykorzystuje metal w miejscu aktywnym.
Wapń jest pierwiastkiem ciężkostrawnym. Związki wapnia dostające się do organizmu człowieka wraz z pożywieniem są praktycznie nierozpuszczalne w wodzie. Alkaliczne środowisko jelita cienkiego sprzyja powstawaniu niestrawnych związków wapnia, a jedynie działanie kwasów żółciowych zapewnia jego wchłanianie.
Przyswajanie wapnia przez tkanki zależy nie tylko od jego zawartości w pożywieniu, ale także od jego stosunku do innych składników pożywienia, a przede wszystkim do tłuszczów, magnezu, fosforu i białek. Przy nadmiarze tłuszczu dochodzi do konkurencji o kwasy żółciowe, a znaczna część wapnia jest wydalana z organizmu przez jelito grube. Na wchłanianie wapnia niekorzystnie wpływa nadmiar magnezu; zalecany stosunek tych pierwiastków to 1:0,5. Jeśli ilość fosforu przekracza poziom wapnia w żywności ponad 2 razy, powstają rozpuszczalne sole, które są ekstrahowane przez krew z tkanki kostnej. Wapń przedostaje się do ścian naczyń krwionośnych, co powoduje ich kruchość, a także do tkanek nerek, co może przyczynić się do powstawania kamieni nerkowych. Dla dorosłych zalecana proporcja wapnia i fosforu w pożywieniu wynosi 1:1,5. Trudność w utrzymaniu tego stosunku wynika z faktu, że najczęściej spożywane pokarmy są znacznie bogatsze w fosfor niż w wapń. Zawarte w wielu produktach roślinnych fityna i kwas szczawiowy mają negatywny wpływ na przyswajanie wapnia. Związki te tworzą z wapniem nierozpuszczalne sole.
Badania powiązały jony miedzi z tworzeniem tętnic lub angiogenezą. Jednym z najbardziej ekscytujących odkryć, które nie zostało jeszcze w pełni zrozumiane, jest to, że pozbawienie zwierzęcia miedzi opóźnia, a nawet hamuje wzrost guzów nowotworowych. Odżywczo może to oznaczać, że miedź jest niezbędna do rozwoju mikrokrążenia.
Wiesz to
Podczas gdy cynk może być najpowszechniejszym metalem przejściowym w enzymach, mangan jest prawdopodobnie najrzadziej powszechny, po części dlatego, że kompleksy manganu z białkami są mało stabilne i łatwo dysocjują. Znane metaloenzymy manganu obejmują karboksylazę pirogronianową i dysmutazę ponadtlenkową manganu w mitochondriach oraz arginazę w cyklu mocznikowym. Mangan może również działać jako kofaktor aktywujący metal dla wielu enzymów wymagających magnezu.
dzienne zapotrzebowanie u dorosłych wapń wynosi 800 mg, a u dzieci i młodzieży - 1000 mg lub więcej.
Przy niewystarczającym spożyciu wapnia lub z naruszeniem jego wchłaniania w organizmie (przy braku witaminy D) rozwija się stan niedoboru wapnia. Następuje zwiększone wydalanie go z kości i zębów. U dorosłych rozwija się osteoporoza - demineralizacja tkanki kostnej, u dzieci zaburzona jest budowa szkieletu, rozwija się krzywica.
Cechy żywienia z brakiem magnezu
Chociaż mangan nie jest uważany za metal redoks w oparciu o jego reaktywność, może jednak występować na 6 stopniach utlenienia, z których trzy nie są obserwowane w układach biologicznych. Kobalt jest przymocowany w kwadratowym, płaskim układzie do pierścienia podobnego do pierścienia gejowskiego, ale o bardzo szczególnych cechach. W przeciwieństwie do hemu, kobalt ma 2 osiowe ligandy, które są wolne od białka, umożliwiając grupom białkowym dostęp do centralnego metalu powyżej i poniżej płaszczyzny.
Najlepszymi źródłami wapnia są mleko i przetwory mleczne, różne sery i twarogi (100-1000 mg/100 g produktu), szczypiorek, pietruszka, fasola. Znacznie mniej wapnia znajduje się w jajach, mięsie, rybach, warzywach, owocach, jagodach (20-40 mg/100 g produktu).
Magnez. Ten pierwiastek jest niezbędny do aktywności wielu kluczowych enzymów. dla metabolizmu organizmu. Magnez bierze udział w utrzymaniu prawidłowego funkcjonowania układu nerwowego i mięśnia sercowego; ma działanie rozszerzające naczynia krwionośne; stymuluje wydzielanie żółci; podnosi aktywność silnika jelit, co pomaga w usuwaniu toksyn z organizmu (w tym cholesterolu).
Dlaczego niedobór magnezu jest niebezpieczny dla kobiet w ciąży?
W jednym kompleksie oktaedrycznym jedna pozycja osiowa jest zwykle zajęta przez jeden benzimidazol, a drugą przez grupę metylową. Urządzenie jest wyjątkowe i umożliwia kobaltowi tworzenie wiązań węgiel-metal, które mogą zachodzić w dwóch różnych reakcjach. Na przykład grupę metylową można usunąć jako jon karbonowy, trzymając oba elektrony w kobalcie, który następnie powraca do mniej stabilnego.
W permutacjach pozycyjnych kobalt zachowuje tylko jeden elektron i tworzy stabilny koion 7 z uwolnieniem wolnego rodnika. Wolne rodniki są wysoce reaktywne i pokonują bariery energetyczne, które mogą utrzymywać inne reagenty. W ten sposób, Właściwości chemiczne grupy przenoszące kobalt, takie jak jony węgla lub wysoce reaktywne rodniki z centrum węgla. Oba produkty są możliwe i wyjaśniają potrzebę kobaltu jako kofaktora, aby reakcja przebiegała w mechanizmie wolnorodnikowym.
Wchłanianie magnezu jest utrudnione przez obecność fityny oraz nadmiaru tłuszczu i wapnia w pożywieniu. Dzienne zapotrzebowanie na magnez nie jest dokładnie określone; uważa się jednak, że dawka 200-300 mg/dobę zapobiega przejawom niedoboru (przyjmuje się, że wchłania się około 30% magnezu).
Przy braku magnezu wchłanianie pokarmu jest zaburzone, wzrost jest opóźniony, wapń odkłada się w ścianach naczyń krwionośnych i rozwija się szereg innych zjawisk patologicznych. U ludzi brak jonów magnezu, ze względu na charakter odżywiania, jest niezwykle mało prawdopodobny. Jednak przy biegunce mogą wystąpić duże straty tego pierwiastka; ich konsekwencje są odczuwalne, gdy do organizmu wprowadzane są płyny niezawierające magnezu. Gdy stężenie magnezu w surowicy spada do około 0,1 mmol/l może wystąpić syndrom przypominający delirium tremens: osoba w stanie półśpiączki, drżenie mięśni, skurcze mięśni nadgarstka i stopy, zwiększona pobudliwość nerwowo-mięśniowa w odpowiedzi na dźwięk, mechaniczna i bodźce wzrokowe. Wprowadzenie magnezu powoduje szybką poprawę kondycji.
Magnez jest bogaty głównie w pokarmy roślinne. Duża jego ilość zawiera otręby pszenne, różne zboża (40 - 200 mg/100 g produktu), rośliny strączkowe, morele, morele suszone, suszone śliwki. W produktach mlecznych, mięsie, rybach, makaronach, większości warzyw i owoców jest mało magnezu (20 – 40 mg/100 g).
Potas. Około 90% potasu znajduje się w komórkach. Wraz z innymi solami zapewnia ciśnienie osmotyczne; uczestniczy w przekazywaniu impulsów nerwowych; regulacja metabolizmu wody i soli; wspomaga usuwanie wody, a co za tym idzie toksyn z organizmu; utrzymuje równowagę kwasowo-zasadową środowiska wewnętrznego organizmu; uczestniczy w regulacji czynności serca i innych narządów; niezbędne do funkcjonowania wielu enzymów.
Potas dobrze wchłania się z jelit, a jego nadmiar jest szybko usuwany z organizmu wraz z moczem. Dzienne zapotrzebowanie na potas u osoby dorosłej wynosi 2000-4000 mg. Zwiększa się przy obfitym poceniu się, przy stosowaniu leków moczopędnych, chorobach serca i wątroby. Potas nie jest składnikiem niedoborowym w diecie, a przy zróżnicowanej diecie niedobór potasu nie występuje. Niedobór potasu w organizmie pojawia się, gdy upośledzona jest funkcja układu nerwowo-mięśniowego i sercowo-naczyniowego, senność, zmniejszona ciśnienie krwi, zaburzenia rytmu serca. W takich przypadkach zalecana jest dieta potasowa.
Większość potasu pochodzi z pokarmów roślinnych. Jej bogatym źródłem są morele, suszone śliwki, rodzynki, szpinak, wodorosty, fasola, groch, ziemniaki, inne warzywa i owoce (100 - 600 mg/100 g produktu). Mniej potasu znajduje się w śmietanie, ryżu, pieczywie z mąki premium (100 - 200 mg/100 g).
Sód. Sód znajduje się we wszystkich tkankach i płynach ustrojowych. Zajmuje się utrzymywaniem ciśnienia osmotycznego w płynach tkankowych i krwi; w przekazywaniu impulsów nerwowych; regulacja równowagi kwasowo-zasadowej, metabolizmu wodno-solnego; zwiększa aktywność enzymów trawiennych.
Metabolizm sodu został szeroko zbadany ze względu na jego właściwości fizjologiczne i znaczenie dla organizmu. Ten składnik odżywczy jest łatwo wchłaniany z jelit. Jony sodu powodują obrzęk koloidów tkankowych, co powoduje zatrzymywanie wody w organizmie i przeciwdziała jej uwalnianiu. Całkowita ilość sodu w płynie pozakomórkowym określa zatem objętość tych płynów. Wzrost stężenia sodu w osoczu prowadzi do uczucia pragnienia. W gorącym klimacie i podczas ciężkiej pracy fizycznej wraz z potem dochodzi do znacznego ubytku sodu i konieczne jest wprowadzenie soli do organizmu w celu uzupełnienia utraconej ilości.
Zasadniczo jony sodu dostają się do organizmu kosztem soli kuchennej - NaCl. Przy nadmiernym spożyciu chlorku sodu pogarsza się usuwanie rozpuszczalnych w wodzie końcowych produktów przemiany materii przez nerki, skórę i inne narządy wydalnicze. Retencja wody w organizmie komplikuje pracę układu sercowo-naczyniowego, podnosi ciśnienie krwi. W związku z tym spożycie soli w odpowiednich chorobach w diecie jest ograniczone. Jednak podczas pracy w gorących sklepach lub gorącym klimacie zwiększa się ilość sodu (w postaci soli kuchennej) wprowadzanego z zewnątrz, aby zrekompensować jego utratę wraz z potem i zmniejszyć pocenie się, które obciąża pracę serca.
Sód jest naturalnie obecny we wszystkich produktach spożywczych. Sposób otrzymywania produktów spożywczych w dużej mierze determinuje ostateczną zawartość w nim sodu. Na przykład mrożony zielony groszek zawiera znacznie więcej sodu niż świeży. Świeże warzywa i owoce zawierają mniej niż 10 mg/kg do 1 g/kg, w przeciwieństwie do zbóż i serów, które mogą zawierać sód w ilości 10-20 g/kg.
Oszacowanie średniego dziennego spożycia sodu z pożywienia jest trudne, ponieważ stężenie sodu w pożywieniu jest bardzo zróżnicowane, a ponadto ludzie są przyzwyczajeni do dodawania soli do żywności. Osoba dorosła spożywa do 15 g soli kuchennej dziennie i tyle samo wydala z organizmu. Ta ilość jest znacznie wyższa niż fizjologicznie konieczna i zależy przede wszystkim od smaku chlorku sodu, nawyku słonych potraw. Zawartość soli kuchennej w żywności dla ludzi można zmniejszyć do 5 g dziennie bez szkody dla zdrowia. Na uwalnianie chlorku sodu z organizmu, a co za tym idzie na jego zapotrzebowanie, wpływa ilość soli potasowych otrzymywanych przez organizm. Pokarmy roślinne, zwłaszcza ziemniaki, są bogate w potas i zwiększają wydalanie chlorku sodu z moczem, a tym samym zwiększają jego zapotrzebowanie.
Fosfor. Fosfor znajduje się we wszystkich tkankach ciała, zwłaszcza mięśniach i mózgu. Ten pierwiastek bierze udział we wszystkich procesach życiowych organizmu. : synteza i rozkład substancji w komórkach; regulacja metabolizmu; wchodzi w skład kwasów nukleinowych i szeregu enzymów; potrzebne do powstania ATP.
Fosfor występuje w tkankach organizmu i produktach spożywczych w postaci kwasu fosforowego i jego związków organicznych (fosforanów). Jego główna masa znajduje się w tkance kostnej w postaci fosforanu wapnia, reszta fosforu wchodzi w skład tkanek miękkich i płynów. W mięśniach zachodzi najintensywniejsza wymiana związków fosforu. Kwas fosforowy bierze udział w budowie cząsteczek wielu enzymów, kwasów nukleinowych itp.
Przy długotrwałym niedoborze fosforu w diecie organizm wykorzystuje własny fosfor z tkanki kostnej. Prowadzi to do demineralizacji kości i naruszenia ich struktury - rozrzedzenia. Kiedy organizm jest wyczerpany fosforem, zmniejsza się sprawność psychiczna i fizyczna, obserwuje się utratę apetytu, apatię.
Dzienne zapotrzebowanie na fosfor dla dorosłych wynosi 1200 mg. Zwiększa się wraz z dużym stresem fizycznym lub psychicznym, z niektórymi chorobami.
Duża ilość fosforu znajduje się w produktach zwierzęcych, zwłaszcza w wątrobie, kawiorze, a także w zbożach i roślinach strączkowych. Jego zawartość w tych produktach waha się od 100 do 500 mg na 100 g produktu. Zboża (płatki owsiane, kasza pęczak) są bogatym źródłem fosforu, zawierają 300-350 mg fosforu/100 g. Jednak związki fosforu są gorzej przyswajane z produktów roślinnych niż przy spożywaniu pokarmów pochodzenia zwierzęcego.
Siarka. O znaczeniu tego pierwiastka w żywieniu decyduje przede wszystkim fakt, że wchodzi on w skład białek w postaci aminokwasów zawierających siarkę. (metionina i cystyna), a także jest integralną częścią niektórych hormonów i witamin.
Jako składnik aminokwasów zawierających siarkę siarka bierze udział w procesach metabolizmu białek, a jej zapotrzebowanie gwałtownie wzrasta podczas ciąży i wzrostu ciała, czemu towarzyszy aktywne włączanie białek do powstałych tkanek, a także podczas stanów zapalnych procesy. Aminokwasy zawierające siarkę, szczególnie w połączeniu z witaminami C i E, mają wyraźne działanie przeciwutleniające. Wraz z cynkiem i krzemem siarka decyduje o stanie funkcjonalnym włosów i skóry.
Chlor. Pierwiastek ten bierze udział w tworzeniu soku żołądkowego, tworzeniu osocza, aktywuje szereg enzymów. Ten składnik odżywczy jest łatwo wchłaniany z jelit do krwi. Interesująca jest zdolność chloru do odkładania się w skórze, zatrzymywania się w organizmie przy nadmiernym spożyciu oraz wydalania z potem w znacznych ilościach. Wydalanie chloru z organizmu następuje głównie z moczem (90%) i potem.
Naruszenia w wymianie chloru prowadzą do rozwoju obrzęku, niewystarczającego wydzielania soku żołądkowego itp. Gwałtowny spadek zawartości chloru w organizmie może prowadzić do poważnego stanu, a nawet śmierci. Wzrost jego stężenia we krwi następuje z odwodnieniem organizmu, a także z naruszeniem funkcji wydalniczej nerek.
Dzienne zapotrzebowanie na chlor wynosi około 5000 mg. Chlor dostaje się do organizmu człowieka głównie w postaci chlorku sodu po dodaniu do żywności.
^
3. Pierwiastki śladowe, ich charakterystyka
Żelazo. Ten pierwiastek jest niezbędny do biosyntezy związków zapewniających oddychanie, hematopoezę; uczestniczy w reakcjach immunobiologicznych i redoks; jest częścią cytoplazmy, jąder komórkowych i szeregu enzymów.
Asymilacji żelaza zapobiegają kwas szczawiowy i fityna. Do przyswojenia tego składnika odżywczego potrzebna jest witamina B12. Kwas askorbinowy również przyczynia się do wchłaniania żelaza, ponieważ żelazo jest wchłaniane w postaci dwuwartościowego jonu.
^ Brak żelaza w organizmie może prowadzić do rozwoju anemii, wymiany gazowej, oddychania komórkowego, czyli zaburzeń podstawowych procesów zapewniających życie. Rozwojowi stanów niedoboru żelaza sprzyjają: niedostateczne spożycie żelaza w organizmie w postaci przyswojonej, zmniejszenie aktywności wydzielniczej żołądka, niedobór witamin (zwłaszcza B 12 , kwas foliowy i askorbinowy) oraz szereg chorób powodujących utratę krwi.
Zapotrzebowanie na żelazo osoby dorosłej (14 mg/dzień) jest pokrywane w nadmiarze przez normalną dietę. Jednak w przypadku stosowania w żywności chleba z mąki szlachetnej, zawierającej niewielką ilość żelaza, bardzo często obserwuje się niedobór żelaza u mieszkańców miast. Jednocześnie należy wziąć pod uwagę, że produkty zbożowe bogate w fosforany i fitynę tworzą z żelazem trudno rozpuszczalne związki i zmniejszają jego przyswajalność przez organizm.
Żelazo jest powszechnym pierwiastkiem. Występuje w podrobach, mięsie, jajach, fasoli, warzywach, jagodach. Natomiast w postaci łatwo przyswajalnej żelazo występuje tylko w produktach mięsnych, wątrobie (do 2000 mg/100 g produktu), żółtku jaja.
Miedź. Miedź jest niezbędnym elementem metabolizmu człowieka, odgrywa rolę w tworzeniu czerwonych krwinek, uwalnianiu żelaza w tkankach oraz rozwoju szkieletu, ośrodkowego układu nerwowego i tkanki łącznej.
Ponieważ miedź jest szeroko rozpowszechniona w żywności, jest mało prawdopodobne, aby ludzie, z możliwym wyjątkiem niemowląt, na diecie czysto mlecznej, kiedykolwiek rozwinęli niedożywienie związane z miedzią.
Spożycie zbyt dużych dawek miedzi przez człowieka prowadzi do podrażnienia i erozji błon śluzowych, rozległego uszkodzenia naczyń włosowatych, uszkodzenia wątroby i nerek oraz podrażnienia ośrodkowego układu nerwowego. Dzienne zapotrzebowanie na ten pierwiastek to około 2 mg. Źródłem miedzi są pokarmy takie jak wątroba, żółtko jaja, zielone warzywa.
Jod. Jod jest niezbędnym pierwiastkiem biorącym udział w tworzeniu hormonu tyroksyny. Wraz z niedoborem jodu rozwija się wole - choroba tarczycy.
Zapotrzebowanie na jod waha się od 100-150 mcg dziennie. Zawartość jodu w środkach spożywczych jest zwykle niska (4-15 µg%). Owoce morza są najbogatsze w jod. Tak więc w rybach morskich zawiera około 50 mcg/100 g, w wątrobie dorsza do 800, w wodorostach w zależności od rodzaju i terminu zbioru – od 50 mcg do 70 000 mcg/100 g produktu. Należy jednak wziąć pod uwagę, że podczas długotrwałego przechowywania i obróbki cieplnej żywności tracona jest znaczna część jodu (od 20 do 60%).
Zawartość jodu w lądowych produktach roślinnych i zwierzęcych jest silnie uzależniona od jego ilości w glebie. Na obszarach, gdzie w glebie jest mało jodu, jego zawartość w produktach spożywczych może być od 10 do 100 razy mniejsza niż średnia. Dlatego w tych obszarach aby zapobiec wola, do soli kuchennej dodaje się niewielką ilość jodanu potasu (25 mg na 1 kg soli). Okres przechowywania takiej jodowanej soli nie przekracza 6 miesięcy, ponieważ jod stopniowo zanika podczas przechowywania soli.
Fluor. Przy braku tego pierwiastka rozwija się próchnica (zniszczenie szkliwa zębów). Nadmiar fluoru ma również negatywny wpływ na organizm, ponieważ sole fluoru gromadzące się w kościach powodują zmianę koloru i kształtu zębów, osteochondrozę, a po tym zgrubieniu stawów i ich unieruchomieniu, narośla kostne. Różnica między użytecznymi a szkodliwymi dawkami fluoru jest tak mała, że wielu badaczy sprzeciwia się fluoryzacji wody.
Fluor spożywany z wodą jest wchłaniany prawie całkowicie, fluor zawarty w pożywieniu jest wchłaniany w mniejszym stopniu. Wchłonięty fluor jest równomiernie rozprowadzany po całym organizmie. Zatrzymywany jest głównie w szkielecie, a niewielka ilość odkłada się w tkance zęba. W dużych dawkach fluor może powodować zaburzenia metabolizmu węglowodanów, lipidów, białek, a także metabolizm witamin, enzymów i soli mineralnych.
W różnych krajach dokonano oszacowań dziennego spożycia fluoru z pożywienia; dla dorosłych wartość ta waha się od 0,2 do 3,1 mg, dla dzieci Grupa wiekowa od 1 roku do 3 lat spożycie fluoru oszacowano na 0,5 mg/dobę.
Prawie wszystkie produkty spożywcze zawierają co najmniej śladowe ilości tego pierwiastka. Wszystkie rodzaje roślinności zawierają pewną ilość fluoru, który pozyskują z gleby i wody. Wysoki poziom fluoru stwierdzono w niektórych produktach spożywczych, zwłaszcza w rybach, niektórych warzywach i herbacie. Stosowanie wody fluorowanej w zakładach przetwórstwa spożywczego może często podwoić poziom fluoru w gotowych produktach.
Do profilaktyki i leczenia próchnicy różne pasty do zębów, proszki, eliksiry, gumy do żucia i tym podobne, które zawierają dodany fluor, głównie w postaci nieorganicznej. Związki te są powszechnie włączane do środków do czyszczenia zębów, zazwyczaj w stężeniach około 1 g/kg.
Chrom. Pierwiastek ten wydaje się być niezbędny do metabolizmu glukozy i lipidów oraz do wykorzystania aminokwasów przez niektóre układy. On także ma znaczenie do zapobiegania łagodnym postaciom cukrzycy i miażdżycy u ludzi.
Chrom jest wchłaniany zarówno z przewodu pokarmowego, jak iz dróg oddechowych. Wchłonięta ilość nie jest jednakowa dla każdego z tych systemów i zależy od postaci chromu. Chrom trójwartościowy jest podstawową formą pierwiastka dla ludzi, chrom sześciowartościowy jest toksyczny. Chrom jest rozprowadzany w tkankach organizmu człowieka w nierównych, ale zazwyczaj niskich stężeniach. Poziom chromu we wszystkich tkankach z wyjątkiem płuc zmniejsza się wraz z wiekiem. Największe ilości chromu u ludzi gromadzą się w skórze, mięśniach i tkance tłuszczowej. Mechanizmy homeostatyczne, w tym mechanizmy transportu w wątrobie i jelitach, zapobiegają nadmiernemu gromadzeniu się chromu trójwartościowego. Chrom jest powoli wydalany z organizmu, głównie z moczem.
Dziś uważa się za normę spożycia około 150 mg chromu dziennie. Jest szczególnie przydatny dla osób starszych, których organizm nie wchłania dobrze węglowodanów, a chrom usprawnia procesy metaboliczne tych właśnie związków. Chrom nieorganiczny jest słabo wchłaniany, znacznie łatwiej – w związkach organicznych, czyli w takiej postaci, w jakiej występuje w organizmach żywych.
Produkty spożywcze różnią się znacznie zawartością chromu, która waha się od 20 do 550 µg/kg. Bogatym źródłem chromu są drożdże piwne, wątroba (10-80 mcg/100 g). W mniejszych ilościach pierwiastek ten znajduje się w ziemniakach ze skórkami, wołowinie, świeżych warzywach, pieczywie pełnoziarnistym, serze.
Mangan. Mangan jest niezbędnym kofaktorem w wielu układach enzymatycznych; odgrywa rolę w prawidłowym funkcjonowaniu flawoprotein, w syntezie siarczanowanych mukopolisacharydów, cholesterolu, hemoglobiny oraz w wielu innych procesach metabolicznych. Ze spożytego manganu wchłania się tylko około 3%.
Wchłanianie manganu jest ściśle związane z wchłanianiem żelaza. Zapotrzebowanie na mangan wynosi 0,2-0,3 mg na 1 kg masy ciała na dzień. Najwięcej manganu znajduje się w żurawinie i herbacie, nieco mniej w kasztanach, kakao, warzywach, owocach (100-200 mcg/100 g).
^ Nikiel. Nikiel został uznany za niezbędny pierwiastek śladowy stosunkowo niedawno. Obecnie ustalono jego rolę jako koenzymu w procesach metabolizmu żelaza. Jednocześnie wzrostowi spożycia żelaza w organizmie towarzyszy wzrost zapotrzebowania na nikiel pokarmowy. Ponadto nikiel przyczynia się do wchłaniania miedzi – kolejnego pierwiastka niezbędnego do hematopoezy. Znaczenie niklu spożywczego lub niklu wyizolowanego z produktów naturalnych podkreśla fakt, że syntetyczne związki tego pierwiastka są rakotwórcze.
Nikiel jest obecny w większości produktów spożywczych, ale w stężeniach poniżej (a często znacznie poniżej) 1 mg/kg. Stwierdzono, że spożycie niklu w diecie waha się od mniej niż 200 do 900 µg/dzień. Przy normalnej diecie wchodzi około 400 mcg / dzień. Wykazano, że zawartość niklu w winach i piwie wynosi odpowiednio 100 i 50 µg/L.
Cynk. Ten pierwiastek śladowy jako koenzym bierze udział w wielu reakcjach biosyntezy białek (ponad 70) i metabolizmu kwasów nukleinowych (w tym w procesach replikacji i transkrypcji DNA), które przede wszystkim zapewniają organizmowi wzrost i dojrzewanie. Jednocześnie cynk wraz z manganem jest specyficznym pierwiastkiem śladowym, który wpływa na stan funkcji seksualnych, a mianowicie na aktywność niektórych hormonów płciowych, spermatogenezę, rozwój męskich gonad oraz drugorzędowe cechy płciowe. Ponadto ostatnio rozważano rolę cynku w zapobieganiu procesom przerostowym gruczołu krokowego.
Cynk wraz z siarką bierze udział we wzroście i odnowie skóry i włosów. Wraz z manganem i miedzią cynk znacząco przyczynia się do odczuwania odczuć smakowych i zapachowych. Cynk jako niezbędny składnik wchodzi w skład cząsteczki insuliny, a jego poziom jest obniżony u pacjentów z cukrzycą. Bardzo ważne jest, aby ten pierwiastek śladowy był koenzymem dehydrogenazy alkoholowej, która zapewnia metabolizm alkoholu etylowego. Jednocześnie znacznie zmniejsza się poziom wchłaniania cynku w przewlekłym alkoholizmie. Tak zwana „nocna ślepota” (czyli upośledzone widzenie w nocy) może rozwinąć się nie tylko przy braku witaminy A, ale także cynku. Cynk wraz z witaminą B 6 zapewnia metabolizm nienasyconych kwasów tłuszczowych oraz syntezę prostaglandyn.
Cynk jest bardzo ważny dla trawienia i wchłaniania składników odżywczych. Tak więc cynk zapewnia syntezę najważniejszych enzymów trawiennych w trzustce, a także bierze udział w tworzeniu chylomikronów – cząstek transportujących, w których tłuszcze pokarmowe mogą być wchłaniane do krwi. Cynk wraz z witaminami z grupy B jest ważnym regulatorem funkcji układu nerwowego. W warunkach niedoboru cynku mogą wystąpić zaburzenia emocjonalne, niestabilność emocjonalna, drażliwość, a w bardzo ciężkich przypadkach dysfunkcja móżdżku. Wreszcie, gromadzi się coraz więcej danych na korzyść udziału cynku w procesach dojrzewania limfocytów i reakcjach odporności komórkowej.
Dzienne zapotrzebowanie na cynk to 8000-22000 mcg%. Jest całkiem zadowolona ze zwykłej diety. Średnie dzienne spożycie cynku z samą wodą pitną wynosi około 400 mcg. Zawartość cynku w produktach spożywczych zwykle waha się w granicach 150-25000 mcg%. Natomiast w wątrobie, mięsie i roślinach strączkowych sięga 3000 – 5000 mcg%. Czasami niedobór cynku może być odczuwany przez organizm dzieci i młodzieży, które nie spożywają wystarczającej ilości produktów pochodzenia zwierzęcego.
^ Selen. Nawet w połowie XX wieku. Selen nie tylko nie był brany pod uwagę przez nauki o żywieniu, ale był nawet uważany za bardzo toksyczny pierwiastek o właściwościach rakotwórczych. Jednak już w latach 60-tych. okazało się, że przy braku selenu cierpi układ sercowo-naczyniowy, co objawia się postępującą miażdżycą i osłabieniem mięśnia sercowego, aw stanach przewlekłego niedoboru selenu może rozwinąć się prawie nieuleczalna kardiomiopatia. Ostatnio na poziomie współczesne badania znajduje potwierdzenie jednej z ważnych obserwacji starożytnej medycyny chińskiej, wskazującej, że odpowiednie zaopatrzenie organizmu w selen pomaga spowolnić procesy starzenia i prowadzi do długowieczności . Warto zauważyć, że słynne lecznicze odmiany zielonej herbaty, dostarczane w celu osiągnięcia zdrowia i długowieczności w cesarskich pałacach w Starożytne Chiny, uprawiano w tych górzystych prowincjach, w glebach, których wysoka zawartość selenu jest już oznaczana nowoczesnymi metodami analitycznymi.
Po odkryciu selenu stwierdzono, że witamina E i selen działają na różne części tego samego procesu i są ściśle komplementarne, to znaczy ich aktywność przeciwutleniająca dramatycznie wzrasta, gdy są stosowane razem. Synergia obu przeciwutleniaczy jest szczególnie interesująca w kontekście działania przeciwnowotworowego. Wykazano zatem, że podawanie preparatów selenu jednocześnie z witaminą E istotnie zwiększało działanie przeciwnowotworowe w stosunku do guzów doświadczalnych.
Spożycie selenu z pokarmem zależy od warunków i charakteru przyjmowania pokarmu oraz poziomu selenu w produktach spożywczych. Warzywa i owoce są na ogół ubogim źródłem selenu, w przeciwieństwie do zbóż, produktów zbożowych, mięsa (zwłaszcza produktów ubocznych), owoców morza, które zawierają znaczne ilości selenu, zazwyczaj znacznie powyżej 0,2 mg/kg mokrej masy . Skład chemiczny Gleba i zawartość w niej selenu istotnie wpływają na ilość selenu w ziarnie, wahającą się od 0,04 mg/kg do 21 mg/kg.
Molibden. Całkowita ilość molibdenu w ciele osoby dorosłej wynosi około 7 mg. Zawartość molibdenu we krwi wynosi około 0,5 mikrograma na 100 ml. Wyższe stężenia tego pierwiastka stwierdzono u ludzi żyjących w rejonach, gdzie gleba jest najbogatsza w związki tego metalu. Tak więc w niektórych regionach Armenii odnotowano częste przypadki dny moczanowej wśród mieszkańców spożywających głównie produkty lokalne, w których stwierdzono niezwykle wysoki poziom molibdenu. Jego zawartość w diecie mieszkańców tego regionu wynosiła 10-15 mg. W innych rejonach, gdzie przypadki dny moczanowej występowały rzadziej, ludzie otrzymywali tylko 1-2 mg molibdenu dziennie z pożywienia.
Molibden jest integralną częścią wielu enzymów, takich jak oksydaza ksantynowa, oksydaza aldehydowa, oksydaza siarczanowa. Wiadomo, że molibden hamuje rozwój próchnicy.
Szacowane dzienne zapotrzebowanie na molibden wynosi 2 mcg na 1 kg masy ciała. W Rosji dzienne spożycie molibdenu wynosi 0,27 mg.
najbogatszy w molibden Różne rodzaje warzywa (takie jak rośliny strączkowe) i narządy wewnętrzne zwierząt.
Kobalt. Biologiczne działanie kobaltu znane jest od 1948 roku, kiedy naukowcy Rickes i Smith odkryli, że atom kobaltu jest centralnym elementem cząsteczki witaminy B 12. Maksymalne stężenie kobaltu w tkankach wynosi około 100 μg/kg. Całkowita zawartość kobaltu w ciele osoby dorosłej wynosi 5 mg. Osoba z jedzeniem codziennie otrzymuje 5,63-7,94 mikrogramów kobaltu, z czego 73-97% jest wchłaniane.
Średnie dzienne zapotrzebowanie na kobalt wynosi 60 mcg na 1 kg masy ciała. Uważa się, że człowiek potrzebuje kobaltu tylko w postaci cyjanokobalaminy (witamina B 12). W niektórych krajach związki kobaltu stosuje się jako dodatek do żywności do piwa w celu stabilizacji piany. Okazało się jednak, że taki dodatek był przyczyną chorób serca u konsumentów piwa. Dlatego obecnie zrezygnowano ze stosowania związków kobaltu jako dodatku do żywności.
^
4 Wpływ przetwarzania na skład mineralny żywności
Podczas przetwarzania surowców spożywczych z reguły zmniejsza się zawartość substancji mineralnych (z wyjątkiem Na, dodawanego w postaci soli spożywczej). W pokarmach roślinnych są tracone wraz z odpadami. Spada zatem zawartość szeregu makro-, a zwłaszcza mikroelementów podczas produkcji zbóż i mąki po obróbce ziarna, gdyż tych składników jest więcej w usuniętych łupinach i zarodkach niż w całym ziarnie. Analiza porównawcza skład mineralny w mące pszennej najwyższej jakości oraz mące z pełnego ziarna podano poniżej (zawartość pierwiastków podana jest w mg/100 g produktu):
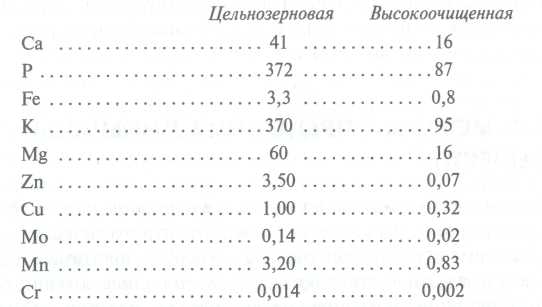
Na przykład ziarno pszenicy i żyta zawiera średnio ok. 1,7% składników popiołu, natomiast w mące, w zależności od odmiany, od 0,5 (w najwyższej jakości) do 1,5% (w mące razowej). Podczas czyszczenia warzyw i ziemniaków traci się od 10 do 30% minerałów. Jeśli są poddawane gotowaniu na gorąco, to w zależności od technologii (gotowanie, smażenie, duszenie) traci się kolejne 5 do 30%.
Mięso, produkty rybne i drób najczęściej tracą makroelementy, takie jak wapń i fosfor, podczas oddzielania miazgi od kości.
Podczas gotowania termicznego (gotowanie, smażenie, duszenie) mięso traci od 5 do 50% składników mineralnych. Jeśli jednak przetwarzanie odbywa się w obecności kości zawierających dużo wapnia, możliwe jest zwiększenie zawartości wapnia w gotowanych produktach mięsnych o 20%.
W procesie technologicznym, ze względu na niewystarczająco wysokiej jakości sprzęt, pewna ilość mikroelementów może przejść do produktu końcowego. Tak więc, robiąc chleb podczas przygotowywania ciasta w wyniku kontaktu ciasta z urządzeniami zawartość żelaza można zwiększyć o 30%. Proces ten jest niepożądany, ponieważ toksyczne pierwiastki zawarte w postaci zanieczyszczeń w metalu mogą również przedostać się do produktu wraz z żelazem. Podczas przechowywania żywności w puszkach w prefabrykowanych puszkach (czyli lutowanych) puszkach ze słabą jakością lutu lub w przypadku zerwania ochronnej warstwy lakieru, do produktu mogą przedostać się wysoce toksyczne pierwiastki, takie jak ołów, kadm i cyna.
Należy wziąć pod uwagę, że wiele metali, takich jak żelazo i miedź, nawet w niewielkich stężeniach, może powodować niepożądane utlenianie produktów. Ich zdolności katalitycznego utleniania są szczególnie wyraźne w odniesieniu do tłuszczów i produktów tłuszczowych. I tak np. przy stężeniu żelaza powyżej 1,5 mg/kg i miedzi 0,4 mg/kg podczas długotrwałego przechowywania masła i margaryn metale te powodują jełczenie produktów. Podczas przechowywania napojów w obecności żelaza powyżej 5 mg/l i miedzi 1 mg/l w pewnych warunkach często można zaobserwować zmętnienie napojów.
^
5. Metody oznaczania substancji mineralnych
Do analizy substancji mineralnych stosuje się głównie metody fizykochemiczne - optyczne i elektrochemiczne.
Niemal wszystkie te metody wymagają specjalnego przygotowania próbek do analizy, które polega na wstępnej mineralizacji przedmiotu badań. Mineralizację można przeprowadzić na dwa sposoby: „na sucho” i „na mokro”. Mineralizacja „na sucho” polega na zwęgleniu, spaleniu i kalcynowaniu próbki testowej w określonych warunkach. Mineralizacja „na mokro” przewiduje również obróbkę przedmiotu badań stężone kwasy(najczęściej HNO 3 i H 2 SO 4).
^ Spektralne metody analizy.
Fotoelektrokolorymetria - analiza oparta na pomiarze absorpcji przez kolorowe roztwory promieniowania monochromatycznego w widzialnym obszarze widma. Pomiary wykonuje się za pomocą kolorymetrów fotoelektrycznych wyposażonych w filtry wąskopasmowe. Jeżeli substancja badana nie jest zabarwiona, musi zostać przekształcona w barwny związek poprzez reakcję chemiczną z pewnymi odczynnikami (analityczna reakcja fotometryczna).
Spektrofotometria to metoda analityczna oparta na pomiarze absorpcji promieniowania monochromatycznego w zakresie ultrafioletowym, widzialnym i podczerwonym widma. Pomiary takie wykonuje się za pomocą spektrofotometrów, w których jako monochromatyzatory stosuje się pryzmaty dyspersyjne i siatki dyfrakcyjne.
Analizę ilościową badanego jonu zwykle przeprowadza się metodą krzywej kalibracyjnej.
Analiza widmowa emisji. Metody analizy widmowej emisji opierają się na pomiarze długości fali, natężenia i innych właściwości światła emitowanego przez atomy i jony substancji w stanie gazowym. Analiza spektralna emisji umożliwia określenie składu pierwiastkowego substancji nieorganicznych i organicznych.
Intensywność linii widmowej jest określona przez liczbę wzbudzonych atomów w źródle wzbudzenia, która zależy nie tylko od stężenia pierwiastka w próbce, ale również od warunków wzbudzenia. Przy stabilnej pracy źródła wzbudzenia zależność między natężeniem linii widmowej a koncentracją pierwiastka (jeśli jest wystarczająco mała) jest liniowa, tj. w ta sprawa analizę ilościową można również przeprowadzić metodą krzywej kalibracyjnej.
Największe zastosowanie jako źródło wzbudzenia otrzymał łuk elektryczny, iskra, płomień. Temperatura łuku sięga 5000 - 6000°C. W łuku można uzyskać widmo prawie wszystkich pierwiastków. Przy wyładowaniu iskrowym rozwija się temperatura 7000 - 10000 ° C i wszystkie elementy są wzbudzane. Płomień daje wystarczająco jasne i stabilne widmo emisji. Metoda analizy wykorzystująca płomień jako źródło wzbudzenia nazywana jest analizą emisji płomienia. Ta metoda oznacza ponad czterdzieści pierwiastków (ziemi alkalicznych i alkalicznych, Cu 2 , Mn 2 itp.).
^ Spektroskopia absorpcji atomowej . Metoda opiera się na zdolności swobodnych atomów pierwiastków w gazach płomieniowych do pochłaniania energii świetlnej o długości fali charakterystycznej dla każdego pierwiastka.
W atomowej spektroskopii absorpcyjnej możliwość nakładania się linii widmowych różnych pierwiastków jest prawie całkowicie wykluczona, ponieważ ich liczba w widmie jest znacznie mniejsza niż w spektroskopii emisyjnej.
Spadek natężenia promieniowania rezonansowego w warunkach atomowej spektroskopii absorpcyjnej jest zgodny z wykładniczym prawem spadku natężenia w zależności od grubości warstwy i stężenia substancji, podobnym do prawa Bouguera-Lamberta-Beera
Niezmienność grubości warstwy pochłaniającej światło (płomień) uzyskuje się za pomocą palników o specjalnej konstrukcji. Metody analizy spektralnej absorpcji atomowej są szeroko stosowane do analizy niemal każdego obiektu technicznego lub przyrodniczego, zwłaszcza w przypadkach, gdy konieczne jest oznaczenie niewielkich ilości pierwiastków.
Opracowano metody oznaczania absorpcji atomowej dla ponad 70 pierwiastków.
^ 2. Elektrochemiczne metody analizy.
Jonometria. Metoda służy do oznaczania jonów K , Na , Ca 2 , Mn 2 , F - , I - , Сl - itp.
Metoda opiera się na zastosowaniu elektrod jonoselektywnych, których membrana przepuszcza określony rodzaj jonów (stąd z reguły wysoka selektywność metody).
Zawartość ilościową oznaczanego jonu przeprowadza się albo za pomocą wykresu kalibracyjnego, który wykreśla się we współrzędnych E - pC, albo metodą dodawania. Standardowa metoda dodawania jest zalecana do oznaczania jonów w układach złożonych zawierających duże stężenia substancji obcych.
Polarografia. Metoda polarografii prądu przemiennego służy do oznaczania pierwiastków toksycznych (rtęć, kadm, ołów, miedź, żelazo).
Metoda opiera się na badaniu krzywych prąd-napięcie uzyskanych podczas elektrolizy substancji elektrooksydacyjnej lub elektroredukującej. Jako elektrodę wskaźnikową w polarografii najczęściej stosuje się rtęciową elektrodę kroplową, czasem mikroelektrody stałe - platynowe, grafitowe. Jako elektrodę odniesienia stosuje się rtęć wylewaną na dno elektrolizera lub nasyconą półogniwo kalomelowe.
Wraz ze wzrostem napięcia następuje moment, w którym wszystkie jony wchodzące do elektrody w wyniku dyfuzji są natychmiast rozładowywane, a ich stężenie w warstwie przyelektrodowej staje się stałe i praktycznie równe zeru. Prąd płynący w tym czasie w obwodzie nazywany jest ograniczającym prądem dyfuzyjnym.
Ilościowa analiza polarograficzna opiera się na wykorzystaniu bezpośredniej zależność proporcjonalna wielkość prądu dyfuzyjnego na stężenie oznaczanego pierwiastka.
^ ELEMENTY MINERALNE
Pierwiastki mineralne (popioły) występują w produktach spożywczych w postaci związków organicznych i nieorganicznych. Występują w wielu organicznych
substancje różnych klas - białka, tłuszcze, glikozydy, enzymy itp. Zazwyczaj pierwiastki mineralne są określane w popiele po spaleniu produktów spożywczych, ponieważ dość trudno jest dokładnie określić, które substancje i w jakiej ilości są zawarte.
Rola pierwiastków mineralnych w życiu ludzi, zwierząt i roślin jest ogromna: wszystkie procesy fizjologiczne w organizmach żywych przebiegają z udziałem tych pierwiastków. Tak więc w organizmie ludzkim i zwierzęcym pierwiastki mineralne biorą udział w procesach plastycznych, tworzeniu i budowie tkanek, metabolizmie wody, utrzymaniu ciśnienia osmotycznego krwi i innych płynów ustrojowych, utrzymaniu równowagi kwasowo-zasadowej w organizmie, i są zawarte w kompleksie substancji tworzących żywe komórki protoplazmy, w składzie niektórych gruczołów dokrewnych itp.
Skład mineralny organizmów zmienia się wraz z wiekiem; wraz ze starzeniem obserwuje się mineralizację organizmów. Tak więc noworodki zawierają około 34 g minerałów na 1 kg masy ciała, u osoby dorosłej zawartość tych substancji wzrasta do 43 g lub więcej.
W organizmie ludzkim i zwierzęcym znaleziono ponad 70 pierwiastków mineralnych. Wiele procesów enzymatycznych zachodzących w różnych tkankach organizmu wymaga udziału szeregu pierwiastków mineralnych. Tak więc do konwersji kwasu pirogronowego do kwasu octowego lub glukozy do fruktozy lub fosfoglicerolu do glukozo-6-mannozy-6- i fruktozo-6-fosforanu obowiązkowy jest udział jonów magnezu. Jony wapnia hamują rozwój tego procesu.
Minerały są nierównomiernie rozmieszczone w tkankach ludzkiego ciała. W tkankach twardych dominują pierwiastki dwuwartościowe: wapń (Ca) i magnez (Mg), aw tkankach miękkich pierwiastki jednowartościowe: potas (K) i sód (Na). Ponadto w tkankach twardych gromadzi się dużo fosforu (P), głównie w postaci soli fosforanowych. Przy braku minerałów w pożywieniu związki te są wydalane z organizmu i zaburzony jest normalny metabolizm.
Substancje mineralne rozpuszczone w osoczu krwi, płynach międzykomórkowych i innych płynach ustrojowych wytwarzają określone ciśnienie osmotyczne, które zależy od stężenia molowego substancji rozpuszczonych w cieczy. Sole w większym stopniu zwiększają ciśnienie osmotyczne
niż nieelektrolity przy tym samym stężeniu molowym, ponieważ sole dysocjują, tworząc jony. Ciśnienie osmotyczne zależy od całkowitej liczby niezdysocjowanych cząsteczek i jonów. Ciśnienie osmotyczne krwi, limfy i płynu międzykomórkowego organizmu ludzkiego i zwierzęcego zależy głównie od rozpuszczonego w nich chlorku sodu (NaCl).
Ciśnienie osmotyczne w płynach ustrojowych wpływa na dystrybucję wody i substancji rozpuszczonych w tkankach. U zwierząt wyższych ciśnienie osmotyczne jest stałe i wynosi 7,5-9,0 atm. Utrzymanie stałego ciśnienia osmotycznego zapewnia aktywność narządów wydalniczych, głównie nerek i gruczołów potowych.
Wnikanie soli mineralnych do krwi prowadzi do wnikania wody międzykomórkowej do krwi, a tym samym zmniejsza się stężenie soli we krwi. Nadmiar wody i soli jest następnie usuwany przez nerki. Zmniejszenie ilości wody w tkankach, działające odruchowo na ośrodki nerwowe, powoduje pragnienie.
Normalna aktywność życiowa organizmu ludzkiego może przebiegać tylko z pewnymi właściwościami płynów międzykomórkowych i śródmiąższowych. W tej niezmienności środowiska ważną rolę odgrywa równowaga kwasowo-zasadowa, w której odczyn krwi, limfy i innych płynów ustrojowych jest zbliżony do obojętnego. Równowaga kwasowo-zasadowa jest utrzymywana przez złożony system regulatory połączone w jedną centralę system nerwowy. Takimi regulatorami są układy buforowe krwi, wymiana tlenu i dwutlenku węgla, soli dwutlenku węgla i chlorków, funkcje wydalnicze nerek, płuc, gruczołów potowych itp.
W procesie złożonej przemiany w organizmie człowieka pokarmów bogatych w wapń, magnez, sód czy potas mogą powstawać związki alkaliczne. Źródła pierwiastków zasadotwórczych obejmują owoce, warzywa, rośliny strączkowe, mleko i produkty mleczne.
Inne produkty, takie jak mięso, ryby, jajka, sery, pieczywo, płatki zbożowe, makarony w procesie przemiany w organizmie człowieka dają związki kwaśne.
Charakter odżywiania może wpływać na zmiany równowagi kwasowo-zasadowej w tkankach ludzkiego ciała. Równowaga kwasowo-zasadowa często przesuwa > stronę kwasowości. W wyniku gwałtownego przesunięcia
dopuszczalnych maksymalnych norm zawartości popiołu, a przy ocenie takich produktów określają jego ilość.
Zwykle rozróżnia się dwa pojęcia - „całkowity (surowy) popiół” i „czysty popiół”. Pojęcie „popiół całkowity” oznacza sumę pierwiastków mineralnych lub ich tlenków, które wchodzą w skład struktury chemicznej produktów spożywczych, a także są wprowadzane do produktu podczas jego produkcji lub „przypadkowo wychwycone jako zanieczyszczenia”. „Czysty popiół” oznacza suma pierwiastków mineralnych lub ich tlenków bez zanieczyszczeń.
Zawartość popiołu w produkcie określa się przez spalanie. Aby to zrobić, próbka jest najpierw ostrożnie spalana, a następnie kalcynowana do stałej masy. Podwyższona ilość popiołu wbrew normie wskazuje na zanieczyszczenie produktu piaskiem, drobinkami metalu i ziemią.
Aby określić „czysty popiół”, powstały popiół traktuje się 10% kwasem solnym. W takim przypadku „czysty popiół” rozpuszcza się w kwasie solnym, a pozostałość wskaże na obecność obcych nieorganicznych zanieczyszczeń w produkcie. Tak więc w przypadku złego mycia pomidorów przed przetwarzaniem lub w skrobi ziemniaczanej, przy niewystarczającym myciu bulw, produkt atomowy zawiera zwiększoną ilość popiołu z powodu obcych zanieczyszczeń mineralnych.
Wapń w organizmie człowieka znajduje się w tkance kostnej i zębach – około 99%. Reszta wapnia dostaje się do krwi w postaci jonów oraz w stanie związanym z białkami i innymi związkami.
Dzienne zapotrzebowanie osoby dorosłej na wapń wynosi 0,8-1,0 g. Kobiety w ciąży i karmiące piersią potrzebują zwiększonych ilości wapnia, do 1,5-2 g dziennie, a także dzieci, w których organizmach wapń jest intensywnie wykorzystywany do tworzenia kości. Niedobór wapnia powoduje deformację szkieletu, kruchość kości i zanik mięśni w organizmie. Wapń charakteryzuje się tym, że nawet przy braku pożywienia jest wydalany z organizmu w znacznych ilościach.
Wapń występuje w produktach spożywczych w postaci soli fosforanowych i chlorkowo-szczawianowych, a także w połączeniu z kwasami tłuszczowymi, białkami itp.
Wszystkie związki wapnia, z wyjątkiem CaC!a, są słabo rozpuszczalne w wodzie i dlatego są słabo wchłaniane
Ciało ludzkie. Nierozpuszczalne związki wapnia częściowo przechodzą z produktów do roztworu w żołądku pod wpływem kwasu solnego sok żołądkowy. Przyswajanie wapnia z produktów spożywczych przez organizm człowieka w dużej mierze zależy od obecności w pożywieniu fosforanów, tłuszczów, związków magnezu itp. Zatem przyswajanie wapnia jest największe, gdy stosunek wapnia do fosforu I w pożywieniu ; 1,5 lub 1:2. Ilość fosforu w pożywieniu zwiększona w stosunku do wskazanych proporcji prowadzi do gwałtownego spadku wchłaniania wapnia. Nadmiar magnezu wpływa również niekorzystnie na przyswajanie wapnia przez organizm człowieka. Ostry zły wpływ przyswajanie wapnia wywierają związki wapnia z kwasem inozytolowo-fosforowym, który występuje w znacznych ilościach w ziarnach zbóż i produktach jego przetwarzania.
Witamina D odgrywa bardzo ważną rolę we wchłanianiu wapnia, co sprzyja przechodzeniu soli wapnia i fosforu z jelit do krwi i odkładaniu się w kościach w postaci fosforanu wapnia.
Zawartość wapnia w niektórych produktach spożywczych wynosi (mg%): w chudym mięsie - 7; w jajach - 54; w mleku - 118; w serze - 930; w twarogu - 140; w płatkach owsianych - 65; w mące pszennej - 15; w ryżu - 9; w jabłkach - 7; w pomarańczach - 45; w orzechach włoskich -89; w burakach - 29; w kalafiorze - 89; w białej kapuście - 45; w marchwi - 56; w ziemniakach - 14. Z powyższych danych wynika, że najważniejszym źródłem wapnia dla człowieka są produkty mleczne. Wapń w produktach mlecznych, a także warzywach i owocach jest związkiem łatwo przyswajalnym.
Magnez w organizmie człowieka jest 30-35 razy mniejszy niż wapń, ale jest bardzo ważny. Większość magnezu znajduje się w tkance kostnej. Magnez odgrywa szczególną rolę w roślinach chlorofilowych, gdzie jest częścią cząsteczki chlorofilu. Podobnie jak wapń, magnez tworzy trudno rozpuszczalne związki. Magnez jest szczególnie trudny do przyswojenia w obecności jonu LO$.
Zawartość magnezu w niektórych produktach spożywczych kształtuje się następująco (mg%): w fasoli – 139; w płatkach owsianych - 133; w grochu - 107; w prosie - 87; w chlebie pszennym - 30; w ziemniakach - 28; w marchwi - 21; w białej kapuście -!Anna - 12; w jabłkach - 8; w cytrynach - 7; w wołowinie - 15; w jajkach - 11; w mleku - 12. W konsekwencji 2 * 35 magnezu znajduje się w największych ilościach w ziarnach i roślinach strączkowych.
Zapotrzebowanie na magnez dla osoby dorosłej wynosi 400 mg dziennie.
Sód jest powszechnie obecny w żywności, zwłaszcza w produktach pochodzenia zwierzęcego. Głównym źródłem sodu dla organizmu człowieka jest NaCt (sól kuchenna). Sód odgrywa ważną rolę w procesach metabolizmu wewnątrzkomórkowego i międzytkankowego. Około 90% ciśnienia osmotycznego osocza krwi zależy od zawartości w nim NaCl. Zazwyczaj 3,3 g sodu rozpuszcza się w litrze ludzkiego osocza krwi. NaC! Odgrywa również ważną rolę w regulowaniu metabolizmu wody w organizmie. Jony sodu powodują obrzęk koloidów tkankowych i tym samym przyczyniają się do zatrzymywania związanej wody w organizmie. Z ciała NaC! wydalany głównie z moczem i potem. Przy wzmożonej pracy i spożyciu płynów osoba traci do 3-5 litrów potu, czyli 99,5% wody. W suchej masie potu główną częścią jest NaGI.
Sól kuchenna, która dostaje się do organizmu człowieka wraz z pożywieniem, uzupełnia zużycie NaCl we krwi i służy do tworzenia kwasu solnego w soku żołądkowym, a także do syntezy NaHCO3 przez gruczoł trzustkowy. Obecność NaHCO3 wyjaśnia alkaliczny odczyn soku trzustkowego, który jest niezbędny do rozkładu białek pokarmowych przez enzym trypsynę.
Dzienne zapotrzebowanie osoby dorosłej na sód wynosi 4-6 g, co odpowiada 10-15 g soli kuchennej. Zwykłe diety ludności zawierają wystarczającą ilość sodu, ponieważ sól kuchenna jest dodawana do żywności.
Potas jest stale iw znacznych ilościach obecny w produktach spożywczych, zwłaszcza pochodzenia roślinnego.W popiołach roślinnych zawartość potasu czasami przekracza 50% jego masy.
W organizmie człowieka potas bierze udział w reakcjach enzymatycznych, tworzeniu układów buforowych, które zapobiegają zmianom reakcji środowiska. Zmniejsza potas
Zdolność białek do zatrzymywania wody, zmniejszająca ich hydro-(zdolność), a tym samym sprzyja wydalaniu wody i sodu z organizmu, dlatego potas można uznać za pewnego fizjologicznego antagonistę sodu.
Dzienne zapotrzebowanie osoby dorosłej na potas wynosi 3-5 g.
Żelazo jest szeroko rozpowszechnione w przyrodzie. Ogólnie rzecz biorąc, prawie wszystkie naturalne produkty spożywcze zawierają żelazo, ale w niewielkich ilościach.
W organizmach ludzkich i zwierzęcych żelazo jest częścią najważniejszych związków organicznych - hemoglobiny we krwi, mioglobiny, niektórych enzymów - katalazy, peroksydazy, oksydazy cytochromowej itp. Hemoglobina we krwi zawiera 2A, żelazo organizmu. Znaczna ilość żelaza znajduje się w śledzionie i wątrobie. Żelazo ma zdolność gromadzenia się w organizmie. Hemoglobina we krwi ulega zniszczeniu podczas życia, a uwolnione w tym przypadku żelazo może zostać ponownie wykorzystane przez organizm do wytworzenia hemoglobiny.
Żelazo, które jest częścią owoców i warzyw, jest dobrze przyswajalne przez organizm człowieka, podczas gdy większość żelaza w produktach zbożowych jest w formie niestrawnej dla organizmu.
Dzienne zapotrzebowanie dorosłego ludzkiego gruczołu wynosi 15 mg.
l l lub r jest częścią żywności naturalnej w niewielkich ilościach. Produkty roślinne zawierają mało chloru, natomiast produkty zwierzęce zawierają nieco więcej. Tak więc zawartość chloru w wołowinie wynosi 76 mg%, w mleku - 106, w jajach -
37106, w serze - 880, w prosie - 19, w ziemniakach - 54, w jabłkach - 5 mg%.
Zawartość chloru jest znacząca we krwi i innych płynach ustrojowych, a także w skórze, płucach i nerkach. Chlor w organizmie jest w stanie zjonizowanym w postaci anionów soli sodu, potasu, wapnia, magnezu, manganu. Związki chloru w produktach spożywczych są dobrze rozpuszczalne i łatwo wchłaniane w jelicie człowieka. Aniony chloru wraz z kationami sodu odgrywają ważną rolę w tworzeniu i regulacji ciśnienia osmotycznego krwi i innych płynów ustrojowych. Sole chloru zapewniają tworzenie kwasu solnego przez błonę śluzową żołądka.
Główne zapotrzebowanie na chlor zaspokaja chlorek sodu, który dodawany jest do żywności w postaci soli.
Całkowita ilość chlorku sodu w organizmie człowieka wynosi zwykle 10-15 g, ale podczas spożywania pokarmów bogatych w sole chloru zawartość chloru w organizmie człowieka może osiągnąć wyższą ilość. Dzienne zapotrzebowanie człowieka na chlor wynosi 5-7 g.
Siarka występuje w największych ilościach w produktach zbożowych, roślinach strączkowych, produktach mlecznych, mięsie, rybach, a zwłaszcza jajach. Wchodzi w skład prawie wszystkich białek ludzkiego organizmu i jest szczególnie bogata w aminokwasy – cystynę, metioninę. Wymiana siarki w organizmie to głównie jej przekształcenie we wskazane aminokwasy. Bierze również udział w tworzeniu witaminy Bg (tiaminy), insuliny i niektórych innych związków. Dużo siarki znajduje się w proteinoidach tkanek podporowych, na przykład w keratynie włosów, paznokci itp.
Kiedy związki ulegają utlenieniu w organizmie, znaczna część siarki jest wydalana z moczem w postaci soli kwasu siarkowego.
Dzienne zapotrzebowanie osoby dorosłej na siarkę przy umiarkowanej pracy wynosi około 1 g.
Jod zawarty jest w organizmie zdrowej osoby ważącej 70 kg w ilości około 25 mg. Połowa tej ilości znajduje się w tarczycy, a reszta w tkankach mięśniowych i kostnych oraz we krwi. Jod związków nieorganicznych w tarczycy jest zastępowany przez związki organiczne – tyroksynę, dijodotyroksynę, trijodotyroksynę. Jod jest szybko wchłaniany przez tarczycę i kilka godzin po dostaniu się do niego zamienia się w organiczny
znajomości. Związki te stymulują procesy metaboliczne w organizmie. Gdy niedostateczna ilość jodu dostanie się do organizmu wraz z pożywieniem, czynność tarczycy zostaje zaburzona i rozwija się poważna choroba zwana wole endemicznym.
Najwięcej jodu znajduje się w produktach roślinnych i zwierzęcych obszarów przybrzeżnych, gdzie koncentruje się w wodzie morskiej, powietrzu i glebie obszarów przybrzeżnych. Niewiele jodu kumuluje się w roślinach i organizmach zwierzęcych górskich lub oddalonych od wybrzeża morskiego rejonach jodu.
Zawartość jodu w produktach zbożowych, warzywach, rybach słodkowodnych nie przekracza 5-8 mcg na 100 g surowca. Wołowina, jajka, masło, owoce wyróżniają się wyższą zawartością jodu. jarmuż morski, ryby morskie i olej rybny zawierają najwięcej jodu. Owoce Feijoa rosnące na wybrzeżu Morza Czarnego w Gruzji gromadzą do 390 mikrogramów jodu na 100 g masy owocowej, czyli znacznie więcej niż zawartość tego pierwiastka w innych owocach i warzywach.
Tam, gdzie produkty spożywcze zawierają niewystarczające ilości jodu, do soli kuchennej dodaje się jodek potasu w ilości 25 g K1 na tonę soli kuchennej. Przy normalnej diecie osoba spożywa 200 mikrogramów jodu dziennie z solą jodowaną. Jednak podczas przechowywania soli jodowanej jod stopniowo zanika, dlatego po 6 miesiącach sól jodowana jest sprzedawana jako zwykła sól kuchenna.
Dzienne zapotrzebowanie człowieka na jod wynosi 100-260 mcg.
Fluor odgrywa ważną rolę w procesach plastycznych podczas tworzenia tkanki kostnej i szkliwa zębów. Najwięcej fluoru jest skoncentrowane w kościach - 200-490 mg/kg i zębach - 240-560 mg/kg.
Woda wydaje się być głównym źródłem fluoru w ludzkim ciele, przy czym fluor Dody jest lepiej wchłaniany niż fluor spożywczy. Zawartość fluoru w wodzie pitnej waha się od 1 do 1,5 mg/l. Brak fluoru w wodzie często wpływa na
39nne do rozwoju choroby zębów, zwanej próchnicą. Nadmiar fluoru w wodzie powoduje fluorozę, w której zaburzona jest normalna struktura zębów, pojawiają się przebarwienia na szkliwie i wzrasta kruchość zębów. Dzieci szczególnie cierpią na niedobór lub nadmiar fluoru.
Codzienne zapotrzebowanie człowieka na fluor nie zostało jeszcze ustalone. Uważa się, że optymalna dla zdrowia ilość fluoru w wodzie pitnej powinna wynosić 0,5-1,2 mg/l.
Miedź w organizmie zwierzęcia wraz z żelazem odgrywa ważną rolę w procesach hematopoezy, stymuluje procesy oksydacyjne i tym samym jest związana z metabolizmem żelaza. Jest częścią enzymów (laktazy, oksydazy askorbinianowej, oksydazy cytochromowej itp.) jako składnik metaliczny.
W roślinach miedź wzmaga procesy oksydacyjne, przyspiesza wzrost i zwiększa plony wielu upraw.
W tych niewielkich ilościach, w których miedź znajduje się w produktach naturalnych, nie szkodzi ludzkiemu organizmowi. Ale podwyższone ilości miedzi mogą powodować zatrucie. Tak więc jednoczesne przyjmowanie 77-120 mg miedzi może powodować nudności, wymioty, a czasem biegunkę. Dlatego zawartość miedzi w produktach spożywczych regulują aktualne przepisy Ministerstwa Zdrowia ZSRR. Na 1 kg produktu, w zależności od zawartości w nim ciał stałych, dopuszcza się od 5 do 30 mg miedzi. Tak więc w skoncentrowanej paście pomidorowej zawartość miedzi nie powinna przekraczać 30 mg / kg, w przecierze pomidorowym - 15-20, w warzywach konserwowych - 10, w dżemie i marmolady - 10, w kompotach owocowych - 5 mg / kg.
Miedź może dostać się do produktów spożywczych podczas ich produkcji - z miedzianych części sprzętu, podczas traktowania winnic pestycydami zawierającymi miedź itp.
Dzienne zapotrzebowanie osoby dorosłej na miedź wynosi 2 mg.
Cynk znajduje się we wszystkich tkankach zwierząt i roślin. Przy braku cynku w organizmach młodych kobiet,
U roślin ich wzrost jest opóźniony, a wraz z jego niedoborem w glebie dochodzi do chorób wielu roślin, co często prowadzi do ich śmierci.
Cynk wchodzi w skład wielu enzymów, a jego rola w cząsteczce enzymu anhydrazy węglanowej, która bierze udział w wiązaniu i wydalaniu dwutlenku węgla z organizmu zwierzęcia, jest szczególnie ważna. Cynk jest niezbędny do prawidłowego funkcjonowania hormonów przysadki, nadnerczy i trzustki. Wpływa również na metabolizm tłuszczów, zwiększając ich rozkład i zapobiegając stłuszczeniu wątroby.
Cynk w żywności w dużych ilościach może powodować zatrucie. Żywność kwaśna i tłusta rozpuszcza metaliczny cynk, dlatego gotowanie lub przechowywanie żywności w sprzęcie lub naczyniach cynkowych jest niedopuszczalne. Zatrucie cynkiem jest podobne do zatrucia miedzią, ale bardziej wyraźne i towarzyszy mu pieczenie i ból w jamie ustnej i żołądku, wymioty, biegunka i osłabienie serca. Przybory cynkowe są dozwolone tylko do przechowywania zimnej wody pitnej, ponieważ w tym przypadku rozpuszczalność cynku jest znikoma.
Dzienne zapotrzebowanie osoby dorosłej na cynk wynosi 10-15 mg. Podczas wzrostu i dojrzewania obserwuje się zwiększone zapotrzebowanie na cynk. Przy normalnej diecie osoba otrzymuje wystarczającą ilość cynku z pożywienia.
Ołów znajduje się w produktach pochodzenia zwierzęcego i roślinnego w bardzo małych ilościach. Tak więc w jabłkach, gruszkach, winogronach, truskawkach zawartość ołowiu wynosi około 0,1 mg na 1 kg produktu, w mleku - 0,8, w mięsie - 0,05, u jesiotra - 0,06 mg na 1 kg.
Ołów jest metalem toksycznym dla ludzi, ma zdolność gromadzenia się w organizmie, głównie w wątrobie i wywoływania ciężkich przewlekłych zatruć.
Przy codziennym stosowaniu 2-4 mg ołowiu z jedzeniem po kilku miesiącach można wykryć oznaki zatrucia ołowiem.
41 Zanieczyszczenie żywności ołowiem może pochodzić z naczyń, lutów, glazury, sprzętu i środków owadobójczych zawierających ołów. Najczęściej do zatrucia ołowiem dochodzi, gdy żywność jest przechowywana w rzemieślniczych naczyniach ceramicznych, które nie są dobrze pokryte szkliwem ołowiowym.
Ze względu na wysoką toksyczność nie dopuszcza się zawartości ołowiu w produktach spożywczych.
Cyna występuje w produktach spożywczych w niewielkich ilościach. Tak więc 0,14 mg/kg cyny znaleziono w wątrobie byka i barana, 0,003 w nerkach, 0,63 w płucach i 0,019 mg/kg w mózgu.
Cyna nie jest tak toksycznym metalem jak ołów, cynk lub miedź, dlatego jest dozwolona w ograniczonych ilościach w wyposażeniu przedsiębiorstw spożywczych, a także do cynowania powierzchni cyny, z której przygotowywane są cynowe puszki, chroniąc ją przed korozją. Jednak często podczas długotrwałego przechowywania konserw w puszkach masa produktu oddziałuje z powłoką cyny cyny, w wyniku czego powstają sole cyny kwasów organicznych. Proces ten jest szczególnie aktywny, gdy w puszce znajdują się produkty o wysokiej kwasowości – owoce, konserwy rybne i warzywa sos pomidorowy i inne Podczas długotrwałego przechowywania zawartość cyny w żywności w puszkach może znacznie wzrosnąć. Zawartość cyny wzrasta szczególnie szybko w produktach, które znajdują się w otwartych metalowych puszkach pokrytych cyną.
Aby wzmocnić ochronę puszki przed korozją, na powierzchnię cyny nakłada się dodatkowo specjalne kwasoodporne lakiery lub emalię lub na powierzchni cyny tworzy się cienka warstwa stabilnych tlenków cyny.
Mangan jest szeroko rozpowszechniony w produktach pochodzenia zwierzęcego i roślinnego. Bierze czynny udział w tworzeniu wielu enzymów, tworzeniu kości, procesach hematopoezy oraz stymuluje wzrost. W roślinach mangan wzmaga proces fotosyntezy i tworzenia kwasu askorbinowego.
Produkty roślinne są w większości przypadków bogatsze w mangan niż produkty pochodzenia zwierzęcego. Tak więc zawartość manganu w produktach zbożowych sięga 1-15 mg na 1 kg w liściu
warzywa - 10-20, owoce - 0,5-1, mleko - 0,02-0,03, jaja - 0,1-0,2, w wątrobie zwierząt - 2,65-2,98 mg na 1 kg.
Przy braku manganu w glebie rośliny chorują i słabo się rozwijają, zmniejsza się plon owoców, warzyw i innych upraw. Dodanie do gleby mikronawozów zawierających mangan pomaga zwiększyć plon.
Dzienne zapotrzebowanie osoby dorosłej na mangan wynosi 5-10 mg dziennie.
Izotopy promieniotwórcze są obecne w ludzkim ciele, stale wchodzą i wychodzą z ciała. Istnieje równowaga między przyjmowaniem związków radioaktywnych do organizmu a ich usuwaniem z organizmu. Wszystkie produkty spożywcze zawierają radioaktywne izotopy potasu (K40), węgla (C14), wodoru (H3), a także rad wraz z produktami jego rozpadu.
Najwyższe stężenie przypada na potas (K40). Izotopy uczestniczą w metabolizmie wraz z nieradioaktywnymi.
Uważa się, że w najbliższym czasie geologicznym nie było dużych zmian w natężeniu promieniowania na Ziemi, a zatem u zwierząt i flora rozwinął rodzaj odporności na te poziomy promieniowania. Ale żywe organizmy są bardzo wrażliwe na podwyższone stężenia. Małe stężenia zwiększają wzrost organizmów żywych, duże stężenia powodują pojawienie się aktywnych rodników, w wyniku czego dochodzi do naruszenia czynności życiowych poszczególnych narządów i tkanek, a także całego organizmu.
Na wybuchy atomowe Izotopy radioaktywne opadają na powierzchnię Ziemi, zanieczyszczając atmosferę, wodę, glebę i rośliny. Poprzez żywność, atmosferę i wodę izotopy promieniotwórcze dostają się do ludzkiego ciała.
Ustalono, że gdy produkty spożywcze są poddawane działaniu promieniowania izotopów radioaktywnych, ich okres przydatności do spożycia wydłuża się, a kiełkowanie ziemniaków jest opóźnione. Zwykle jednak napromieniowana żywność może mieć specyficzny zapach i smak i możliwe jest tworzenie się substancji toksycznych. Aby określić bezpieczeństwo takich produktów, wymagane są długoterminowe eksperymenty.
pytania testowe
Jakie pierwiastki chemiczne to makroelementy?
Jakie funkcje pełnią minerały w ludzkim ciele?
Jaka jest rola wapnia w organizmie człowieka?
Jakie pierwiastki chemiczne zaliczane są do pierwiastków śladowych i jakie są ich funkcje w organizmie człowieka?
Jaką rolę odgrywa żelazo w ludzkim ciele iw jakiej żywności się znajduje?
Jakie są konsekwencje niedoboru jodu w organizmie i jak można tego uniknąć?
Jakie rodzaje przetwarzania technologicznego surowców i produktów spożywczych przyczyniają się do utraty minerałów?
Podaj przykłady interakcji niektórych mikroelementów i witamin.
Jakie znasz metody oznaczania zawartości makro- i mikroelementów?
Len Kukushkin rozmnaża się: przez zoospory;
nasiona w niesprzyjających warunkach;
sprzeczanie się; +
aplanospory.
- liście truskawki:
niesparowane pierzaste;
potrójny; +
trójskładnikowe, jednoskrzydłowe;
złożona jednolistna. Pszczoły robotnice to:
osoby bezpłciowe;
samice z niedorozwiniętymi narządami rozrodczymi; +
samce z niedorozwiniętymi narządami rozrodczymi;
samce i samice z normalnie rozwiniętymi narządami rozrodczymi, ale czasowo nie rozmnażającymi się. Trawienie w polipach koralowych:
tylko wnęka;
tylko wewnątrzkomórkowe;
brzuszne i wewnątrzkomórkowe; +
jama, wewnątrzkomórkowa i zewnętrzna. Mięczaki pteropodów, które mają zdolność świecenia w ciemności, mogą być częścią:
bentos;
neuston;
fitoplankton;
zooplankton. + Cykl rozwoju Blowfly został po raz pierwszy opisany przez:
Antona Levenguka;
Francesco Redi; +
Henri Fabre;
Ludwika Pasteura. Gąsienice motyli mają:
trzy pary nóg piersiowych;
trzy pary nóg piersiowych i pięć par fałszywych nóg brzusznych; +
osiem par fałszywych nóg;
brakuje kończyn. Układ krążenia lancetu:
otwarty;
zamknięty, jest jeden krąg krążenia krwi; +
zamknięte, są dwa kręgi krążenia krwi;
zaginiony. Wybierz poprawne zdania:
- Wybierz poprawne zdania:
- W cyklostomach przewód pokarmowy ma:
kształt prostej rurki;
odrost wątroby;
wyrostki odźwiernika;
zawór spiralny. + Z ryb z Zakonu Jesiotrów nie jest widok mijania:
bieługa;
jesiotr gwiaździsty;
sterlet; +
jesiotr. Gruczoły ślinowe podczas ewolucji kręgowców po raz pierwszy pojawiają się w:
ryby dwudyszne;
płazy; +
Gady;
ssaki. Spośród ryb z rzędu dorsza żyje i składa tarło tylko w słodkiej wodzie:
dorsz;
plamiak;
miętus; +
mintaja. Pochodzenie skrzydła ptaka ze swobodnej kończyny przedniej charakterystycznej dla czworonożnych kręgowców wyraźnie ilustruje przykład piskląt:
struś;
kiwi;
hoacyna; +
pingwin. O właściwościach aerodynamicznych ptaka w locie nie wpływają pióra:
koła zamachowe;
puchaty; +
sterowniczy;
kontur. Wśród ptaków widzenie stereoskopowe jest najbardziej rozwinięte u gatunków:
owadożerne;
ziarnożerne;
mięsożerny; +
roślinożerny.
Glikokaliks komórek zwierzęcych tworzy:
białka i lipidy;
białka i nukleotydy;
białka i węglowodany; +
węglowodany i nukleotydy.
Proces, w którym ameba czerwonkowa pochłania czerwone krwinki:
osmoza;
pinocytoza;
fagocytoza; +
ułatwiona dyfuzja.
Szczątki pitekantropa po raz pierwszy odkryto w:
Afryka Południowa;
Australia;
Azja centralna;
Azja Południowo-Wschodnia. +
Najstarszym z wymienionych kopalnych przodków człowieka jest:
neandertalczyk;
Pitekantropus;
Australopitek; +
Cro-Magnon.
Organelle znajdujące się w komórkach zarówno prokariontów, jak i eukariontów:
retikulum endoplazmatyczne;
mitochondria;
lizosomy;
rybosomy. +
Głównymi składnikami eukariotycznej chromatyny jądrowej są:
DNA i RNA;
RNA i białka;
DNA i białka; +
DNA i lipidy. mikrotubule nie dostarczaj:
utrzymanie kształtu komórki;
zmiana kształtu komórki; +
ruch organelli;
ruch chromosomów podczas podziału komórki. Białka komórkowe przeznaczone do sekrecji są sortowane i pakowane w:
lizosomy;
endosomy;
retikulum endoplazmatyczne;
trans sieci Golgiego. +
Lokalizacja enzymu syntetazy ATP w mitochondriach to:
matryca;
przestrzeń międzybłonowa;
zewnętrzna męmbrana;
wewnętrzna membrana. +
Utlenianie związków organicznych do CO 2 w mitochondriach następuje:
w matrycy; +
w przestrzeni międzybłonowej;
na zewnętrznej membranie;
na wewnętrznej membranie.
Antykodon zawiera:
jeden nukleotyd;
dwa nukleotydy;
trzy nukleotydy; +
cztery nukleotydy.
Ostatecznym akceptorem elektronów w oddychaniu komórkowym jest:
NADH;
woda;
tlen; +
ATP.
Właściwość kodu genetycznego, która zwiększa niezawodność przechowywania i przekazywania informacji genetycznej:
tryplet;
uniwersalność;
nadmierność; +
brak znaków interpunkcyjnych.
Jony magnezu wchodzą w skład:
hemoglobina;
insulina;
chlorofil; +
tyroksyna. Cząsteczki RNA zdolne do wykazywania aktywności katalitycznej nazywane są:
rybonukleazy;
rybosomy;
rybozymy; +
rybonukleotydy. Związki makroergiczne nazywane są:
charakteryzuje się obecnością wiązań kowalencyjnych o wysokiej energii;
w niszczeniu niektórych wiązań, w których uwalniana jest duża ilość darmowej energii; +
którego synteza zachodzi przy wydatku dużej ilości energii;
które wydzielają dużo ciepła po spaleniu.
W procesie fotosyntezy źródłem tlenu jako produktu ubocznego jest:
bisfosforan rybulozy;
glukoza;
woda; +
dwutlenek węgla.
Rozwój bakterii nitryfikacyjnych prowadzi do:
zakwaszenie środowiska; +
alkalizacja środowiska;
neutralizacja środowiska;
nie wpływa na pH podłoża.
Acidophilus powstaje w wyniku fermentacji mleka:
bakterie kwasu mlekowego; +
drożdże;
mieszana kultura bakterii kwasu mlekowego i drożdży;
mieszana kultura bakterii kwasu mlekowego i kwasu propionowego.
Spośród tych chorób wywoływany jest przez wirus:
cholera;
ospa; +
plaga;
malaria.
Spośród składników komórek roślinnych wirus mozaiki tytoniu infekuje:
mitochondria;
chloroplasty; +
jądro;
wakuole.