เกลือแร่ให้ เนื้อเยื่อกระดูกความแข็งแกร่งความแข็งแกร่ง ปริมาณเกลือแร่ที่เพิ่มขึ้นและลดลงในเนื้อเยื่อกระดูกทำให้คุณสมบัติความแข็งแรงของมันลดลง ในเด็ก การทำให้เนื้อเยื่อกระดูกมีแร่ธาตุไม่เพียงพอทำให้การเจริญเติบโตของกระดูกท่ออ่อนยากขึ้น ซึ่งนำไปสู่ความโค้งของกระดูก มีแร่ธาตุไม่เพียงพอ อิทธิพลเชิงลบเกี่ยวกับความแข็งแรงของกระดูกและในวัยผู้ใหญ่
ด้วยเกลือแร่ที่มากเกินไปเนื้อเยื่อกระดูกจะเปราะความแข็งแรงลดลงอย่างมาก
กรดและเกลือที่ละลายน้ำได้ในร่างกายจะอยู่ในรูปไอออไนซ์ ของไพเพอร์เนื้อหาของไอออน Na + , K + , Ca 2+ , Mg 2+ , Zn 2+ , Fe 3+ , Fe 2+ จะสูงสุด Zn 2+ , Ni 2+ , Cr 3+ , Mn 2+ , Cd 2+ , Ba 2+ , Cu 2+ , Co 2+ , Mo 2+ และไอออนโลหะอื่นๆ มีอยู่ในปริมาณที่น้อยกว่ามาก เนื่องจากมีเนื้อหาในร่างกายต่ำ ไอออนเหล่านี้จึงเรียกว่าธาตุ
ของประจุลบ กรดคาร์บอนิก กรดไฮโดรคลอริก และกรดฟอสฟอริกที่ตกค้างที่เป็นกรดมีอยู่อย่างแพร่หลายที่สุด ประจุลบของกรดซัลฟิวริกมีอยู่ในปริมาณที่น้อยกว่ามาก
ไอออนสามารถเป็นได้ทั้งในสภาวะอิสระและในสถานะที่ถูกผูกมัดในองค์ประกอบของสารประกอบต่างๆ ของร่างกาย หน้าที่ของไอออนอิสระและไอออนที่ถูกผูกไว้แตกต่างกัน ไอออนกำหนดความดันออสโมติกของของเหลวชีวภาพ สร้างศักย์ไฟฟ้าของเยื่อหุ้มเซลล์ ให้การก่อตัวและการส่งผ่านของแรงกระตุ้นของเส้นประสาท ทำหน้าที่เป็นตัวกระตุ้น ปัจจัยร่วมหรือส่วนประกอบของเอนไซม์และสารประกอบทางชีวภาพอื่นๆ
ให้เราอาศัยรายละเอียดเพิ่มเติมเกี่ยวกับเนื้อหาและบทบาทของไอออนแต่ละตัวในร่างกาย
แคลเซียมไอออนแคลเซียมไอออนพบได้ทั้งในเลือดและในเซลล์ของร่างกาย ปริมาณ Ca 2+ ในเลือดอยู่ที่ประมาณ 5.7 มก.% (5.7 มก. ต่อ 100 มล. ของเลือด) มีการกระจายอย่างไม่สม่ำเสมอระหว่างพลาสมาและองค์ประกอบที่เกิดขึ้น เม็ดเลือดแดงประกอบด้วยประมาณ 1.0 มก.% เม็ดเลือดขาว - ประมาณ 4.0-5.0 มก.% ในเลือดความเข้มข้นของแคลเซียมสูงขึ้นอย่างเห็นได้ชัด
ในเซลล์ของร่างกาย แคลเซียมมีการแปลเป็นภาษาท้องถิ่นเป็นหลักในไมโทคอนเดรีย ซาร์โคพลาสมิก เรติคูลัม และไรโบโซม
แคลเซียมไอออนกระตุ้นการทำงานของเซลล์เม็ดโลหิตขาว เพิ่มความต้านทานของร่างกายต่อการติดเชื้อและอาการมึนเมา ลดการซึมผ่านของเส้นเลือดฝอย จึงมีฤทธิ์ต้านการอักเสบและป้องกันอาการแพ้ พวกเขาทำให้ความตื่นเต้นง่ายของระบบประสาทส่วนปลายกระตุ้นการทำงานของระบบประสาทขี้สงสาร มาก บทบาทสำคัญแคลเซียมไอออนเล่นกันของการกระตุ้นด้วยการหดตัวในกล้ามเนื้อหัวใจและโครงร่าง
ซึ่งไม่จำกัดเฉพาะบทบาทของแคลเซียมไอออนในร่างกาย พวกเขาเป็นส่วนหนึ่งของเยื่อหุ้มเซลล์เพื่อให้เกิดความเสถียรมีส่วนร่วมในการส่งผ่านแรงกระตุ้นของเส้นประสาทไซแนปติกและเป็นตัวควบคุมการทำงานของเอนไซม์หลายชนิด แคลเซียมไอออนมีความจำเป็นต่อการทำงานของต่อมไร้ท่อจำนวนหนึ่ง (ต่อมใต้สมอง, ต่อมหมวกไต), ต่อม ระบบทางเดินอาหาร. พวกเขามีส่วนร่วมในกระบวนการแข็งตัวของเลือด
ไอออน Na + และ K +คุณค่าของโซเดียมไอออนในร่างกายสูงมาก Na + ion เป็นไอออนหลักในพลาสมาเลือดและของเหลวนอกเซลล์ พวกเขามีบทบาทสำคัญในการรักษาสมดุลของน้ำในร่างกายมนุษย์ เนื้อหาของโซเดียมไอออนในร่างกายเป็นตัวกำหนดปริมาตรของของเหลว (น้ำ) และการละเมิดใดๆ ในการเผาผลาญจะนำไปสู่การแจกจ่ายซ้ำ การกักเก็บ หรือการสูญเสียน้ำในทันที
ความเข้มข้นของโซเดียมไอออนในตัวกลางที่เป็นของเหลวของร่างกายเป็นปัจจัยที่ส่งผลต่อการทำงานของเอนไซม์บางชนิด โดยเฉพาะอย่างยิ่ง เอ็นไซม์ของการเปลี่ยนแปลงแบบไม่ใช้ออกซิเจนของคาร์โบไฮเดรต เช่นเดียวกับเอ็นไซม์ที่กักเก็บพลังงานในสารประกอบฟอสเฟตระดับมหภาค
การขาดโซเดียมนำไปสู่ความผิดปกติหลายอย่างในร่างกาย: เนื้อเยื่อขาดน้ำ การไหลเวียนโลหิตถูกรบกวน สูญเสียความอยากอาหาร และความสามารถทางจิตลดลง ความผิดปกติทั้งหมดเหล่านี้โดยส่วนใหญ่ไม่ได้เกิดจากการขาดเกลือ (แหล่งหลักของโซเดียมและคลอรีนสำหรับร่างกาย) ในอาหาร แต่เกิดจากการสูญเสียครั้งใหญ่ในสภาวะและโรคบางอย่าง เช่น อาเจียน ท้องร่วง เหงื่อออกมากเกินไป
โซเดียมไอออนทำหน้าที่สำคัญในการรักษาสมดุลกรดเบสในร่างกาย การกระทำนี้แสดงออกโดยเฉพาะอย่างยิ่งในไต ในท่อไต โซเดียมไอออนจะถูกดูดกลับเพื่อแลกกับไฮโดรเจนไอออนที่หลั่งออกมา ดังนั้นการรักษาค่า pH ให้คงที่ในระหว่างการก่อตัวของสารที่เป็นกรดและการอนุรักษ์โซเดียมไอออนในร่างกายจึงมั่นใจได้ ความสามารถในไตนี้สูงมากจนอัตราส่วนของความเข้มข้นของไฮโดรเจนไอออนในปัสสาวะและเลือดสูงถึง 800:1
เนื่องจากแหล่งโซเดียมหลักสำหรับร่างกายคือเกลือแกง จึงมักกล่าวกันว่าต้องการเกลือแกง ไม่ใช่โซเดียม ในผู้ใหญ่ความต้องการเกลือแกงคือ 4-5 กรัมต่อวัน ความต้องการเกลือบริโภคที่เพิ่มขึ้นอาจเกี่ยวข้องกับโรคบางชนิด เช่นเดียวกับการขับเหงื่อที่เพิ่มขึ้น ซึ่งโซเดียมไอออนจำนวนมากจะสูญเสียไป ทำให้ความต้องการเกลือในนักกีฬาเพิ่มขึ้น ความต้องการเกลือสูงโดยเฉพาะอย่างยิ่งในผู้ที่เล่นกีฬาซึ่งการฝึกและกิจกรรมการแข่งขันเกี่ยวข้องกับการขับเหงื่อออกมาก
โพแทสเซียมไอออนมักพบในเซลล์ของอวัยวะและเนื้อเยื่อต่างจากโซเดียม ปริมาณโพแทสเซียมทั้งหมดในร่างกายมนุษย์ที่มีน้ำหนัก 70 กก. คือประมาณ 140 กรัมจากจำนวนนี้มีเพียง 25 กรัมเท่านั้นที่อยู่ในพื้นที่นอกเซลล์ ปริมาณโพแทสเซียมไอออนสูงสุดในเม็ดเลือดแดง เส้นใยกล้ามเนื้อ เซลล์ตับ
โพแทสเซียมภายในเซลล์ส่วนใหญ่เกี่ยวข้องกับโปรตีน คาร์โบไฮเดรต ฟอสเฟต ครีเอทีน ฟอสเฟต กระบวนการสังเคราะห์หลายอย่างในร่างกายจำเป็นต้องมีโพแทสเซียมไอออน ดังนั้นโพแทสเซียมจึงมีส่วนร่วมในการสังเคราะห์ไกลโคเจน ด้วยการสร้าง gluconeogenesis ในตับและกล้ามเนื้อ ความเข้มข้นของโพแทสเซียมไอออนอิสระจะลดลง ในทางตรงกันข้าม ด้วยการสลายตัวของไกลโคเจนอย่างเข้มข้น เช่น ระหว่างการทำงานของกล้ามเนื้ออย่างเข้มข้น ความเข้มข้นของโพแทสเซียมไอออนอิสระจะเพิ่มขึ้นอย่างเห็นได้ชัด
มีการสังเกตการจับกันของโพแทสเซียมไอออนในระหว่างการสังเคราะห์โปรตีน, ATP, creatine phosphate ดังนั้น ในระหว่างการสังเคราะห์โปรตีน 2 กรัม โพแทสเซียมไอออนประมาณ 1 เมกกะไบต์จะถูกจับ ด้วยการขาดโพแทสเซียมในร่างกาย การสังเคราะห์สารเหล่านี้จะหยุดชะงัก
โพแทสเซียมมีส่วนร่วมในการส่งแรงกระตุ้นของเส้นประสาทในรูปแบบ synaptic มันมีส่วนร่วมในการสังเคราะห์ acetylcholine ซึ่งเป็นสื่อกลางของการกระตุ้นประสาท นอกจากโซเดียมไอออนแล้ว โพแทสเซียมยังมีส่วนช่วยในการแบ่งขั้วของเยื่อหุ้มเซลล์และการกระตุ้นเซลล์เพื่อให้มั่นใจว่ากล้ามเนื้อหดตัว
โพแทสเซียมไอออนมีส่วนเกี่ยวข้องในการควบคุมการทำงานของหัวใจ หัวใจไวต่อความผันผวนของความเข้มข้นของโพแทสเซียมในเลือด นอกจากนี้ยังมีผลการขยายหลอดเลือด
แมกนีเซียมไอออนปริมาณแมกนีเซียมทั้งหมดในร่างกายมนุษย์ที่มีน้ำหนัก 70 กก. คือประมาณ 14.4 กรัม ปริมาณแมกนีเซียมสูงสุดอยู่ในเนื้อเยื่อกระดูก โดยจะอยู่ในรูปของเกลือฟอสเฟต คาร์บอนิก และฟลูออไรด์ เถ้ากระดูกมีแมกนีเซียมสูงถึง 1.5% เนื้อเยื่อกระดูกมีเกลือแมกนีเซียมที่ละลายน้ำได้จำนวนหนึ่ง ซึ่งจะสร้างคลังเก็บในร่างกาย การขาดแมกนีเซียมเกลือในเนื้อเยื่อกระดูกทำให้เกิดความล่าช้าในการเจริญเติบโตในความยาวและความหนา
แมกนีเซียมเป็นส่วนหนึ่งของเลือด กล้ามเนื้อ ตับ ไต และอวัยวะและเนื้อเยื่ออื่นๆ ซึ่งทำหน้าที่สำคัญต่างๆ ที่นั่น มันเป็นตัวกระตุ้นของเอ็นไซม์หลายชนิด: cholinesterase, phosphoglucomutase, pyrophosphatase, arginase, carboxylase, dipeptidase ในลำไส้ แมกนีเซียมมีความจำเป็นในการสังเคราะห์อะเซทิลโคลีน สำหรับการเกิดไกลโคไลซิส ในการสังเคราะห์โปรตีน การก่อตัวและการสลายของเอทีพี เขามีส่วนร่วมในการหดตัวของกล้ามเนื้อควบคุมการทำงานของหัวใจ การศึกษาจำนวนมากได้แสดงให้เห็นความสัมพันธ์แบบผกผันระหว่างการตายจากโรคหัวใจและเนื้อหาของแมกนีเซียมที่แตกตัวเป็นไอออนในร่างกาย เช่นเดียวกับในน้ำดื่มซึ่งเป็นแหล่งแมกนีเซียมหลักสำหรับร่างกาย
นอกเหนือจากที่กล่าวมาแล้ว แมกนีเซียมยังทำหน้าที่อื่นๆ ในร่างกายมนุษย์ และการขาดหรือมากเกินไปของแมกนีเซียมอาจทำให้เกิดความผิดปกติร้ายแรงได้ ดังนั้นแมกนีเซียมจึงจำเป็นสำหรับการดูดซึมผลิตภัณฑ์ย่อยอาหารในทางเดินอาหาร อย่างไรก็ตามแมกนีเซียมส่วนเกินจะลดอัตราการดูดซึมของบางชนิดโดยเฉพาะกรดไขมันเนื่องจากการก่อตัวของสารเชิงซ้อนที่ไม่ละลายน้ำ
การขาดแมกนีเซียมนำไปสู่การเปลี่ยนแปลงที่สำคัญในองค์ประกอบแร่ธาตุของเซลล์ การเพิ่มขึ้นของความเข้มข้นของไตรกลีเซอไรด์ในเลือด การแทรกซึมของไขมันในตับ การกลายเป็นปูนของหลอดเลือด และปริมาณอีลาสตินที่ลดลง การขาดแมกนีเซียมทำให้เกิดเนื้อร้ายและจุดโฟกัสของการกลายเป็นปูนในกล้ามเนื้อหัวใจ, ภาวะเลือดคั่งของเยื่อเมือกของตา, จมูก, ปาก, ผมร่วง, ชัก และในที่สุดสามารถนำไปสู่ความตายของร่างกาย
คลอรีนไอออนปริมาณคลอรีนในร่างกายมนุษย์ที่มีน้ำหนัก 70 กก. อยู่ที่ประมาณ 88.7 กรัม คลอรีนไอออนเป็นแอนไอออนหลักในพลาสมาในเลือด ซึ่งคิดเป็นประมาณ 75% ของจำนวนแอนไอออนทั้งหมดในเลือด เช่นเดียวกับโซเดียมไอออน คลอไรด์ไอออนมีส่วนเกี่ยวข้องในการรักษาความดันออสโมติกของพลาสมาในเลือดและของเหลวทางชีวภาพอื่นๆ ในเรื่องนี้ปริมาณน้ำในร่างกายและอวัยวะและเนื้อเยื่อแต่ละส่วนถูกกำหนดโดยความเข้มข้นของคลอไรด์ไอออนเป็นส่วนใหญ่ คลอไรด์ไอออนที่มากเกินไปจะมาพร้อมกับปริมาณน้ำที่เพิ่มขึ้น การขาดสารนี้จะทำให้สูญเสียน้ำ
คลอรีนไอออนมีส่วนร่วมในการล้างพิษของร่างกายโดยผูกมัดผลิตภัณฑ์เมตาบอลิซึมที่เป็นพิษ โดยเฉพาะอย่างยิ่งพวกเขามีส่วนร่วมในการกำจัดแอมโมเนียและไฮโดรเจนไอออนออกจากร่างกายผ่านทางไต ส่วนหนึ่งของแอมโมเนียที่เกิดขึ้นในเซลล์ของร่างกายในกระบวนการกำจัดกรดอะมิโนและสารประกอบที่มีไนโตรเจนอื่น ๆ ถูกส่งไปยังไตโดยกรดกลูตามิกหรือแอสปาร์ติก มันถูกแยกออกจากกรดอะมิโนที่ระบุและรวมกับคลอไรด์และไฮโดรเจนไอออนเพื่อสร้างแอมโมเนียมคลอไรด์ (NH 4 Cl) ซึ่งขับออกจากร่างกายในปัสสาวะ ในเวลาเดียวกัน ไฮโดรเจนไอออนจะถูกจับและขับออกจากร่างกาย ซึ่งช่วยให้รักษาสมดุลกรดเบสของร่างกายได้ ปฏิกิริยาดำเนินไปตามสมการ:
NH 3 + H + + Cl¯ → NH 4 Cl
คลอรีนเข้าสู่ร่างกายร่วมกับโซเดียมเป็นหลัก (เป็นส่วนหนึ่งของเกลือแกง) ความต้องการเกลือบริโภคที่กล่าวถึงก่อนหน้านี้ตอบสนองความต้องการของร่างกายมนุษย์ทั้งโซเดียมและคลอรีน
ไมโครอิลิเมนต์นอกเหนือจากข้างต้น ร่างกายมนุษย์ประกอบด้วยไอออนจำนวนหนึ่งที่มีความเข้มข้นเล็กน้อย (ไม่เกิน 0.001%) ซึ่งรวมถึง: Fe 2+ , Zn 2+ , Mn 2+ , Mo 2+ , Co 2+ , J‾ และอื่นๆ เนื่องจากมีเนื้อหาในร่างกายต่ำจึงเรียกว่าธาตุ หน้าที่ของธาตุในร่างกายมนุษย์มีความหลากหลายแม้ว่าบทบาทของบางส่วนยังไม่ได้รับการศึกษาอย่างเพียงพอ ให้เราอาศัยบทบาทขององค์ประกอบการติดตามบางอย่าง
ไอออนของเหล็กเป็นส่วนหนึ่งของฮีโมโกลบินในเลือดและไมโอโกลบินที่มีอยู่ในเนื้อเยื่อของกล้ามเนื้อ เนื้อเยื่อและอวัยวะอื่นๆ ไอออน Fe 2+ เกี่ยวข้องกับการส่งออกซิเจนไปยังเนื้อเยื่อ ทำให้มั่นใจได้ว่าจะเปลี่ยนจากเลือดไปเป็นเนื้อเยื่อและสะสมไว้ในนั้น นอกจากนี้ ไอออนของเหล็กยังเป็นส่วนหนึ่งของเอนไซม์ของแอโรบิกออกซิเดชัน (ไซโตโครม) เช่นเดียวกับคาตาเลสซึ่งเป็นเอนไซม์ที่สลายไฮโดรเจนเปอร์ออกไซด์ที่เกิดขึ้นในกระบวนการออกซิเดชันทางชีวภาพ
กิจกรรมของกล้ามเนื้อที่รุนแรงนั้นมาพร้อมกับการเพิ่มขึ้นอย่างมีนัยสำคัญในการเผาผลาญพลังงานและด้วยเหตุนี้การเพิ่มขึ้นของการสลายตัวของสารประกอบที่มีธาตุเหล็กที่เกี่ยวข้องกับการจัดเตรียมนั้นการเพิ่มขึ้นของการเผาผลาญของธาตุเหล็กโดยทั่วไป ในขณะเดียวกัน ระดับการดูดซึมธาตุเหล็กจากอาหารก็ต่ำมาก เป็นผลให้ในช่วงระยะเวลาของการฝึกที่รุนแรง ภาวะขาดธาตุเหล็กของร่างกายอาจเกิดขึ้นและความจำเป็นในการเตรียมสารที่มีธาตุเหล็กเป็นปัจจัยทางโภชนาการเพิ่มเติม
ไอออนของสังกะสีเป็นส่วนหนึ่งของเอนไซม์จำนวนหนึ่งที่เกี่ยวข้องกับปฏิกิริยาการสังเคราะห์และกระบวนการแคแทบอลิซึม จำเป็นสำหรับกระบวนการถ่ายโอนข้อมูลทางพันธุกรรมในเซลล์ สำหรับการสังเคราะห์ฮีโมโกลบิน ไอออนของสังกะสีมีส่วนเกี่ยวข้องในการรักษาเสถียรภาพของโครงสร้างของโมเลกุลขนาดใหญ่ กระบวนการเจริญเติบโตของร่างกาย การทำงานของระบบภูมิคุ้มกัน กระบวนการสมานแผล การพัฒนาสมองในทารกในครรภ์ และกระตุ้นการทำงานของฮอร์โมนในตับอ่อน
ไอออนของแมงกานีสมีส่วนเกี่ยวข้องกับการเผาผลาญของกลูโคซามิโนไกลแคน ซึ่งเป็นส่วนหนึ่งของเนื้อเยื่อเกี่ยวพัน กลูโคส ไกลโคเจน และไขมัน พวกเขามีบทบาทสำคัญในการเผาผลาญในสมอง ด้วยการขาดแมงกานีสการเผาผลาญในเนื้อเยื่อเกี่ยวพันทำให้สมองถูกรบกวนอัตราการสังเคราะห์ไกลโคเจนลดลง
กลไกการออกฤทธิ์ของแมงกานีสไอออนยังไม่ชัดเจนในหลาย ๆ ด้าน จนถึงขณะนี้มีเพียงบทบาทที่เป็นปัจจัยร่วมของเอนไซม์จำนวนหนึ่งโดยเฉพาะไกลโคซิลทรานสเฟอเรสเท่านั้นที่แสดงให้เห็นอย่างชัดเจน
โคบอลต์มีส่วนเกี่ยวข้องกับการสร้างเม็ดเลือดแดง (การสังเคราะห์ฮีโมโกลบิน) และการควบคุมการเผาผลาญธาตุเหล็กในร่างกาย มีบทบาทสำคัญในการควบคุมไขมันในเลือดและปฏิกิริยาการเผาผลาญบางอย่างที่เกิดขึ้นในหัวใจ เนื้อเยื่อประสาท และผนังของทางเดินอาหาร
ไอออนของทองแดง นิกเกิล โครเมียม และธาตุอื่นๆ ทำหน้าที่สำคัญในร่างกาย ดังนั้นทองแดงจึงมีส่วนร่วมในการก่อตัวของฟลาโวโปรตีนและไซโตโครมออกซิเดส - เอนไซม์ของการเผาผลาญพลังงานมีผลกระตุ้นการทำงานของไกลโคไลซิส ธาตุบางชนิดไม่เพียงแต่เป็นส่วนหนึ่งของเอ็นไซม์เท่านั้น แต่ยังรวมถึงฮอร์โมนด้วย ดังนั้นไอโอดีนจึงเป็นองค์ประกอบโครงสร้างของฮอร์โมนไทรอยด์ ได้แก่ ไทรอกซินและไตรไอโอโดไทโรนีน
แมกนีเซียมเป็นหนึ่งในองค์ประกอบการติดตามที่สำคัญและขาดไม่ได้สำหรับร่างกายมนุษย์ และในช่วงที่คลอดบุตรความต้องการนั้นก็เพิ่มขึ้นหลายเท่า มันเป็นสิ่งสำคัญทั้งสำหรับการทำงานปกติของร่างกายของมารดาและการตั้งครรภ์ที่ประสบความสำเร็จ และสำหรับการเจริญเติบโตและพัฒนาการตามปกติของทารก
ธาตุติดตามนี้เกี่ยวข้องกับกระบวนการเผาผลาญหลายอย่าง ซึ่งมีส่วนช่วยในการทำงานปกติของกล้ามเนื้อ กระดูก ระบบประสาท และระบบภูมิคุ้มกัน นั่นคือเหตุผลที่การขาดสารอาหารสำหรับหญิงตั้งครรภ์สามารถคุกคามด้วยผลร้ายแรง
บทบาทของแมกนีเซียมคืออะไร?
แมกนีเซียมมีส่วนเกี่ยวข้องกับกระบวนการเผาผลาญในร่างกาย ช่วยปรับกระบวนการส่งกระแสประสาทในเนื้อเยื่อของกล้ามเนื้อให้เป็นปกติผ่อนคลายกล้ามเนื้อลดเสียงที่มากเกินไปและทำให้ระบบประสาทสงบ
บ่อยครั้งที่ผู้หญิงได้รับแมกนีเซียมเพิ่มเติมในขั้นตอนการเตรียมการสำหรับการตั้งครรภ์ ได้รับการพิสูจน์แล้วว่าแมกนีเซียมส่งเสริมและควบคุมกระบวนการถ่ายโอนสารพันธุกรรมของผู้ปกครองไปยังเด็ก ไอออน Mg 2+ มีส่วนร่วมในการสังเคราะห์ส่วนประกอบโครงสร้างดีเอ็นเอ
นอกจากนี้ จุลธาตุนี้ยังมีส่วนสำคัญในการสังเคราะห์โปรตีน ซึ่งเป็นวัสดุก่อสร้างสำหรับอวัยวะภายในและระบบของทารกโดยตรง
แมกนีเซียมยังมีส่วนเกี่ยวข้องกับการทำงานเต็มรูปแบบของรกตลอดการตั้งครรภ์ โดยควบคุมการเผาผลาญระหว่างสิ่งมีชีวิตของแม่และเด็ก
ทำไมการขาดแมกนีเซียมจึงเป็นอันตรายต่อสตรีมีครรภ์?
การขาดแมกนีเซียม (hypomagnesemia) สามารถกระตุ้นการก่อตัวของข้อบกพร่องในเศษขนมปัง พัฒนาการก่อนคลอดระบบกล้ามเนื้อและกระดูกหรือหัวใจ การขาดแมกนีเซียมสามารถนำไปสู่การคลอดก่อนกำหนดหรือการแท้งบุตรที่ถูกคุกคาม
บน วันหลังและในการคลอดบุตร แมกนีเซียมมีความสำคัญต่อสตรีมีครรภ์พอๆ กับตลอดการตั้งครรภ์ การขาดองค์ประกอบขนาดเล็กนี้นำไปสู่การลดลงของความยืดหยุ่นของเส้นใยกล้ามเนื้อและการละเมิดการหดตัวซึ่งอาจนำไปสู่การละเมิดกิจกรรมแรงงาน (ความอ่อนแอ, การไม่ประสานกันของกิจกรรมแรงงาน) เป็นผลให้ความเสี่ยงของการบาดเจ็บและการแตกของช่องคลอดของมารดาเพิ่มขึ้น
ความต้องการแมกนีเซียมในระหว่างตั้งครรภ์เพิ่มขึ้นประมาณ 30% ท้ายที่สุด สิ่งมีชีวิตทั้งสองต้องการมัน - แม่และเด็ก
เติมเต็มการขาดสารใด ๆ ที่จำเป็นสำหรับเด็กในช่วงเวลา การตั้งครรภ์กำลังจะมาจากร่างกายสำรองของมารดา ดังนั้นจึงเป็นที่ชัดเจนว่าบางครั้งสตรีมีครรภ์อาจมีสัญญาณที่ชัดเจนของการขาดธาตุ
หากอาหารมีแมกนีเซียมเข้าสู่ร่างกายไม่เพียงพอ ร่างกายก็จะดึงแมกนีเซียมออกจากกระดูก ฟัน และต่อมไร้ท่อ ดังนั้นเขาจึงพยายามชดเชยระดับแมกนีเซียมในเลือดที่ลดลงในช่วงเริ่มต้น
มันจึงสำคัญไฉน หญิงมีครรภ์ป้องกันภาวะขาดแมกนีเซียมในทุกระยะ - ตั้งแต่การวางแผนการตั้งครรภ์จนถึงการคลอดเอง
จะตรวจสอบการขาดแมกนีเซียมในร่างกายได้อย่างไร?
อาการที่พบในหญิงตั้งครรภ์ที่มีภาวะขาดแมกนีเซียม:
จาก กล้ามเนื้อกระตุก
บ่อยครั้งหากขาดแมกนีเซียม สตรีมีครรภ์มักกังวลว่าจะมีอาการปวดที่หลังส่วนล่างและแขนขาส่วนล่าง มีอาการตึงของกล้ามเนื้อและรู้สึกไม่สบายที่คอ
การขาดแมกนีเซียมยังแสดงออกโดยความตึงเครียด (การหดตัว) ของกล้ามเนื้อของมดลูก ผู้หญิงอธิบายอาการนี้ว่า "ท้องแข็ง", "ท้องตึงโดยไม่ตั้งใจ" ในกรณีนี้มีอาการปวดเกร็งเกร็งในช่องท้องส่วนล่าง เสียงของมดลูกที่เพิ่มขึ้นดังกล่าวสามารถนำไปสู่การยุติการตั้งครรภ์
อาการแสดงของการหดตัวของกล้ามเนื้อบกพร่องในการขาดแมกนีเซียมก็คือตะคริวของกล้ามเนื้อน่อง การหดตัวของกล้ามเนื้อน่องอย่างรุนแรง ต่อเนื่อง และเจ็บปวดมากมักเกิดขึ้นในเวลากลางคืนเป็นหลัก สภาพค่อนข้างไม่เป็นที่พอใจเจ็บปวด
คุณต้องเข้าใจว่าตะคริวที่ขากรรไกรล่างสามารถบ่งบอกถึงการขาดแมกนีเซียมไม่เพียง แต่ยังขาดแคลเซียมในร่างกายของหญิงตั้งครรภ์ด้วย
การเปลี่ยนแปลงของระบบประสาท
ในระหว่างตั้งครรภ์ สภาพจิตใจของผู้หญิงจะเปลี่ยนไป มีความกังวลเกี่ยวกับสุขภาพของทารกและความเป็นอยู่ที่ดีของตัวเอง และด้วยการขาดแมกนีเซียม ความรุนแรงของความกังวลใจ ความหงุดหงิดอย่างไม่สมเหตุผล การรบกวนการนอนหลับ ความอ่อนไหวทางอารมณ์ การร้องไห้ และประสิทธิภาพที่ลดลงก็เพิ่มขึ้นอย่างมาก
การเปลี่ยนแปลงของระบบหัวใจและหลอดเลือด
การขาดแมกนีเซียมเป็นที่ประจักษ์โดยเพิ่มขึ้น ความดันโลหิต. ในเวลาเดียวกัน อาการวิงเวียนศีรษะและปวดศีรษะก็เข้าร่วมกับความกดดันสูง เมื่อเทียบกับพื้นหลังของความดันที่เพิ่มขึ้นการไหลเวียนของเลือดดำจากส่วนล่างจะถูกรบกวนซึ่งแสดงออกโดยอาการบวมที่ขา
ด้วยการขาดแมกนีเซียมไอออนที่เด่นชัดการนำหัวใจอาจถูกรบกวนด้วยการพัฒนาของภาวะหัวใจเต้นผิดจังหวะและการเกิดความเจ็บปวดในบริเวณหัวใจ
ระดับแมกนีเซียมในเลือดที่ลดลงต่ำกว่า 0.7 mmol / l บ่งชี้ว่าขาดธาตุนี้ ในสภาวะนี้ การแลกเปลี่ยนอิเล็กโทรไลต์ (โซเดียม โพแทสเซียม แมกนีเซียม) จะถูกรบกวนระหว่างการหดตัวของกล้ามเนื้อหัวใจ (กล้ามเนื้อหัวใจ)
ด้วยการขาดแมกนีเซียมในร่างกาย การผ่อนคลายของผนังกล้ามเนื้อของหลอดเลือดก็ถูกรบกวนเช่นกัน เป็นผลให้เนื่องจาก vasospasm ระดับปานกลางอย่างต่อเนื่องการไหลเวียนของเลือดไปยังส่วนสุดท้ายของร่างกายจึงน้อยกว่าปกติ ดังนั้นผู้ที่ขาดแมกนีเซียมจะไวต่อความหนาวเย็นมากขึ้น อากาศหนาวเย็นแม้ในฤดูร้อน
การเปลี่ยนแปลงของระบบย่อยอาหาร
การขาดแมกนีเซียมกระตุ้นให้เกิดการหดตัวของลำไส้ซึ่งก็คือการบีบตัวของมัน ดังนั้นอาการท้องผูกและท้องอืดจึงมักเกิดขึ้นพร้อมกับอาการที่บกพร่องดังกล่าว
คุณสมบัติของโภชนาการที่ขาดแมกนีเซียม
แมกนีเซียมถูกดูดซึมจากอาหารในลำไส้ ส่วนใหญ่เป็นอาหารบาง แต่บางส่วนอยู่ในส่วนที่หนา แต่น่าเสียดายที่แมกนีเซียมเพียง 35% ถูกดูดซึมจากอาหารผ่านทางเดินอาหาร
สิ่งที่สามารถทำได้เพื่อดูดซับแมกนีเซียมมากกว่า 35%? การดูดซึมจะดีขึ้นโดยวิตามินบี 6 และกรดอินทรีย์บางชนิด (แลกติก ซิตริก แอสปาร์ติก)
นอกจากนี้ยังมีความสำคัญในรูปแบบใดที่แมกนีเซียมเข้าสู่ร่างกาย ดังนั้นสารประกอบอินทรีย์ เช่น แมกนีเซียมซิเตรต (สารประกอบแมกนีเซียมกับกรดซิตริก) แมกนีเซียมแลคเตต (สารประกอบแมกนีเซียมกับกรดแลคติก) จะถูกดูดซึมผ่านลำไส้ได้ดี แต่ เกลืออนินทรีย์แทบไม่ถูกดูดซึม เช่น แมกนีเซียมซัลเฟต
เพื่อป้องกันการขาดแมกนีเซียมในหญิงตั้งครรภ์ จำเป็นต้องรวมอาหารที่อุดมด้วยแมกนีเซียมในอาหาร เหล่านี้รวมถึง: ผักชีฝรั่ง ผักชีฝรั่ง ถั่ว พืชตระกูลถั่ว ปลาและอาหารทะเล ข้าวโอ๊ตและบัควีท แตงโม ไข่แดง ถั่วเหลือง รำ กล้วย ยี่หร่า ขนมปังโฮลเกรน

มีแมกนีเซียมจำนวนมากในอาหารจากพืชสีเขียวทั้งหมด สีเขียวให้คลอโรฟิลล์พืช นี่เป็นสารพิเศษซึ่งเป็นโปรตีนที่ซับซ้อนซึ่งพืชมีกระบวนการสังเคราะห์ด้วยแสงที่สำคัญมาก
โครงสร้างทางเคมีของคลอโรฟิลล์คล้ายกับโปรตีนในเลือดมนุษย์ มีเพียงเฮโมโกลบินที่มีไอออนของเหล็ก และคลอโรฟิลล์มีแมกนีเซียมไอออน ดังนั้นควรกินผักและผลไม้สีเขียวให้มากขึ้น เหล่านี้เป็นแหล่งแมกนีเซียมที่สำคัญที่สุดสำหรับร่างกายมนุษย์
แต่แมกนีเซียมที่เข้มข้นที่สุดก็ยังไม่ใช่อาหารที่เป็นมิตรต่อสิ่งแวดล้อม ด้านล่างนี้คือตารางผู้นำด้านอาหารในแง่ของปริมาณแมกนีเซียมต่อผลิตภัณฑ์ 100 กรัม มาดูกันว่าผลิตภัณฑ์ใดที่เหมาะสมที่สุดสำหรับคุณในการเติมแมกนีเซียมสำรองในร่างกาย
| ชื่อผลิตภัณฑ์ | ปริมาณแมกนีเซียม มก./100 กรัมของส่วนที่กินได้ของผลิตภัณฑ์ |
|---|---|
| เมล็ดฟักทอง | 534 |
| รำข้าวสาลี | 448 |
| โกโก้ 20% | 442 |
| งา (เมล็ดคั่ว) | 356 |
| เม็ดมะม่วงหิมพานต์ (ดิบ) | 292 |
| อัลมอนด์ (คั่ว) | 286 |
| ถั่วไพน์นัท | 251 |
| ถั่วเหลือง (ถั่วแห้ง) | 240 |
| จมูกข้าวสาลีดิบ | 239 |
| บัควีท (ดิบ) | 231 |
| แตงโม | 224 |
| คอร์นเฟล็ค | 214 |
| เกล็ดข้าวโอ๊ต | 130 |
| เมล็ดทานตะวัน (อบ) | 129 |
| ถั่วลันเตา | 128 |
| โรสฮิป (แห้ง) | 120 |
| วอลนัท | 100 |
ทีนี้มาดูว่าปัจจัยใดบ้างที่ขัดขวางการดูดซึมแมกนีเซียมหรือมีส่วนทำให้ปริมาณสำรองในร่างกายหมดไป
- เครื่องดื่มที่มีคาเฟอีน
- อาหารที่ซ้ำซากจำเจที่มีคาร์โบไฮเดรตและขนมหวานที่ย่อยง่ายมากเกินไป
- โซดาหวาน
- แอลกอฮอล์การสูบบุหรี่
- อาการปวดเรื้อรังหรือความเครียด
- โรคต่อมไร้ท่อ: พร่อง, เบาหวาน;
- โรคที่มาพร้อมกับการขับเหงื่อเพิ่มขึ้น
- ทานยาบางชนิด (ยาขับปัสสาวะ, ยากันชัก, เกลือแคลเซียม)
ความต้องการแมกนีเซียมในแต่ละวันระหว่างตั้งครรภ์และให้นมบุตร
ข้อมูลความต้องการแมกนีเซียมในแต่ละวันสำหรับสตรีมีครรภ์และให้นมบุตรใน แหล่งต่างๆแตกต่าง. นักโภชนาการและนักวิทยาศาสตร์ยังไม่ได้ตกลงร่วมกัน
ด้านล่างคือ ตารางเปรียบเทียบความต้องการแมกนีเซียมที่เพิ่มขึ้นโดยคำนึงถึงอายุของผู้หญิง เหล่านี้เป็นตัวเลขที่ผู้เชี่ยวชาญจำนวนมากที่สุดยึดถือ
แมกนีเซียมกำหนดให้กับหญิงตั้งครรภ์เมื่อใด
สามารถตรวจพบการขาดแมกนีเซียมโดยใช้การตรวจเลือดทางชีวเคมี
- ด้วยการขาดแมกนีเซียมที่รุนแรงปานกลาง: 12 - 17 มก. / ล. (0.5 - 0.7 มิลลิโมล / ลิตร);
- ด้วยการขาดแมกนีเซียมอย่างรุนแรง: ต่ำกว่า 12 มก. / ล. (0.5 มิลลิโมล / ลิตร)
มีการระบุการเตรียมแมกนีเซียมสำหรับการขาดแมกนีเซียมที่กำหนดโดยการทดสอบทางคลินิก เช่นเดียวกับการปรากฏของสัญญาณของการขาดแมกนีเซียมที่อธิบายไว้ข้างต้น (ความหงุดหงิด, น้ำตาไหล, นอนหลับไม่ดี, อ่อนเพลีย, กล้ามเนื้อกระตุก, ฯลฯ )
การบริโภคแมกนีเซียมเพิ่มเติมจะถูกระบุโดยตรงสำหรับภาวะ hypertonicity ของมดลูก ภาวะนี้มักเกิดขึ้นในช่วงไตรมาสแรกของการตั้งครรภ์และเพิ่มความเสี่ยงต่อการแท้งบุตรในระยะแรก ๆ การรักษามีการกำหนดไว้ตลอดระยะเวลาการคลอดบุตร
แพทย์สามารถกำหนดการเตรียมแมกนีเซียมได้ทั้งในขั้นตอนการวางแผนการตั้งครรภ์และระหว่างตั้งครรภ์ในช่วงเวลาต่างๆ
การเลือกการเตรียมแมกนีเซียม การกำหนดขนาดยา รูปแบบขนาดยา และระยะเวลาในการรักษาจะดำเนินการโดยแพทย์เป็นรายบุคคลในแต่ละกรณีเท่านั้น
ส่วนใหญ่แพทย์สั่งแมกนีเซียมให้กับหญิงตั้งครรภ์ในรูปแบบของยา Magne B 6 ด้านล่างนี้เป็นคำอธิบายของยานี้
การใช้ Magne B 6 ในหญิงตั้งครรภ์
สารออกฤทธิ์ของ Magne B 6 คือแมกนีเซียม แลคเตท ไดไฮเดรต และ ไพริดอกซิน ไฮโดรคลอไรด์ (รูปแบบออกฤทธิ์ของวิตามินบี 6) ไพริดอกซิช่วยเพิ่มการดูดซึมแมกนีเซียม ส่งเสริมการเข้าสู่เซลล์ของร่างกาย
มีการผลิตยาสองเวอร์ชัน: Magne B 6 และ Magne B 6 forte ในระหว่างตั้งครรภ์อนุญาตให้ใช้แบบฟอร์มเหล่านี้ได้ ความแตกต่างระหว่างพวกเขาอยู่ในความเข้มข้นของสารออกฤทธิ์
ใน Magna B 6 forte ปริมาณของสารออกฤทธิ์จะเพิ่มเป็นสองเท่า นอกจากนี้ เนื่องจากเนื้อหาของสารปรุงแต่งต่างๆ จึงมีการดูดซึมสูง (ความสามารถในการดูดซึมในร่างกาย) ระดับการดูดซึมของ Magne B 6 forte อยู่ที่ประมาณ 90% ในขณะที่การดูดซึมของ Magne B6 นั้นใกล้เคียงกับ 50%
การปลดปล่อยยามีหลายรูปแบบ: ยาเม็ดเคลือบ สีขาว, หลอดที่มีสารละลายสำหรับการบริหารช่องปากและหลอดสำหรับการฉีด (สารละลายสำหรับการฉีดเข้ากล้ามหรือทางหลอดเลือดดำ). สารละลายมีอยู่ในหลอดแก้วสี ในแพ็คเกจ 10 หลอด ทางแก้เองมี สีน้ำตาลและกลิ่นคาราเมล
มอบหมายให้ Magne B 6th 6-8 เม็ดในหนึ่งวัน. ตามกฎแล้วแนะนำให้รับประทาน 2 เม็ดวันละสามครั้งพร้อมอาหาร ยาในหลอดสำหรับการบริหารช่องปากใช้เวลา 2-4 หลอดต่อวัน แบบฟอร์มนี้ต้องการการเจือจางยาเบื้องต้นในน้ำ 200 มิลลิลิตร
ข้อห้ามและผลข้างเคียงของ Magne B 6
Magne B 6 มีข้อห้ามใน:
- แพ้ยาและส่วนประกอบ
- ภาวะไตวาย.
- แพ้ฟรุกโตส malabsorption ของกลูโคสและกาแลคโตส
- Phenylketonuria เมื่อการเผาผลาญของกรดอะมิโนบางชนิดถูกรบกวน
- เด็กอายุต่ำกว่า 1 ปี
- การให้นมลูก
โดยทั่วไปแล้ว Magne B 6 จะทนได้ดี แต่คำแนะนำสำหรับยารวมถึงผลข้างเคียงที่เป็นไปได้ดังต่อไปนี้:
- ปวดท้อง;
- ความผิดปกติของอุจจาระในรูปแบบของอาการท้องร่วง
- อาการแพ้ในรูปแบบของลมพิษ, อาการบวมน้ำของ Quincke
หากมีอาการเหล่านี้เกิดขึ้นขณะรับประทานยา ควรปรึกษาแพทย์ทันที
การเสริมแมกนีเซียมในระยะยาวปลอดภัยหรือไม่?
หลักสูตรระยะยาวในปริมาณการรักษาที่กำหนดโดยแพทย์ที่มีการทำงานของไตปกติไม่สามารถนำไปสู่การให้ยาเกินขนาดได้ การดูดซึมแมกนีเซียมและการเข้าสู่กระแสเลือดจะค่อยๆ ยาถูกขับออกทางไต ดังนั้นไตที่แข็งแรงสามารถรับมือกับผลิตภัณฑ์เมตาบอลิซึมของยาและส่วนเกินได้
การเตรียมแมกนีเซียมเข้าสู่ เต้านม. ดังนั้นจึงไม่แนะนำให้คุณแม่พยาบาลรับประทานยานี้
เมื่อสั่งจ่ายอาหารเสริมแมกนีเซียม อย่าลืมบอกแพทย์เกี่ยวกับการใช้วิตามินรวมเพิ่มเติมหรือยาอื่นๆ (แคลเซียม ธาตุเหล็ก) แพทย์จะต้องคำนวณปริมาณแมกนีเซียมที่ต้องการโดยคำนึงถึงเนื้อหาของธาตุนี้ในคอมเพล็กซ์ของคุณ
นี่เป็นสิ่งสำคัญเช่นกันเนื่องจากแมกนีเซียมและแคลเซียมเป็นปฏิปักษ์ (คู่แข่ง) ในร่างกายและขัดขวางการดูดซึมของกันและกัน การต้อนรับของพวกเขาควรแบ่งตามเวลา นอกจากนี้ คุณไม่สามารถรับประทานแมกนีเซียมและธาตุเหล็กพร้อมกันได้ เนื่องจากจะลดการดูดซึมของแมกนีเซียมแต่ละตัว
แม้ว่าการเตรียมแมกนีเซียมจะถือว่าปลอดภัย แต่คุณไม่ควรสั่งจ่ายเอง มีเพียงแพทย์เท่านั้นที่สามารถคำนวณขนาดยาและขั้นตอนการรักษาที่คุณต้องการ
บทบาทในชีวิตพืช
ปริมาณแมกนีเซียมในพืชโดยเฉลี่ยอยู่ที่ 0.07% (โดยน้ำหนัก) เขามีส่วนร่วมในงานที่ยิ่งใหญ่ - การสะสมของพลังงานแสงอาทิตย์ในกระบวนการสังเคราะห์แสงซึ่งเป็นอะตอมกลางในโมเลกุลคลอโรฟิลล์ คลอโรฟิลล์ดูดซับพลังงานแสงอาทิตย์และเปลี่ยนคาร์บอนไดออกไซด์และน้ำให้เป็นสารอินทรีย์ที่ซับซ้อน เช่น น้ำตาล แป้ง ฯลฯ แมกนีเซียมเป็นองค์ประกอบสำคัญของไรโบโซม: ด้วยการมีส่วนร่วม (ร่วมกับ ATP) กรดอะมิโนจึงจับกับ tRNA ในระหว่างการสังเคราะห์โปรตีน . แมกนีเซียมไอออน Mg 2+ โมเลกุลโปรตีน "เชื่อมขวาง" เข้าไปในโกลเมอรูไล โดยคงไว้ซึ่งโครงสร้างของโมเลกุลโปรตีน แมกนีเซียมกระตุ้นการสังเคราะห์ ATP จากนิวคลีโอไซด์ไดฟอสเฟต กระตุ้นระบบเอนไซม์เพื่อเปลี่ยนกรดมาลิกเป็นกรดซิตริก และกรดออกซาลิกเป็นกรดฟอร์มิกและคาร์บอนไดออกไซด์
ด้วยการขาดแมกนีเซียม ผลผลิตของพืชที่ปลูกลดลง การก่อตัวของคลอโรพลาสต์และคลอโรฟิลล์ถูกรบกวน: ใบ (ส่วนใหญ่ส่วนล่าง) กลายเป็น "หินอ่อน": พวกมันซีดระหว่างเส้นเลือดและยังคงเป็นสีเขียวตามเส้นเลือด เนื้อเยื่อระหว่างเส้นเลือดจะได้รับสีที่แตกต่างกัน - สีเหลือง, สีส้ม, สีแดง, สีม่วง จากนั้นพวกมันจะตายโดยเริ่มจากขอบใบ: ใบไม้ม้วนงอและค่อยๆร่วงหล่น ในต้นสนจะสังเกตเห็นสีเหลืองของปลายเข็ม
ตัวบ่งชี้พืชที่มีแมกนีเซียมสูงคือ kostenets
ร่างกายของสัตว์มีแมกนีเซียมประมาณ 0.03–0.07% (โดยมวล) ซึ่งเป็นส่วนหนึ่งของกระดูกและฟัน พบในตับ เลือด เนื้อเยื่อประสาท และสมอง และเกี่ยวข้องกับการเผาผลาญโปรตีนและคาร์โบไฮเดรต สำหรับผู้ที่มีน้ำหนัก 70 กก. ร่างกายจะมีแมกนีเซียม 19–20 กรัม มันมีผลน้ำยาฆ่าเชื้อและ vasodilators ลดความดันโลหิตและคอเลสเตอรอลในเลือดช่วยเพิ่มกระบวนการของการยับยั้งในเปลือกสมองมีผลสงบ (ยากล่อมประสาท) ในระบบประสาทมีบทบาทสำคัญในการเปิดใช้งาน กองกำลังป้องกันร่างกายในการต่อสู้กับโรคมะเร็ง แมกนีเซียมเสริมสร้างระบบภูมิคุ้มกัน มีฤทธิ์ต้านการเต้นของหัวใจ ส่งเสริมการพักฟื้นหลังการออกแรงทางกายภาพ

ด้วยการขาด Mg ความไวต่ออาการหัวใจวายเพิ่มขึ้น สิ่งนี้แสดงให้เห็นโดยการทดลองของนักวิทยาศาสตร์ชาวฮังการีที่ดำเนินการในศตวรรษที่ 20 กับสัตว์ (ในสัตว์โรคนี้เรียกว่า tetany สมุนไพร) สุนัขบางตัวได้รับอาหารที่อุดมด้วยเกลือแมกนีเซียม บางตัวก็น่าสงสาร เมื่อสิ้นสุดการทดลอง สุนัขที่รับประทานอาหารที่มีแมกนีเซียมต่ำ “ได้รับ” ภาวะกล้ามเนื้อหัวใจตาย
แมกนีเซียมถูกขับออกจากร่างกายด้วยปัสสาวะ อุจจาระ และเหงื่อ
ผลิตภัณฑ์จากผัก: ผลไม้, ถั่ว (อัลมอนด์, ถั่วลิสง, วอลนัท), ผัก (มะเขือเทศ, มันฝรั่ง, ฟักทอง, ถั่ว, ผักกาดหอม), มิ้นต์, ชิกโครี, มะกอก, ผักชีฝรั่ง, ข้าวสาลีเต็มเมล็ด, ข้าวโอ๊ต, บัควีท; ขนมปังข้าวไรย์,ข้าวฟ่าง,รำ. ผลิตภัณฑ์จากสัตว์: ตับ ไข่แดง

MgSO 4- แมกนีเซียมซัลเฟต เกลือขม หรือ Epsom
MgCO 3– แมกนีเซียมคาร์บอเนต, แมกนีเซียม.
MgO- แมกนีเซียมออกไซด์, แมกนีเซียที่ถูกเผาไหม้
แมกนีเซียมซิลิเกต: talc 3 มก.O X 4 SiO2 X เอช 2 โอและแร่ใยหิน เฉา X 3 มก.O X 4 SiO2.
คลอโรฟิลล์.
คุณรู้หรือไม่ว่า...
แมกนีเซียมได้รับครั้งแรกในปี พ.ศ. 2351 โดยนักเคมีชาวอังกฤษ จี. เดวี่ จากออกไซด์ของ MgO เปียก ชื่อมาจาก ลาด. แมกนีเซียอัลบ้า(แมกนีเซียสีขาว) ตามแร่ไฮโดรแมกนีไซต์ซึ่งมีโลหะนี้และถูกค้นพบโดยชาวกรีกโบราณใกล้กับเมืองแมกนีเซีย

จำนวนอะตอมแมกนีเซียมในร่างกายมนุษย์คือ 8.7 x 10 23 และในเซลล์เดียว - 8.7 x 10 9
ปริมาณแมกนีเซียมทั้งหมดในคลอโรฟิลล์ของพืชทั้งหมดบนโลกอยู่ที่ประมาณ 100 พันล้านตัน
ปริมาณแมกนีเซียมพร้อมอาหารในร่างกายต่อวันควรอยู่ที่ 240–720 มก.
แมกนีเซียมซัลเฟต MgSO 4 (เกลือขมหรือ Epsom) ใช้ในยาเป็นยาระบาย choleretic และยาแก้ปวด
แมกนีเซียมไอออนไม่เพียงแต่ทำให้น้ำทะเลมีรสเค็ม แต่ยังทำให้ไม่สามารถดื่มได้ ทำให้ท้องเสียและอาเจียนอย่างรุนแรง
คลอโรฟิลล์มีหลายประเภท (คลอโรฟิลล์ เอบีซีดี) ซึ่งแตกต่างกันในโครงสร้างและสเปกตรัมการดูดกลืนแสง พืชและสาหร่ายที่สูงขึ้นมีคลอโรฟิลล์เป็นเม็ดสีหลัก เอและเป็นส่วนเพิ่มเติม - คลอโรฟิลล์ ขไดอะตอมและสาหร่ายสีน้ำตาล - คลอโรฟิลล์เท่านั้น คและสาหร่ายสีแดง - คลอโรฟิลล์ d.
เหล็ก

บทบาทในชีวิตของพืชและจุลินทรีย์
ด้วยการขาดของมันการก่อตัวของคลอโรฟิลล์ช้าลง บางทีการปรากฏตัวของคลอโรซิส (สีเหลือง) ในตอนแรกของใบอ่อนการสูญเสียสี ด้วยการขาดธาตุเหล็กในระยะยาวในไม้ล้มลุก เนื้อเยื่อตายตามขอบใบมีด หน่อตายในต้นไม้ และผลผลิตโดยรวมและความต้านทานของพืชต่อโรคลดลง
ไม้วอร์มวูดและพืชชนิดอื่นๆ เป็นตัวบ่งชี้ปริมาณธาตุเหล็กในดินสูง ในเวลาเดียวกัน ใบของบอระเพ็ดจะกลายเป็นสีเหลืองสดใส และดอกไม้ของพืชบางชนิด เช่น ไฮเดรนเยีย ได้รับสีฟ้าที่ผิดปกติ
ในธรรมชาติมีสิ่งที่เรียกว่าแบคทีเรียธาตุเหล็ก ในกระบวนการสังเคราะห์ทางเคมี พวกมันออกซิไดซ์เหล็กเฟอร์รัสไปเป็นเหล็กเฟอริก ซึ่งสะสมอยู่บนพื้นผิวของเซลล์ ไฮดรอกไซด์เหล็กที่เกิดขึ้น (III) ตกตะกอนและก่อตัวเป็นแร่หนองบึง:
4FeCO 3 + O 2 + 6H 2 O ––> 4Fe(OH) 3 + 4CO 2 + พลังงาน
แบคทีเรียสังเคราะห์เคมีที่ออกซิไดซ์ธาตุเหล็กและแมงกานีสถูกค้นพบโดยนักวิชาการ S.N. วิโนกราดสกี้. พวกมันแพร่หลายอย่างมากทั้งในน้ำจืดและน้ำทะเล ด้วยกิจกรรมที่สำคัญของพวกเขา แร่เหล็กและแร่แมงกานีสจำนวนมากจึงก่อตัวขึ้นที่ด้านล่างของหนองน้ำและทะเล ในและ. Vernadsky ผู้ก่อตั้ง biogeochemistry พูดถึงแหล่งแร่ดังกล่าวซึ่งเป็นผลมาจากกิจกรรมที่สำคัญของแบคทีเรียในสมัยทางธรณีวิทยาโบราณ
บทบาทในชีวิตของสัตว์และมนุษย์
ร่างกายของสัตว์มีธาตุเหล็กประมาณ 0.01% (โดยมวล) ธาตุเหล็กเป็นสิ่งที่ขาดไม่ได้ในกระบวนการสร้างเม็ดเลือดและการเผาผลาญภายในเซลล์ ธาตุเหล็กประมาณ 55% เป็นส่วนหนึ่งของฮีโมโกลบินของเม็ดเลือดแดง ประมาณ 24% เกี่ยวข้องกับการก่อตัวของสีของกล้ามเนื้อ (ไมโอโกลบิน) ประมาณ 21% จะถูกสะสม "สำรอง" ในตับและม้าม

เป็นธาตุเหล็กที่กำหนดสีของเลือดตลอดจนความสามารถในการจับและปล่อยออกซิเจน เซลล์เม็ดเลือดแดงนำออกซิเจนจากปอดไปทั่วร่างกายและกำจัดคาร์บอนไดออกไซด์ ออกซิเจนเป็นตัวออกซิไดซ์ที่แรง แต่เฮโมโกลบินต้องขอบคุณธาตุเหล็กที่บรรจุอยู่จึงสามารถบรรทุกออกซิเจนได้ ร่างกายมนุษย์มีเอนไซม์ที่มีธาตุเหล็ก นอกจากนี้ยังมีคอมเพล็กซ์โปรตีนเฟอร์ริตินซึ่งมีการสร้างสารที่มีธาตุเหล็กอื่น ๆ ที่จำเป็นสำหรับร่างกาย เฟอร์ริกไอออนในร่างกายถูกถ่ายโอนโดยใช้โปรตีนทรานเฟอร์รินที่ซับซ้อน (พบในเลือด นม ไข่ขาว) ธาตุเหล็กมีบทบาทสำคัญในกระบวนการปลดปล่อยพลังงาน ในปฏิกิริยาของเอนไซม์ ในการสร้างภูมิคุ้มกันในการเผาผลาญคอเลสเตอรอล
คนที่มีน้ำหนัก 70 กก. ร่างกายมีธาตุเหล็ก 4.2–5 กรัม ความต้องการธาตุเหล็กในแต่ละวันของผู้ใหญ่ที่มีสุขภาพดีสำหรับธาตุเหล็กคือ 10-20 มก. และเติมเต็มด้วยอาหารที่สมดุลตามปกติ
เมื่อปริมาณธาตุเหล็กในเลือดลดลงจะทำให้เกิดภาวะโลหิตจาง โรคโลหิตจางจากการขาดธาตุเหล็กที่พบบ่อยที่สุดหรือที่เรียกว่าโรคโลหิตจาง

ธาตุเหล็กถูกขับออกจากร่างกายด้วยปัสสาวะ อุจจาระ และเหงื่อ
แหล่งที่มาหลักของการเข้าสู่ร่างกาย
ผักใบเขียว: หัวหอม, หัวผักกาดอ่อน, หัวไชเท้า, มัสตาร์ด, แครอท, แพงพวย, สีน้ำตาล, ถั่วลันเตา, มะเขือเทศ (ดิบเท่านั้น), กะหล่ำปลี, กระเทียม, ถั่ว, มะรุม, แตงกวา ผลไม้และผลเบอร์รี่: แอปเปิ้ล, ทับทิม, ราสเบอร์รี่, สตรอเบอร์รี่, เชอร์รี่, ลูกแพร์, องุ่น, แตงโม, ผลไม้แห้งใด ๆ ผลิตภัณฑ์จากสัตว์: ตับ ไต ไข่แดง
การเชื่อมต่อที่พบบ่อยที่สุด
เฮโมโกลบิน.
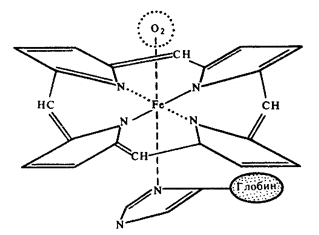
แผนผังของพันธะเฮมโกลบินในโมเลกุลเฮโมโกลบิน
คุณรู้หรือไม่ว่า...
ความคุ้นเคยของมนุษย์โบราณที่มีธาตุเหล็กที่มาจากจักรวาลนั้นพิสูจน์ได้จากข้อเท็จจริงที่ว่าชาวกรีนแลนด์ซึ่งไม่มีความคิดเกี่ยวกับแร่เหล็กมีผลิตภัณฑ์จากเหล็ก อุกกาบาตจำนวนมากประกอบด้วยเหล็กพื้นเมืองที่มีส่วนผสมของนิกเกิลสูงถึง 5.5% นักเล่นแร่แปรธาตุระบุว่าเหล็กในรูปของหอกและโล่ - คุณลักษณะเฉพาะของเทพเจ้าแห่งสงครามดาวอังคาร จึงได้ชื่อมาจากลัต เฟอร์โร- ดาบ
จำนวนอะตอมของธาตุเหล็กในร่างกายมนุษย์คือ 4.5 x 10 22 และในเซลล์เดียว - 4.5 x 10 8
เลือดมนุษย์ 100 มล. มีฮีโมโกลบิน 13-16 กรัม
ใช้เวลาประมาณ 90 วินาทีในการ "รวบรวม" โมเลกุลของเฮโมโกลบินในร่างกายมนุษย์ และทุกๆ วินาทีจะมีการสร้างโมเลกุลเฮโมโกลบิน 650 x 10 12 ขึ้น
วัตถุที่มีชีวิตจำนวนมากมีลักษณะเฉพาะโดยปรากฏการณ์ของแม่เหล็กชีวภาพ การวางแนวของมันในสนามแม่เหล็กของโลกนั้นดำเนินการด้วยความช่วยเหลือของเหล็กออกไซด์ซึ่งอยู่ในรูปแบบพิเศษ - แมกนีโตโซมซึ่งเกิดขึ้นในรูปแบบของโซ่ 10-25 คริสตัลที่มีความยาวรวมประมาณ 50 นาโนเมตร
เกลือของธาตุเหล็กและธาตุเหล็กเฟอริกใช้เพื่อชดเชยการขาดธาตุเหล็กในการรักษาโรคโลหิตจาง
มีการสร้างความสัมพันธ์ระหว่างปริมาณธาตุเหล็กที่เพิ่มขึ้นในร่างกายและ การพัฒนาในช่วงต้นหลอดเลือด, โรคขาดเลือด, เนื้องอก

กรดกำมะถันเหล็ก FeSO 4 x 7H 2 O (เหล็ก (II) ผลึกไฮเดรต) ใช้เพื่อควบคุมศัตรูพืชและเตรียมสีแร่ เหล็กคลอไรด์ (III) FeCl 3 ใช้เป็นสีย้อมผ้าในการย้อมผ้า
สังกะสี

บทบาทในชีวิตของพืช เชื้อรา
สังกะสีเป็นองค์ประกอบย่อยที่สำคัญ มีเนื้อหาในพืชเฉลี่ย 0.003% (โดยน้ำหนัก) กระตุ้นระบบเอ็นไซม์ 30 ระบบในเซลล์ เห็ด (โดยเฉพาะมีพิษ) ไลเคน ต้นสน อุดมไปด้วยสังกะสี ในพืชพร้อมกับการหายใจ โปรตีน และเมแทบอลิซึมของนิวเคลียส สังกะสีจะควบคุมการเจริญเติบโต ส่งผลต่อการก่อตัวของกรดอะมิโนทริปโตเฟน และเพิ่มเนื้อหาของจิบเบอเรลลิน สังกะสีมีความสำคัญต่อการพัฒนาของไข่และทารกในครรภ์ ช่วยเพิ่มความทนทานต่อความแห้งแล้ง ความร้อน และความเย็นของพืช
การขาดมันนำไปสู่การหยุดชะงักของการแบ่งเซลล์ (จุดใบในผลส้ม) ใบแคบบิดเป็นเกลียวจะเกิดขึ้นบนพืช เนื้อเยื่อระหว่างเส้นเลือดเปลี่ยนสีและโดดเด่นด้วยตาข่ายสีเขียวใส
สังกะสีที่มากเกินไปเป็นอันตรายต่อพืชเพราะ สามารถทำให้อวัยวะเสียรูปได้: ในดอกป๊อปปี้ดอกไม้กลายเป็นสองเท่าและในยารุตกะกลีบจะใหญ่มาก ในพืชชนิดอื่น ใบคลอโรซิสสามารถแพร่กระจายจากด้านบนสู่โคนใบได้ ตัวบ่งชี้ของพืชที่มีปริมาณสังกะสีเพิ่มขึ้นในดินคือสีม่วงไตรรงค์หางม้า pansies
บทบาทในชีวิตของสัตว์และมนุษย์
ปริมาณสังกะสีในร่างกายของสัตว์อยู่ที่ประมาณ 0.01% (โดยน้ำหนัก) สัตว์ทะเลที่ไม่มีกระดูกสันหลังบางชนิด เช่น หอยนางรม มีสังกะสี 0.4% (โดยน้ำหนัก) สังกะสีในพิษงูค่อนข้างมาก (เพื่อป้องกันผลกระทบของพิษของมันเอง) ในสัตว์ Zn นอกเหนือจากการมีส่วนร่วมในการหายใจและเมแทบอลิซึมของนิวเคลียสแล้วยังเพิ่มกิจกรรมของอวัยวะสืบพันธุ์ส่งผลต่อการก่อตัวของโครงกระดูกของทารกในครรภ์ ด้วยการขาดสังกะสี เนื้อหาของ RNA จะลดลงและการสังเคราะห์โปรตีนในสมองลดลง การพัฒนาของสมองช้าลง
คนที่มีน้ำหนัก 70 กก. ร่างกายจะมีสังกะสีมากถึง 3 กรัม มันเป็นส่วนหนึ่งของเอนไซม์ที่สำคัญที่สุด: carbonic anhydrase (เร่งการปล่อยก๊าซคาร์บอนไดออกไซด์ในปอด), ดีไฮโดรจีเนสต่างๆ, ฟอสฟาเตส (เกี่ยวข้องกับการหายใจและกระบวนการทางสรีรวิทยาอื่น ๆ), โปรตีเอสและเปปไทเดสที่เกี่ยวข้องกับการเผาผลาญโปรตีน, เอนไซม์ของเมแทบอลิซึมของนิวเคลียส ( RNA และ DNA พอลิเมอเรส ). สังกะสีเล่น บทบาทสำคัญในการสังเคราะห์โมเลกุล mRNA ในส่วนที่เกี่ยวข้องของ DNA (การถอดความ) ในการรักษาเสถียรภาพของโครงสร้างของไรโบโซมและไบโอโพลีเมอร์ (RNA, DNA, โปรตีนบางชนิด) สังกะสีเป็นส่วนสำคัญของเอนไซม์ในเลือด จำเป็นสำหรับการบำรุงผิวตามปกติ การเจริญเติบโตของเส้นผมและเล็บ และการสมานแผล เนื่องจากเกี่ยวข้องกับการสังเคราะห์โปรตีน สังกะสีเป็นส่วนหนึ่งของอินซูลิน ฮอร์โมนตับอ่อนที่ควบคุมระดับน้ำตาลในเลือด และฮอร์โมนไทมัส สังกะสีมีบทบาทสำคัญในการแปรรูปแอลกอฮอล์ในร่างกาย ดังนั้นการขาดสังกะสีจึงอาจเพิ่มความโน้มเอียงที่จะเป็นโรคพิษสุราเรื้อรัง (โดยเฉพาะในเด็กและวัยรุ่น) เพื่อให้ร่างกายดูดซึมสังกะสีได้ดีขึ้น จำเป็นต้องมีวิตามิน A และ B 6

การขาดธาตุสังกะสีทำให้เกิดคนแคระ พัฒนาการทางเพศล่าช้า
สังกะสีส่วนเกินมีผลเสียต่อการทำงานของหัวใจและเลือด ไม่ใช่เรื่องบังเอิญที่เนื้อหาของสังกะสีในอาหารได้รับการควบคุมตามกนง.: อาหารสำหรับเด็กและอาหาร - 5.0 มก./กก.; น้ำมันพืช - 10.0 มก. / กก. โปรตีนถั่วเหลือง - 60.0 มก. / กก.
ในเซลล์และอวัยวะแต่ละส่วน ระหว่างการเปลี่ยนแปลงที่ร้ายแรง เนื้อหาของไอออนโลหะบางชนิดจะเพิ่มขึ้น ความเข้มข้นของสังกะสีเพิ่มขึ้นหลายเท่า สาเหตุยังไม่ทราบ แต่คาดว่าน่าจะใช้ การวินิจฉัยเบื้องต้นโรคมะเร็ง.
สังกะสีถูกขับออกจากร่างกายด้วยปัสสาวะ อุจจาระ เหงื่อ

แหล่งที่มาหลักของการเข้าสู่ร่างกาย
ผลิตภัณฑ์จากผัก: ผัก ข้าวโพด ถั่ว ผลิตภัณฑ์เบเกอรี่ เห็ด. ผลิตภัณฑ์จากสัตว์: เนื้อวัว, ตับ, เนื้อสัตว์, นม; อาหารทะเล (หอยนางรม, หอย, ปลาเฮอริ่ง)
การเชื่อมต่อที่พบบ่อยที่สุด
ZnS- ซิงค์ซัลไฟด์, ซิงค์เบลนด์
ZnSO 4 X 7H 2 O- ซิงค์ไฮโดรซัลเฟต, สังกะสีกรดกำมะถัน
ZnCl2- ซิงค์คลอไรด์
คุณรู้หรือไม่ว่า...
เป็นที่เชื่อกันว่าแร่สังกะสีเป็นที่รู้จักของคนมาตั้งแต่สมัยโบราณ ในศตวรรษที่สองก่อนคริสต์ศักราช ชาวกรีกรู้วิธีหลอมทองเหลืองซึ่งเป็นโลหะผสมของสังกะสีและทองแดงแล้ว ในอินเดียในศตวรรษที่ 12 มีการผลิตสังกะสีโลหะ แต่ในยุโรปก็ปรากฏขึ้นมากในภายหลัง นักโลหะวิทยาชาวแซ็กซอน I. Genkel อธิบายว่าสังกะสีเป็นโลหะ และในปี 1746 นักเคมีชาวเยอรมัน A. Marggraf ได้พัฒนาวิธีการในการรับสังกะสีจากแร่ธาตุ calamine และ sphalerite ZnS (zinc blende) ชื่อมาจากเขา สังกะสี- โลหะสีขาว
จำนวนอะตอมของสังกะสีในร่างกายมนุษย์คือ 2.2 x 10 22 และในเซลล์เดียว - 2.2 x 10 8
ปริมาณสังกะสีในร่างกายพร้อมอาหารต่อวันคือ 13 มก.
มีเอนไซม์ที่มีสังกะสีมากกว่า 200 ชนิด
สารแขวนลอย ซึ่งรวมถึงอินซูลิน โพรทามีน และซิงค์คลอไรด์ เป็นสารต้านเบาหวานที่มีประสิทธิภาพซึ่งทำงานได้ดีกว่าอินซูลินบริสุทธิ์
ในยาแผนปัจจุบัน สารประกอบสังกะสีใช้รักษาโรคภูมิคุ้มกันบกพร่อง ภาวะมีบุตรยาก โรคผิวหนัง ผม เล็บ และตับ ในรูปแบบของสารละลายสังกะสีคลอไรด์ ZnCl 2 ใช้เป็นสารกัดกร่อน, ครีมสังกะสี ZnO เป็นยาแห้ง, ยาสมานแผลและยาฆ่าเชื้อสำหรับโรคผิวหนัง, สังกะสีกรดกำมะถัน ZnSO 4 x 7H 2 O เป็นส่วนหนึ่งของยาหยอดตา
สารประกอบสังกะสีมีส่วนช่วยในการป้องกันโรคหวัดในเด็ก เพิ่มความอยากอาหาร การเจริญเติบโต พัฒนาการ เพิ่มความเข้มข้น
ยังมีต่อ
ทุกอย่างเริ่มต้นด้วยการสังเคราะห์ด้วยแสง เป็นเรื่องน่าแปลกที่ทราบว่าความสำคัญของแมกนีเซียมต่อร่างกายของเราและผลที่ตามมาของการขาดแมกนีเซียมนั้นเริ่มได้รับการประเมินในเวลาเดียวกันกับที่มีการค้นพบความลับของการสังเคราะห์ด้วยแสงของพืชเมื่อไม่กี่ทศวรรษที่แล้ว
กระบวนการสร้างอินทรียวัตถุอย่างต่อเนื่องเริ่มขึ้นเมื่อหลายพันล้านปีก่อน เมื่อเม็ดสีปรากฏขึ้นบนโลก ทำให้เกิดปฏิกิริยาเคมีโดยการดูดซับแสงแดด บทบาทชี้ขาดในเรื่องนี้เล่นโดยสาร "ไวแสง" จากกลุ่มที่เกิดขึ้นจากสารประกอบธรรมดา - และกลีเซอรอล อย่างไรก็ตาม ด้วยการปรากฏตัวของอนุพันธ์แมกนีเซียมของพอร์ไฟรินในรูปของคลอโรฟิลล์เท่านั้นที่ทำ ประวัติศาสตร์ธรรมชาติรูปแบบที่สูงขึ้นของชีวิตอินทรีย์ คลอโรฟิลล์มีความสามารถในการทำปฏิกิริยาโฟโตเคมีที่ไม่สามารถย้อนกลับได้ ซึ่งเป็นพลังงานที่สะสมอยู่ในสารประกอบทางชีวเคมีที่เสถียร
กระบวนการสังเคราะห์แสงเริ่มเป็นรูปเป็นร่างขึ้นในช่วงปลายยุคพรีแคมเบรียน (ประมาณ 1,000 ล้านปีก่อน) โครงสร้างของคลอโรฟิลล์นั้นใกล้เคียงกับโครงสร้างของ heme ซึ่งเป็นส่วนประกอบหลักของเม็ดเลือด ความแตกต่างก็คือ คลอโรฟิลล์ประกอบด้วยแมกนีเซียม (แมกนีเซียมไอออน) และฮีม เฮโมโกลบิน - (ไอออนของเหล็ก) การค้นพบนี้โดยศาสตราจารย์แห่งมหาวิทยาลัย Jagiellonian Leon Marklevsky ยืนยันความเชื่อมโยงระหว่างวิวัฒนาการของพืชและสัตว์
เราสามารถพูดได้ว่าสิ่งเดียวกันเกิดขึ้นกับบุคคลแม้ว่า ... ทุกอย่างซับซ้อนกว่ามาก คนเราไม่สามารถมีสุขภาพที่ดีได้หากมีแมกนีเซียมไม่เพียงพอในอาหาร ผู้เข้าร่วมการประชุมสภาคองเกรสเรื่องโรคที่เกิดจากการขาดแมกนีเซียมครั้งแรกได้ข้อสรุปนี้ การประชุมจัดขึ้นในเดือนพฤษภาคม 2514 ที่เมืองวิตเทล แมกนีเซียมไอออนมีบทบาทพิเศษในเกือบทุกกระบวนการที่เกิดขึ้นในร่างกาย ดังนั้นในกระบวนการสร้างภูมิคุ้มกันจึงทำหน้าที่เป็นสารต้านความเครียด ต้านพิษ ต้านภูมิแพ้ ต้านแอนาฟิแล็กติก (ชนิดแพ้ง่าย) ต้านการอักเสบ ป้องกันรังสีไอออไนซ์ ควบคุมอุณหภูมิ กระตุ้นและมีส่วนร่วมในการสร้าง ของแอนติบอดี้ แมกนีเซียมมีผลผ่อนคลายและลดความไวของร่างกาย ตอนนั้นเองที่การประชุมที่ Vittel ศาสตราจารย์ Dürlach กล่าวว่า "สัญญาณของโลกอารยะสมัยใหม่คือระดับแมกนีเซียมไอออนที่ลดลงเรื่อยๆ"
ดูเหมือนว่าโรคของอารยธรรมส่วนใหญ่เกิดจากการขาดแมกนีเซียมในร่างกายมนุษย์ ดังนั้นจึงควรค่าแก่การพิจารณาแมกนีเซียมอย่างใกล้ชิด
เราได้รับแมกนีเซียมจากดิน - ผ่านอาหารจากพืชและอาหารที่ได้จากสัตว์กินพืช แมกนีเซียมเข้าสู่ร่างกายของเรามากเท่ากับที่อยู่ในดิน
ในขณะเดียวกันมีแมกนีเซียมเพียงเล็กน้อยในดิน การขาดแมกนีเซียมพบได้ใน 40% ของดินแดนโปแลนด์ เนื้อหาเฉลี่ยใน 34% ของที่ดิน และเนื้อหาที่เพียงพอหรือสูงในน้อยกว่า 26% ปุ๋ยเทียมไม่ได้ทำให้ดินอุดมสมบูรณ์ด้วยแมกนีเซียมเลย หรือได้รับแมกนีเซียมน้อยเกินไป ตัวอย่างเช่น ในปี 2514-2518 ปริมาณแมกนีเซียมเฉลี่ยที่เติมลงในดินแดนโปแลนด์คือ 10-12 กิโลกรัมของแมกนีเซียมออกไซด์ (MgO) ต่อ 1 เฮกตาร์ของพื้นที่เพาะปลูก มันมากหรือน้อย? ข้าวสาลีที่ให้ผลผลิต 40 q/ha ควรได้รับจากดินประมาณ 17 กก. พร้อม MgO 1 เฮกตาร์ และหัวบีตที่ให้ผลผลิตเพียง 350 q/ha - ประมาณ 66 กก.
แน่นอนว่าปริมาณปุ๋ยแมกนีเซียมที่ต้องการนั้นขึ้นอยู่กับปริมาณแมกนีเซียมในดินและชนิดของพืชที่ปลูก โดยปกติแล้วจะอยู่ที่ 130 ถึง 260 กก./เฮกตาร์ จากปริมาณคีเซอไรต์นี้ (ปุ๋ยแมกนีเซียม) แมกนีเซียมออกไซด์ 30-60 กิโลกรัมและโพแทสเซียมออกไซด์ 15-31 กิโลกรัมจะผ่านเข้าไปในดิน ปุ๋ยคอกมีแมกนีเซียม 0.18% ซึ่งหมายความว่าถ้าเราใช้ปุ๋ยคอก 300 กก. ต่อ 1 เฮกตาร์ เราจะได้มกประมาณ 54 กก. นี้ไม่เพียงพออย่างแน่นอน
คลอโรฟิลล์ประกอบด้วยแมกนีเซียม 2.7% แมกนีเซียมไอออนควบคุมระดับความชุ่มชื้นของเซลล์ ด้วยการขาดแมกนีเซียมในพืช กระบวนการระเหยของน้ำจึงมีจำกัด และหากมากเกินไป พืชจะดูดซับน้ำอย่างเข้มข้น เพื่อให้ดินแห้งภายในระบบราก
สำหรับผู้ที่สนใจนี่คือตาราง
แร่ธาตุ.doc
แร่ธาตุ1. บทบาทของแร่ธาตุในร่างกายมนุษย์ 1
2. ธาตุอาหารหลัก ลักษณะของพวกมัน
3. ติดตามองค์ประกอบลักษณะของพวกเขา
4. อิทธิพลของการประมวลผลทางเทคโนโลยี
เกี่ยวกับองค์ประกอบแร่ธาตุของผลิตภัณฑ์อาหาร
5. วิธีการกำหนดสารแร่
1. บทบาทของแร่ธาตุในร่างกายมนุษย์
ธาตุหลายชนิดในรูปของเกลือแร่ ไอออน สารประกอบเชิงซ้อน และ อินทรียฺวัตถุเป็นส่วนหนึ่งของสิ่งมีชีวิตและเป็นสารอาหารที่จำเป็นที่ต้องบริโภคทุกวันพร้อมกับอาหาร เนื้อหาของแร่ธาตุในอาหารหลักแสดงไว้ในตาราง 5.1.
ตามคำแนะนำของคณะกรรมการควบคุมอาหาร สถาบันแห่งชาติสหรัฐอเมริกาการบริโภคองค์ประกอบทางเคมีในแต่ละวันควรอยู่ในระดับหนึ่ง (ตารางที่ 5.2) ต้องขับองค์ประกอบทางเคมีจำนวนเท่ากันทุกวันเนื่องจากเนื้อหาในองค์ประกอบนั้นค่อนข้างคงที่
บทบาทของแร่ธาตุในร่างกายมนุษย์มีความหลากหลายมาก แม้ว่าจะไม่ใช่องค์ประกอบสำคัญของโภชนาการก็ตาม สารแร่มีอยู่ในโปรโตปลาสซึมและของเหลวชีวภาพ ซึ่งมีบทบาทสำคัญในการทำให้มั่นใจว่าแรงดันออสโมติกคงที่ ซึ่งเป็นเงื่อนไขที่จำเป็นสำหรับการทำงานปกติของเซลล์และเนื้อเยื่อ พวกมันเป็นส่วนหนึ่งของสารประกอบอินทรีย์ที่ซับซ้อน (เช่น เฮโมโกลบิน ฮอร์โมน เอนไซม์) เป็นวัสดุพลาสติกสำหรับสร้างกระดูกและเนื้อเยื่อฟัน ในรูปของไอออน สารแร่มีส่วนในการส่งกระแสประสาท ทำให้เกิดการแข็งตัวของเลือด และกระบวนการทางสรีรวิทยาอื่นๆ ของร่างกาย
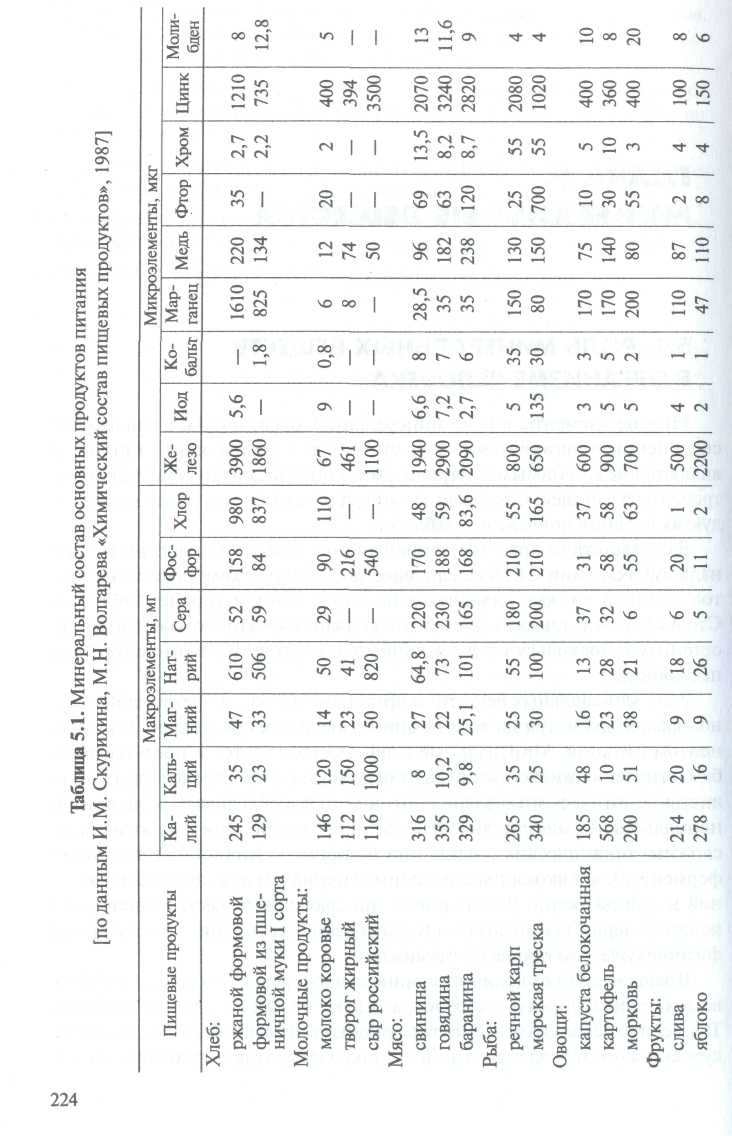 |
ขึ้นอยู่กับปริมาณแร่ธาตุในร่างกายมนุษย์และผลิตภัณฑ์อาหาร แบ่งออกเป็น มาโคร- และ องค์ประกอบการติดตามดังนั้น ถ้าเศษส่วนมวลของธาตุในร่างกายเกิน 10 -2% ก็ควรพิจารณาว่าเป็นองค์ประกอบมหภาค สัดส่วนของธาตุในร่างกายคือ 10 -3 -10 -5% หากเนื้อหาขององค์ประกอบต่ำกว่า 10 -5% จะถือว่าเป็นองค์ประกอบพิเศษ ธาตุอาหารหลัก ได้แก่ โพแทสเซียม โซเดียม แคลเซียม แมกนีเซียม ฟอสฟอรัส คลอรีน และกำมะถัน พวกมันอยู่ในปริมาณที่วัดได้เป็นร้อยและสิบมิลลิกรัมต่อเนื้อเยื่อหรืออาหาร 100 กรัม ธาตุติดตามเป็นส่วนหนึ่งของเนื้อเยื่อของร่างกายในระดับความเข้มข้นที่แสดงเป็นสิบ, ในร้อยและหนึ่งในพันของมิลลิกรัม และจำเป็นสำหรับการทำงานปกติ ธาตุตามเงื่อนไขแบ่งออกเป็นสองกลุ่มตามเงื่อนไข: อย่างแน่นอนหรือสำคัญ (โคบอลต์, เหล็ก, ทองแดง, สังกะสี, แมงกานีส, ไอโอดีน, โบรมีน, ฟลูออรีน) และสิ่งที่เรียกว่าอาจจำเป็น (อลูมิเนียม, สตรอนเทียม, โมลิบดีนัม, ซีลีเนียม, นิกเกิล, วานาเดียมและอื่น ๆ ). ธาตุที่ติดตามเรียกว่ามีความสำคัญหากขาดหรือขาดการทำงานปกติของร่างกายหยุดชะงัก
การกระจายของธาตุในร่างกายขึ้นอยู่กับของพวกเขา คุณสมบัติทางเคมีและหลากหลายมาก ตัวอย่างเช่น ธาตุเหล็ก เป็นส่วนสำคัญของฮีโมโกลบิน ไมโอโกลบิน และสารสีระบบทางเดินหายใจอื่น ๆ นั่นคือสารที่เกี่ยวข้องกับการดูดซึมและการขนส่งออกซิเจนไปยังเนื้อเยื่อทั้งหมดของร่างกาย อะตอมของทองแดงรวมอยู่ในศูนย์กลางการทำงานของเอ็นไซม์จำนวนหนึ่ง ฯลฯ
การกระทำขององค์ประกอบขนาดเล็กยังสามารถเป็นทางอ้อม - ผ่านอิทธิพลต่อความเข้มหรือธรรมชาติของเมแทบอลิซึม ดังนั้น จุลธาตุบางชนิด (เช่น แมงกานีส สังกะสี ไอโอดีน) ส่งผลต่อการเจริญเติบโต และการบริโภคอาหารไม่เพียงพอกับอาหารยับยั้งภาวะปกติ พัฒนาการทางร่างกายเด็ก. ธาตุอื่นๆ (เช่น โมลิบดีนัม ทองแดง แมงกานีส) มีส่วนเกี่ยวข้องกับการสืบพันธุ์ และการขาดธาตุในร่างกายส่งผลเสียด้านลบของชีวิตมนุษย์
ให้แร่ธาตุที่บกพร่องที่สุดในอาหาร ผู้ชายสมัยใหม่รวมถึงแคลเซียมและธาตุเหล็กส่วนเกิน - โซเดียมและฟอสฟอรัส
การขาดหรือมากเกินไปในอาหารของแร่ธาตุใด ๆ ทำให้เกิดการละเมิดการเผาผลาญโปรตีน, ไขมัน, คาร์โบไฮเดรต, วิตามินซึ่งนำไปสู่การพัฒนาของโรคต่างๆ ด้านล่างนี้คือลักษณะอาการ (โดยทั่วไป) ของการขาดองค์ประกอบทางเคมีต่างๆ ในร่างกายมนุษย์: ผลที่ตามมาจากความไม่สมดุลของปริมาณแคลเซียมและฟอสฟอรัสในอาหารคือฟันผุ กระดูกบาง การขาดฟลูออไรด์ในน้ำดื่ม เคลือบฟันถูกทำลาย การขาดสารไอโอดีนในอาหารและน้ำทำให้เกิดโรคไทรอยด์ ดังนั้นแร่ธาตุจึงมีความสำคัญมากสำหรับการกำจัดและป้องกันโรคต่างๆ


เราแสดงรายการสาเหตุของความผิดปกติของการเผาผลาญของสารแร่ที่อาจเกิดขึ้นได้แม้จะมีปริมาณเพียงพอในอาหาร:
A) โภชนาการที่ไม่สมดุล (โปรตีน, ไขมัน, คาร์โบไฮเดรต, วิตามิน, ฯลฯ ในปริมาณที่ไม่เพียงพอหรือมากเกินไป);
ข) การใช้กรรมวิธีในการประกอบอาหารทำให้สูญเสียแร่ธาตุ เช่น ในระหว่างการละลายน้ำแข็ง (ใน น้ำร้อน) เนื้อสัตว์ ปลา หรือเมื่อทำการต้มผักและผลไม้โดยที่เกลือที่ละลายน้ำได้ผ่านไป
C) การขาดการแก้ไของค์ประกอบของอาหารในเวลาที่เหมาะสมเมื่อความต้องการของร่างกายสำหรับแร่ธาตุที่เกี่ยวข้องกับการเปลี่ยนแปลงเหตุผลทางสรีรวิทยา เช่น คนทำงานในสภาวะ อุณหภูมิที่สูงขึ้นสภาพแวดล้อมภายนอกความต้องการโพแทสเซียมโซเดียมคลอรีนและแร่ธาตุอื่น ๆ เพิ่มขึ้นเนื่องจากส่วนใหญ่ขับออกจากร่างกายด้วยเหงื่อ
D) การละเมิดกระบวนการดูดซึมแร่ธาตุในทางเดินอาหารหรือการสูญเสียของเหลวที่เพิ่มขึ้น (เช่นการสูญเสียเลือด)
^
2. ธาตุอาหารหลัก ลักษณะของพวกมัน
แคลเซียม.เป็นองค์ประกอบโครงสร้างหลักของกระดูกและฟัน เป็นส่วนหนึ่งของนิวเคลียสของเซลล์ ของเหลวในเซลล์และเนื้อเยื่อ ซึ่งจำเป็นต่อการแข็งตัวของเลือด แคลเซียมก่อตัวเป็นสารประกอบที่มีโปรตีน ฟอสโฟลิปิด กรดอินทรีย์ มีส่วนร่วมในการควบคุมการซึมผ่านของเยื่อหุ้มเซลล์ในการส่งผ่านแรงกระตุ้นของเส้นประสาทในกลไกระดับโมเลกุลของการหดตัวของกล้ามเนื้อควบคุมกิจกรรมของเอนไซม์จำนวนหนึ่ง แคลเซียมไม่เพียงทำหน้าที่เกี่ยวกับพลาสติกเท่านั้น แต่ยังส่งผลต่อกระบวนการทางชีวเคมีและสรีรวิทยาในร่างกายอีกด้วย
แคลเซียมเป็นธาตุที่ย่อยยาก สารประกอบแคลเซียมที่เข้าสู่ร่างกายมนุษย์ด้วยอาหารจะไม่ละลายในน้ำ สภาพแวดล้อมที่เป็นด่างของลำไส้เล็กส่งเสริมการก่อตัวของสารประกอบแคลเซียมที่ย่อยไม่ได้และมีเพียงการกระทำของกรดน้ำดีเท่านั้นที่ดูดซึมได้
การดูดซึมแคลเซียมโดยเนื้อเยื่อไม่เพียงขึ้นอยู่กับปริมาณแคลเซียมในอาหารเท่านั้น แต่ยังขึ้นกับอัตราส่วนของแคลเซียมกับส่วนประกอบอาหารอื่นๆ และประการแรกคือไขมัน แมกนีเซียม ฟอสฟอรัส และโปรตีน ด้วยไขมันส่วนเกิน มีการแข่งขันกันสำหรับกรดน้ำดี และแคลเซียมส่วนสำคัญถูกขับออกจากร่างกายผ่านทางลำไส้ใหญ่ การดูดซึมแคลเซียมจะได้รับผลกระทบจากแมกนีเซียมที่มากเกินไป อัตราส่วนที่แนะนำขององค์ประกอบเหล่านี้คือ 1:0.5 หากปริมาณฟอสฟอรัสเกินระดับแคลเซียมในอาหารมากกว่า 2 เท่า เกลือที่ละลายน้ำได้จะเกิดขึ้น ซึ่งเลือดจะถูกสกัดจากเนื้อเยื่อกระดูก แคลเซียมเข้าสู่ผนังหลอดเลือดซึ่งทำให้เกิดความเปราะบางเช่นเดียวกับเข้าไปในเนื้อเยื่อของไตซึ่งสามารถนำไปสู่การเกิดนิ่วในไต สำหรับผู้ใหญ่ อัตราส่วนแคลเซียมและฟอสฟอรัสที่แนะนำในอาหารคือ 1:1.5 ความยากลำบากในการรักษาอัตราส่วนนี้เกิดจากการที่อาหารที่บริโภคโดยทั่วไปมีฟอสฟอรัสมากกว่าแคลเซียมมาก ไฟตินและกรดออกซาลิกที่มีอยู่ในผลิตภัณฑ์จากพืชหลายชนิดมีผลเสียต่อการดูดซึมแคลเซียม สารประกอบเหล่านี้สร้างเกลือที่ไม่ละลายน้ำกับแคลเซียม
ความต้องการแคลเซียมรายวันในผู้ใหญ่คือ 800 มก. และในเด็กและวัยรุ่น - 1,000 มก. หรือมากกว่า
ด้วยการบริโภคแคลเซียมไม่เพียงพอหรือละเมิดการดูดซึมในร่างกาย (โดยขาดวิตามินดี) จะเกิดภาวะขาดแคลเซียมขึ้น มีการขับออกจากกระดูกและฟันเพิ่มขึ้น ในผู้ใหญ่โรคกระดูกพรุนพัฒนา - การทำให้เนื้อเยื่อกระดูกไม่มีแร่ธาตุในเด็กการก่อตัวของโครงกระดูกถูกรบกวนและโรคกระดูกอ่อนพัฒนา
แหล่งแคลเซียมที่ดีที่สุด ได้แก่ นมและผลิตภัณฑ์จากนม ชีสต่างๆ และคอทเทจชีส (100-1000 มก. / 100 กรัมของผลิตภัณฑ์) หัวหอมสีเขียว ผักชีฝรั่ง ถั่ว พบแคลเซียมน้อยลงอย่างเห็นได้ชัดในไข่ เนื้อสัตว์ ปลา ผัก ผลไม้ ผลเบอร์รี่ (20-40 มก. / 100 กรัมของผลิตภัณฑ์)
แมกนีเซียม.องค์ประกอบนี้จำเป็นสำหรับการทำงานของเอ็นไซม์สำคัญจำนวนหนึ่ง เพื่อการเผาผลาญของร่างกาย แมกนีเซียมมีส่วนในการรักษาการทำงานปกติของระบบประสาทและกล้ามเนื้อหัวใจ มีผลขยายหลอดเลือด; กระตุ้นการหลั่งน้ำดี ยกขึ้น กิจกรรมมอเตอร์ลำไส้ซึ่งช่วยขับสารพิษออกจากร่างกาย (รวมถึงคอเลสเตอรอล)
การดูดซึมแมกนีเซียมถูกขัดขวางโดยการปรากฏตัวของไฟตินและไขมันส่วนเกินและแคลเซียมในอาหาร ความต้องการแมกนีเซียมในแต่ละวันนั้นไม่ได้กำหนดไว้อย่างแม่นยำ เป็นที่เชื่อกันว่าปริมาณ 200-300 มก. / วันช่วยป้องกันการสำแดงของการขาด (สันนิษฐานว่าประมาณ 30% ของแมกนีเซียมถูกดูดซึม)
หากขาดแมกนีเซียม การดูดซึมอาหารหยุดชะงัก การเจริญเติบโตล่าช้า แคลเซียมจะสะสมอยู่ที่ผนังหลอดเลือด และปรากฏการณ์ทางพยาธิวิทยาอื่นๆ อีกจำนวนหนึ่งพัฒนาขึ้น ในมนุษย์ การขาดแมกนีเซียมไอออนอันเนื่องมาจากธรรมชาติของสารอาหารนั้นไม่น่าเป็นไปได้อย่างยิ่ง อย่างไรก็ตามการสูญเสียองค์ประกอบนี้เป็นจำนวนมากอาจเกิดขึ้นกับอาการท้องร่วง ผลที่ตามมาจะรู้สึกได้หากมีการนำของเหลวที่ไม่มีแมกนีเซียมเข้าสู่ร่างกาย เมื่อความเข้มข้นของแมกนีเซียมในซีรัมลดลงเหลือประมาณ 0.1 mmol / l อาจเกิดอาการคล้ายอาการเพ้อคลั่ง: บุคคลมีอาการกึ่งโคม่า, การสั่นสะเทือนของกล้ามเนื้อ, กล้ามเนื้อกระตุกในข้อมือและเท้า, ความตื่นเต้นง่ายของกล้ามเนื้อเพิ่มขึ้นในการตอบสนองต่อเสียง , กลไก และสิ่งเร้าทางสายตา การแนะนำของแมกนีเซียมทำให้อาการดีขึ้นอย่างรวดเร็ว
แมกนีเซียมอุดมไปด้วยอาหารจากพืชเป็นหลัก จำนวนมากประกอบด้วยรำข้าวสาลี, ซีเรียลต่างๆ (40 - 200 มก. / 100 กรัมของผลิตภัณฑ์), พืชตระกูลถั่ว, แอปริคอต, แอปริคอตแห้ง, ลูกพรุน มีแมกนีเซียมเพียงเล็กน้อยในผลิตภัณฑ์นม เนื้อสัตว์ ปลา พาสต้า ผักและผลไม้ส่วนใหญ่ (20 - 40 มก. / 100 ก.)
โพแทสเซียม. โพแทสเซียมประมาณ 90% อยู่ภายในเซลล์ ร่วมกับเกลืออื่น ๆ ให้แรงดันออสโมติก มีส่วนร่วมในการส่งกระแสประสาท ระเบียบการเผาผลาญเกลือน้ำ ส่งเสริมการกำจัดน้ำและเป็นผลให้สารพิษออกจากร่างกาย รักษาสมดุลกรดเบสของสภาพแวดล้อมภายในของร่างกายมีส่วนร่วมในการควบคุมการทำงานของหัวใจและอวัยวะอื่น ๆ จำเป็นต่อการทำงานของเอ็นไซม์หลายชนิด
โพแทสเซียมถูกดูดซึมได้ดีจากลำไส้และส่วนเกินจะถูกลบออกจากร่างกายอย่างรวดเร็วด้วยปัสสาวะ ความต้องการโพแทสเซียมต่อวันในผู้ใหญ่คือ 2,000-4,000 มก. มันเพิ่มขึ้นด้วยเหงื่อออกมากด้วยการใช้ยาขับปัสสาวะโรคของหัวใจและตับ โพแทสเซียมไม่ใช่สารอาหารที่ขาดในอาหาร และการรับประทานอาหารที่หลากหลาย การขาดโพแทสเซียมจะไม่เกิดขึ้น การขาดโพแทสเซียมในร่างกายเกิดขึ้นเมื่อการทำงานของระบบประสาทและกล้ามเนื้อและระบบหัวใจและหลอดเลือดบกพร่อง, อาการง่วงนอน, ความดันโลหิตลดลง, และภาวะหัวใจเต้นผิดจังหวะ ในกรณีเช่นนี้จะมีการกำหนดอาหารโพแทสเซียม
โพแทสเซียมส่วนใหญ่มาจากอาหารจากพืช แหล่งที่อุดมสมบูรณ์ ได้แก่ แอปริคอต ลูกพรุน ลูกเกด ผักโขม สาหร่ายทะเล ถั่ว ถั่วลันเตา มันฝรั่ง ผักและผลไม้อื่นๆ (100 - 600 มก. / 100 กรัมของผลิตภัณฑ์) พบโพแทสเซียมน้อยในครีม, ข้าว, ขนมปังที่ทำจากแป้งพรีเมี่ยม (100 - 200 มก. / 100 ก.)
โซเดียม.โซเดียมมีอยู่ในเนื้อเยื่อและของเหลวในร่างกายทั้งหมด เขามีส่วนร่วมในการรักษาแรงดันออสโมติกในของเหลวในเนื้อเยื่อและเลือด ในการส่งกระแสประสาท การควบคุมความสมดุลของกรดเบสเมตาบอลิซึมของเกลือน้ำ เพิ่มการทำงานของเอนไซม์ย่อยอาหาร
การเผาผลาญโซเดียมได้รับการศึกษาอย่างกว้างขวางเนื่องจากคุณสมบัติทางสรีรวิทยาและความสำคัญต่อร่างกาย สารอาหารนี้ถูกดูดซึมได้ง่ายจากลำไส้ โซเดียมไอออนทำให้เกิดการบวมของคอลลอยด์เนื้อเยื่อ ซึ่งทำให้เกิดการกักเก็บน้ำในร่างกายและต่อต้านการปลดปล่อย ปริมาณโซเดียมทั้งหมดในของเหลวนอกเซลล์จึงกำหนดปริมาตรของของเหลวเหล่านี้ การเพิ่มขึ้นของความเข้มข้นของโซเดียมในพลาสมาทำให้รู้สึกกระหายน้ำ ในสภาพอากาศที่ร้อนจัดและระหว่างการออกกำลังกายอย่างหนัก เหงื่อออกโซเดียมจะสูญเสียไปอย่างมาก และจำเป็นต้องนำเกลือเข้าสู่ร่างกายเพื่อชดเชยปริมาณที่เสียไป
โดยทั่วไปโซเดียมไอออนจะเข้าสู่ร่างกายด้วยค่าใช้จ่ายของเกลือแกง - NaCl ด้วยการบริโภคโซเดียมคลอไรด์มากเกินไป การกำจัดผลิตภัณฑ์สุดท้ายที่ละลายน้ำได้ของการเผาผลาญผ่านทางไต ผิวหนัง และอวัยวะขับถ่ายอื่น ๆ จะแย่ลง การกักเก็บน้ำในร่างกายทำให้การทำงานของระบบหัวใจและหลอดเลือดซับซ้อนเพิ่มความดันโลหิต. ดังนั้นการบริโภคเกลือในโรคที่เกี่ยวข้องในอาหารจึงมีจำกัด อย่างไรก็ตาม เมื่อทำงานในร้านค้าร้อนหรือในสภาพอากาศร้อน ปริมาณโซเดียม (ในรูปของเกลือแกง) ที่นำเข้าจากภายนอกจะเพิ่มขึ้นเพื่อชดเชยการสูญเสียด้วยเหงื่อและลดเหงื่อออกซึ่งเป็นภาระในการทำงานของหัวใจ
โซเดียมมีอยู่ตามธรรมชาติในอาหารทุกชนิด วิธีการได้มาซึ่งผลิตภัณฑ์อาหารส่วนใหญ่จะกำหนดปริมาณโซเดียมในขั้นสุดท้าย ตัวอย่างเช่น ถั่วเขียวแช่แข็งมีโซเดียมมากกว่าถั่วสด ผักและผลไม้สดมีปริมาณน้อยกว่า 10 มก./กก. ถึง 1 กรัม/กก. ซึ่งแตกต่างจากซีเรียลและชีสซึ่งมีโซเดียมในปริมาณ 10-20 กรัม/กก.
การประมาณปริมาณโซเดียมที่บริโภคต่อวันโดยเฉลี่ยจากอาหารนั้นทำได้ยาก เนื่องจากความเข้มข้นของโซเดียมในอาหารนั้นแตกต่างกันอย่างมาก และนอกจากนี้ ผู้คนยังคุ้นเคยกับการเติมเกลือลงในอาหารอีกด้วย ผู้ใหญ่บริโภคเกลือแกงมากถึง 15 กรัมต่อวันและขับออกจากร่างกายในปริมาณเท่ากัน ปริมาณนี้มากเกินความจำเป็นทางสรีรวิทยามาก และถูกกำหนดโดยรสชาติของโซเดียมคลอไรด์เป็นหลัก นิสัยของอาหารรสเค็ม เนื้อหาของเกลือแกงในอาหารของมนุษย์สามารถลดลงได้ถึง 5 กรัมต่อวันโดยไม่เป็นอันตรายต่อสุขภาพ การปล่อยโซเดียมคลอไรด์ออกจากร่างกายและด้วยเหตุนี้ความต้องการจึงได้รับผลกระทบจากปริมาณเกลือโพแทสเซียมที่ร่างกายได้รับ อาหารจากพืชโดยเฉพาะมันฝรั่งนั้นอุดมไปด้วยโพแทสเซียมและเพิ่มการขับโซเดียมคลอไรด์ในปัสสาวะและทำให้ความต้องการเพิ่มขึ้น
ฟอสฟอรัส.ฟอสฟอรัสพบได้ในทุกเนื้อเยื่อของร่างกาย โดยเฉพาะกล้ามเนื้อและสมอง องค์ประกอบนี้เกี่ยวข้องกับกระบวนการชีวิตทั้งหมดของร่างกาย : การสังเคราะห์และการสลายตัวของสารในเซลล์ ระเบียบการเผาผลาญ เป็นส่วนหนึ่งของกรดนิวคลีอิกและเอนไซม์จำนวนหนึ่ง จำเป็นสำหรับการสร้าง ATP
ฟอสฟอรัสพบได้ในเนื้อเยื่อของร่างกายและผลิตภัณฑ์อาหารในรูปของกรดฟอสฟอริกและสารประกอบอินทรีย์ (ฟอสเฟต) มวลหลักของมันอยู่ในเนื้อเยื่อกระดูกในรูปของแคลเซียมฟอสเฟตส่วนที่เหลือของฟอสฟอรัสเป็นส่วนหนึ่งของเนื้อเยื่ออ่อนและของเหลว ในกล้ามเนื้อมีการแลกเปลี่ยนสารประกอบฟอสฟอรัสอย่างเข้มข้นที่สุด กรดฟอสฟอริกมีส่วนเกี่ยวข้องกับการสร้างโมเลกุลของเอนไซม์ กรดนิวคลีอิก เป็นต้น
ด้วยการขาดฟอสฟอรัสในอาหารเป็นเวลานาน ร่างกายจึงใช้ฟอสฟอรัสของตัวเองจากเนื้อเยื่อกระดูก สิ่งนี้นำไปสู่การลดแร่ธาตุของกระดูกและการละเมิดโครงสร้าง - การหายาก เมื่อร่างกายขาดฟอสฟอรัส สมรรถภาพทางกายและจิตใจจะลดลง เบื่ออาหาร ไม่รู้สึกตัว
ความต้องการรายวันสำหรับฟอสฟอรัสสำหรับผู้ใหญ่คือ 1200 มก. มันเพิ่มขึ้นด้วยความเครียดทางร่างกายหรือจิตใจที่ดีกับโรคบางชนิด
ฟอสฟอรัสจำนวนมากพบได้ในผลิตภัณฑ์จากสัตว์ โดยเฉพาะในตับ คาเวียร์ เช่นเดียวกับในซีเรียลและพืชตระกูลถั่ว เนื้อหาในผลิตภัณฑ์เหล่านี้มีตั้งแต่ 100 ถึง 500 มก. ต่อ 100 กรัมของผลิตภัณฑ์ แหล่งที่อุดมไปด้วยฟอสฟอรัสคือซีเรียล (ข้าวโอ๊ต ข้าวบาร์เลย์มุก) ซึ่งประกอบด้วยฟอสฟอรัส 300-350 มก. / 100 กรัม อย่างไรก็ตาม สารประกอบฟอสฟอรัสถูกดูดซึมจากผลิตภัณฑ์จากพืชได้แย่กว่าเมื่อรับประทานอาหารที่มาจากสัตว์
กำมะถัน.ความสำคัญขององค์ประกอบนี้ในด้านโภชนาการถูกกำหนดโดยประการแรกโดยข้อเท็จจริงที่ว่ามันเป็นส่วนหนึ่งของโปรตีนในรูปของกรดอะมิโนที่มีกำมะถัน (เมไทโอนีนและซีสทีน) และยังเป็นส่วนสำคัญของฮอร์โมนและวิตามินบางชนิดอีกด้วย
ในฐานะที่เป็นส่วนประกอบของกรดอะมิโนที่มีกำมะถันกำมะถันมีส่วนร่วมในกระบวนการเผาผลาญโปรตีนและความต้องการจะเพิ่มขึ้นอย่างรวดเร็วในระหว่างตั้งครรภ์และการเจริญเติบโตของร่างกายพร้อมกับการรวมโปรตีนในเนื้อเยื่อที่เกิดขึ้นตลอดจนในระหว่างการอักเสบ กระบวนการกรดอะมิโนที่มีกำมะถัน โดยเฉพาะอย่างยิ่งเมื่อใช้ร่วมกับวิตามิน C และ E มีฤทธิ์ต้านอนุมูลอิสระที่เด่นชัด นอกจากสังกะสีและซิลิกอนแล้ว กำมะถันเป็นตัวกำหนดสถานะการทำงานของเส้นผมและผิวหนัง
คลอรีน.องค์ประกอบนี้เกี่ยวข้องกับการก่อตัวของน้ำย่อย, การก่อตัวของพลาสม่า, กระตุ้นเอนไซม์จำนวนหนึ่ง สารอาหารนี้ถูกดูดซึมได้ง่ายจากลำไส้เข้าสู่กระแสเลือด ความสามารถของคลอรีนที่จะสะสมในผิวหนัง ตกค้างในร่างกายด้วยการบริโภคที่มากเกินไป และถูกขับออกด้วยเหงื่อในปริมาณมากเป็นสิ่งที่น่าสนใจ การขับคลอรีนออกจากร่างกายส่วนใหญ่เกิดขึ้นกับปัสสาวะ (90%) และเหงื่อ
การละเมิดในการแลกเปลี่ยนคลอรีนนำไปสู่การพัฒนาของอาการบวมน้ำการหลั่งน้ำย่อยไม่เพียงพอ ฯลฯ ปริมาณคลอรีนในร่างกายที่ลดลงอย่างรวดเร็วอาจนำไปสู่ภาวะร้ายแรงแม้กระทั่งความตาย การเพิ่มขึ้นของความเข้มข้นในเลือดเกิดขึ้นจากการคายน้ำของร่างกายเช่นเดียวกับการละเมิดการขับถ่ายของไต
ความต้องการคลอรีนต่อวันอยู่ที่ประมาณ 5,000 มก. คลอรีนเข้าสู่ร่างกายมนุษย์ส่วนใหญ่อยู่ในรูปของโซเดียมคลอไรด์เมื่อเติมลงในอาหาร
^
3. ติดตามองค์ประกอบลักษณะของพวกเขา
เหล็ก.องค์ประกอบนี้จำเป็นสำหรับการสังเคราะห์สารประกอบที่ให้การหายใจการสร้างเม็ดเลือด มันมีส่วนร่วมในปฏิกิริยาภูมิคุ้มกันและรีดอกซ์; เป็นส่วนหนึ่งของไซโตพลาสซึม นิวเคลียสของเซลล์ และเอ็นไซม์อีกจำนวนหนึ่ง
การดูดซึมธาตุเหล็กป้องกันได้ด้วยกรดออกซาลิกและไฟติน สำหรับการดูดซึมสารอาหารนี้จำเป็นต้องมีวิตามินบี 12 กรดแอสคอร์บิกยังมีส่วนช่วยในการดูดซึมธาตุเหล็ก เนื่องจากธาตุเหล็กถูกดูดซึมในรูปของไอออนไดวาเลนต์
^ การขาดธาตุเหล็กในร่างกายสามารถนำไปสู่การพัฒนาของโรคโลหิตจาง, การแลกเปลี่ยนก๊าซ, การหายใจของเซลล์นั่นคือกระบวนการพื้นฐานที่ทำให้ชีวิตหยุดชะงัก การพัฒนาของภาวะขาดธาตุเหล็กนั้นอำนวยความสะดวกโดย: การบริโภคธาตุเหล็กในร่างกายไม่เพียงพอในรูปแบบที่หลอมรวม, กิจกรรมการหลั่งของกระเพาะอาหารลดลง, การขาดวิตามิน (โดยเฉพาะ B 12 ,กรดโฟลิกและแอสคอร์บิก) และโรคหลายชนิดที่ทำให้เสียเลือด
ความต้องการธาตุเหล็กของผู้ใหญ่ (14 มก./วัน) เกินความต้องการโดยอาหารปกติ อย่างไรก็ตาม เมื่อใช้ขนมปังจากแป้งละเอียดที่มีธาตุเหล็กเพียงเล็กน้อยในอาหาร มักพบภาวะขาดธาตุเหล็กในคนเมือง ในเวลาเดียวกัน ควรคำนึงว่าผลิตภัณฑ์จากธัญพืชที่อุดมไปด้วยฟอสเฟตและไฟตินสร้างสารประกอบที่ละลายได้น้อยด้วยธาตุเหล็ก และลดการดูดซึมโดยร่างกาย
เหล็กเป็นธาตุที่แพร่หลาย พบในเครื่องใน, เนื้อสัตว์, ไข่, ถั่ว, ผัก, ผลเบอร์รี่ อย่างไรก็ตาม ในรูปแบบที่ย่อยง่าย ธาตุเหล็กพบได้เฉพาะในผลิตภัณฑ์จากเนื้อสัตว์ ตับ (มากถึง 2,000 มก. / 100 กรัมของผลิตภัณฑ์) ไข่แดง
ทองแดง. ทองแดงเป็นองค์ประกอบสำคัญในการเผาผลาญของมนุษย์ โดยมีบทบาทในการก่อตัวของเซลล์เม็ดเลือดแดง การปล่อยของเนื้อเยื่อเหล็ก และการพัฒนาของโครงกระดูก ระบบประสาทส่วนกลาง และเนื้อเยื่อเกี่ยวพัน
เนื่องจากทองแดงมีการแพร่กระจายอย่างกว้างขวางในอาหาร จึงไม่น่าเป็นไปได้ที่ผู้คนจะพัฒนารูปแบบของการขาดสารอาหารที่เกี่ยวข้องกับทองแดง ยกเว้นทารก ที่ทานอาหารจากนมล้วนๆ ยกเว้นทารก
การบริโภคทองแดงในปริมาณมากเกินไปโดยบุคคลทำให้เกิดการระคายเคืองและการพังทลายของเยื่อเมือก, ความเสียหายอย่างกว้างขวางต่อเส้นเลือดฝอย, ความเสียหายต่อตับและไต, และการระคายเคืองของระบบประสาทส่วนกลางความต้องการรายวันสำหรับองค์ประกอบนี้คือประมาณ 2 มก. แหล่งที่มาของทองแดง ได้แก่ อาหารเช่น ตับ ไข่แดง ผักใบเขียว
ไอโอดีน.ไอโอดีนเป็นองค์ประกอบสำคัญที่เกี่ยวข้องกับการก่อตัวของฮอร์โมนไทรอกซิน ด้วยการขาดสารไอโอดีนคอพอกพัฒนา - โรคของต่อมไทรอยด์
ความต้องการไอโอดีนอยู่ระหว่าง 100-150 ไมโครกรัมต่อวัน ปริมาณไอโอดีนในอาหารมักจะต่ำ (4-15 ไมโครกรัม%) อาหารทะเลมีไอโอดีนมากที่สุด ดังนั้นในปลาทะเล มันมีประมาณ 50 mcg / 100 g ในตับปลาถึง 800 ในสาหร่ายทะเลขึ้นอยู่กับชนิดและระยะเวลาของการรวบรวม - จาก 50 mcg ถึง 70,000 mcg / 100 g ของผลิตภัณฑ์ แต่ต้องคำนึงว่าในระหว่างการเก็บรักษาในระยะยาวและการรักษาความร้อนของอาหารจะสูญเสียไอโอดีนส่วนสำคัญ (จาก 20 ถึง 60%)
ปริมาณไอโอดีนในพืชบกและผลิตภัณฑ์จากสัตว์ขึ้นอยู่กับปริมาณในดินเป็นอย่างมาก ในพื้นที่ที่มีไอโอดีนน้อยในดิน ปริมาณไอโอดีนในผลิตภัณฑ์อาหารอาจน้อยกว่าค่าเฉลี่ย 10 ถึง 100 เท่า ดังนั้นในพื้นที่เหล่านี้เพื่อป้องกันโรคคอพอก ให้เติมโพแทสเซียมไอโอเดตเล็กน้อย (25 มก. ต่อเกลือ 1 กิโลกรัม) ลงในเกลือแกง อายุการเก็บรักษาของเกลือเสริมไอโอดีนนั้นไม่เกิน 6 เดือน เนื่องจากไอโอดีนจะค่อยๆ หายไประหว่างการเก็บรักษาเกลือ
ฟลูออรีน.เมื่อขาดองค์ประกอบนี้ ฟันผุก็พัฒนาขึ้น (การทำลายเคลือบฟัน) ฟลูออรีนที่มากเกินไปก็ส่งผลเสียต่อร่างกายเช่นกัน เนื่องจากเกลือฟลูออรีนที่สะสมอยู่ในกระดูกทำให้เกิดการเปลี่ยนแปลงในสีและรูปร่างของฟัน osteochondrosis และหลังจากการหยาบของข้อต่อและความไม่สามารถเคลื่อนไหวได้ การเติบโตของกระดูก ความแตกต่างระหว่างปริมาณฟลูออรีนที่มีประโยชน์และเป็นอันตรายนั้นน้อยมากจนนักวิจัยหลายคนไม่เห็นด้วยกับฟลูออไรด์ในน้ำ
ฟลูออรีนที่บริโภคกับน้ำจะถูกดูดซึมเกือบหมด ฟลูออรีนที่มีอยู่ในอาหารจะถูกดูดซึมได้ในระดับที่น้อยกว่า ฟลูออรีนที่ดูดซับจะกระจายไปทั่วร่างกายอย่างสม่ำเสมอ ส่วนใหญ่ยังคงอยู่ในโครงกระดูกและมีปริมาณเล็กน้อยสะสมอยู่ในเนื้อเยื่อทันตกรรม ในปริมาณที่สูง ฟลูออรีนอาจทำให้เกิดการละเมิดการเผาผลาญคาร์โบไฮเดรต ไขมัน โปรตีน เช่นเดียวกับการเผาผลาญวิตามิน เอนไซม์ และเกลือแร่
มีการประมาณการการบริโภคฟลูออไรด์จากอาหารในแต่ละวันในหลายประเทศ สำหรับผู้ใหญ่ ค่านี้จะแตกต่างกันไปตั้งแต่ 0.2 ถึง 3.1 มก. สำหรับเด็ก กลุ่มอายุตั้งแต่ 1 ถึง 3 ปี ปริมาณฟลูออไรด์ประมาณ 0.5 มก./วัน
ผลิตภัณฑ์อาหารเกือบทั้งหมดมีปริมาณธาตุนี้อย่างน้อย พืชพรรณทุกชนิดมีฟลูออรีนอยู่จำนวนหนึ่งซึ่งได้จากดินและน้ำ พบฟลูออไรด์ระดับสูงในอาหารบางชนิด โดยเฉพาะปลา ผักและชาบางชนิด การใช้น้ำที่มีฟลูออไรด์ในโรงงานแปรรูปอาหารมักจะเพิ่มระดับฟลูออไรด์ในผลิตภัณฑ์สำเร็จรูปเป็นสองเท่า
สำหรับป้องกันและรักษาโรคฟันผุ ยาสีฟันต่างๆ ผง ยาอายุวัฒนะ เคี้ยวหมากฝรั่งและของที่คล้ายกัน ซึ่งมีฟลูออรีนเพิ่ม ซึ่งส่วนใหญ่อยู่ในรูปแบบอนินทรีย์ สารประกอบเหล่านี้มักถูกรวมเข้าไว้ในยาสีฟัน โดยทั่วไปที่ความเข้มข้นประมาณ 1 กรัม/กก.
โครเมียม. องค์ประกอบนี้ดูเหมือนจะจำเป็นสำหรับการเผาผลาญกลูโคสและไขมัน และสำหรับการใช้กรดอะมิโนโดยบางระบบ เขายังมี ความสำคัญเพื่อป้องกันโรคเบาหวานชนิดไม่รุนแรงและโรคหลอดเลือดในมนุษย์
โครเมียมถูกดูดซึมทั้งจากทางเดินอาหารและจากทางเดินหายใจ ปริมาณที่ดูดซับไม่เหมือนกันสำหรับแต่ละระบบเหล่านี้และขึ้นอยู่กับรูปแบบของโครเมียม โครเมียมไตรวาเลนท์เป็นรูปแบบที่จำเป็นของธาตุสำหรับมนุษย์ โครเมียมเฮกซะวาเลนท์เป็นพิษ โครเมียมกระจายไปทั่วเนื้อเยื่อของร่างกายมนุษย์ในปริมาณที่ไม่เท่ากัน แต่มักจะมีความเข้มข้นต่ำ ระดับโครเมียมในเนื้อเยื่อทั้งหมดยกเว้นปอดจะลดลงตามอายุ โครเมียมจำนวนมากที่สุดในมนุษย์สะสมอยู่ในผิวหนัง กล้ามเนื้อ และเนื้อเยื่อไขมัน กลไก Homeostatic รวมถึงกลไกการขนส่งในตับและลำไส้ ป้องกันการสะสมของโครเมียมไตรวาเลนต์มากเกินไป โครเมียมถูกขับออกจากร่างกายอย่างช้าๆ โดยเฉพาะในปัสสาวะ
วันนี้ถือเป็นบรรทัดฐานของการบริโภคโครเมียมประมาณ 150 มก. ต่อวัน มีประโยชน์อย่างยิ่งสำหรับผู้สูงอายุที่ร่างกายดูดซึมคาร์โบไฮเดรตได้ไม่ดี และโครเมียมช่วยเพิ่มกระบวนการเผาผลาญอาหารของสารประกอบเฉพาะเหล่านี้ โครเมียมอนินทรีย์ถูกดูดซึมได้ไม่ดีและง่ายกว่ามาก - ในสารประกอบอินทรีย์นั่นคือในรูปแบบที่พบในสิ่งมีชีวิต
ผลิตภัณฑ์อาหารมีระดับโครเมียมแตกต่างกันมาก ซึ่งอยู่ในช่วง 20 ถึง 550 ไมโครกรัม/กก. แหล่งโครเมียมที่อุดมไปด้วย ได้แก่ ยีสต์ของผู้ผลิตเบียร์ ตับ (10-80 ไมโครกรัม/100 กรัม) ในปริมาณที่น้อยกว่าองค์ประกอบนี้พบได้ในมันฝรั่งที่มีหนัง, เนื้อวัว, ผักสด, ขนมปังโฮลวีต, ชีส
แมงกานีส.แมงกานีสมีความสำคัญในฐานะปัจจัยร่วมในระบบเอนไซม์จำนวนหนึ่ง มันมีบทบาทในการทำงานที่เหมาะสมของ flavoproteins ในการสังเคราะห์ sulfated mucopolysaccharides, คอเลสเตอรอล, เฮโมโกลบินและในกระบวนการเผาผลาญอื่น ๆ. ของแมงกานีสที่กินเข้าไปจะดูดซึมได้เพียง 3% เท่านั้น
การดูดซึมของแมงกานีสมีความสัมพันธ์อย่างใกล้ชิดกับการดูดซึมธาตุเหล็ก ความต้องการแมงกานีสคือ 0.2-0.3 มก. ต่อน้ำหนักมนุษย์ 1 กิโลกรัมต่อวัน แมงกานีสส่วนใหญ่พบในแครนเบอร์รี่และชา มีน้อยในเกาลัด โกโก้ ผัก ผลไม้ (100-200 mcg / 100 g)
^ นิกเกิล. นิกเกิลได้รับการยอมรับว่าเป็นธาตุที่จำเป็นเมื่อไม่นานนี้ ปัจจุบันมีบทบาทเป็นโคเอ็นไซม์ในกระบวนการเมแทบอลิซึมของธาตุเหล็ก ในเวลาเดียวกัน การเพิ่มขึ้นของปริมาณธาตุเหล็กในร่างกายจะมาพร้อมกับความต้องการอาหารนิกเกิลที่เพิ่มขึ้น นอกจากนี้ นิกเกิลยังมีส่วนช่วยในการดูดซึมทองแดง ซึ่งเป็นอีกองค์ประกอบหนึ่งที่ขาดไม่ได้สำหรับการสร้างเม็ดเลือด ความสำคัญของนิกเกิลในอาหารหรือนิกเกิลที่แยกได้จากผลิตภัณฑ์จากธรรมชาตินั้นเน้นย้ำโดยข้อเท็จจริงที่ว่าสารประกอบสังเคราะห์ขององค์ประกอบนี้เป็นสารก่อมะเร็ง
นิกเกิลมีอยู่ในอาหารส่วนใหญ่ แต่มีความเข้มข้นต่ำกว่า (และมักจะต่ำกว่ามาก) 1 มก./กก. การบริโภคนิกเกิลมีรายงานว่าอยู่ในช่วงน้อยกว่า 200 ถึง 900 ไมโครกรัมต่อวัน ด้วยอาหารปกติประมาณ 400 ไมโครกรัม / วันเข้ามา พบว่ามีปริมาณนิกเกิลในไวน์และเบียร์อยู่ที่ 100 และ 50 ไมโครกรัม/ลิตร ตามลำดับ
สังกะสี.องค์ประกอบการติดตามนี้เป็นโคเอ็นไซม์เกี่ยวข้องกับปฏิกิริยาการสังเคราะห์โปรตีนที่หลากหลาย (มากกว่า 70 รายการ) และเมแทบอลิซึมของกรดนิวคลีอิก (รวมถึงกระบวนการการจำลองและการถอดรหัสดีเอ็นเอ) ซึ่งรับประกันการเจริญเติบโตและวัยแรกรุ่นของร่างกายเป็นหลัก ในเวลาเดียวกัน สังกะสีพร้อมกับแมงกานีสเป็นองค์ประกอบเฉพาะที่ส่งผลต่อสถานะของการทำงานทางเพศ กล่าวคือ กิจกรรมของฮอร์โมนเพศบางชนิด การสร้างอสุจิ การพัฒนาของอวัยวะเพศชายและลักษณะทางเพศทุติยภูมิ นอกจากนี้ยังมีการพิจารณาบทบาทของสังกะสีในการป้องกันกระบวนการ hypertrophic ในต่อมลูกหมาก
สังกะสีร่วมกับกำมะถันมีส่วนเกี่ยวข้องกับการเจริญเติบโตและการต่ออายุของผิวหนังและเส้นผม นอกจากแมงกานีสและทองแดงแล้ว สังกะสียังมีส่วนช่วยอย่างมากในการรับรู้รสชาติและกลิ่นสังกะสีเป็นส่วนประกอบที่ขาดไม่ได้เป็นส่วนหนึ่งของโมเลกุลอินซูลิน และระดับของสังกะสีจะลดลงในผู้ป่วยเบาหวาน เป็นสิ่งสำคัญมากที่ธาตุนี้เป็นโคเอ็นไซม์ของแอลกอฮอล์ดีไฮโดรจีเนสซึ่งช่วยรับรองการเผาผลาญของเอทิลแอลกอฮอล์ ในขณะเดียวกันระดับการดูดซึมสังกะสีในโรคพิษสุราเรื้อรังเรื้อรังก็ลดลงอย่างรวดเร็ว อาการที่เรียกว่า "ตาบอดกลางคืน" (เช่น การมองเห็นไม่ชัดในตอนกลางคืน) สามารถพัฒนาได้ไม่เฉพาะในกรณีที่ไม่มีวิตามินเอ แต่ยังมีสังกะสีด้วย สังกะสีร่วมกับวิตามินบี 6 ช่วยให้การเผาผลาญกรดไขมันไม่อิ่มตัวและการสังเคราะห์พรอสตาแกลนดิน
สังกะสีมีความสำคัญมากต่อการย่อยอาหารและการดูดซึมสารอาหาร ดังนั้นสังกะสีจึงให้การสังเคราะห์เอนไซม์ย่อยอาหารที่สำคัญที่สุดในตับอ่อนและยังมีส่วนร่วมในการก่อตัวของ chylomicrons - อนุภาคขนส่งซึ่งไขมันในอาหารสามารถดูดซึมเข้าสู่กระแสเลือดได้ สังกะสีพร้อมกับวิตามินบีเป็นตัวควบคุมที่สำคัญของการทำงานของระบบประสาท ภายใต้เงื่อนไขของการขาดธาตุสังกะสี ความผิดปกติทางอารมณ์ ความไม่มั่นคงทางอารมณ์ ความหงุดหงิด และในกรณีที่รุนแรงมาก ความผิดปกติของสมองน้อยอาจเกิดขึ้นได้ ในที่สุดข้อมูลที่เพิ่มขึ้นเรื่อย ๆ เพื่อสนับสนุนการมีส่วนร่วมของสังกะสีในกระบวนการเจริญเติบโตของเซลล์เม็ดเลือดขาวและปฏิกิริยาของภูมิคุ้มกันของเซลล์
ความต้องการสังกะสีต่อวันคือ 8000-22000 mcg% เธอค่อนข้างพอใจกับอาหารปกติ ปริมาณสังกะสีที่บริโภคต่อวันโดยเฉลี่ยกับน้ำดื่มเพียงอย่างเดียวคือ 400 ไมโครกรัม ปริมาณสังกะสีในผลิตภัณฑ์อาหารมักอยู่ในช่วง 150-25000 mcg% อย่างไรก็ตามในตับ เนื้อสัตว์ และพืชตระกูลถั่ว จะสูงถึง 3000 - 5000 mcg% บางครั้ง ร่างกายของเด็กและวัยรุ่นที่บริโภคผลิตภัณฑ์จากสัตว์ไม่เพียงพออาจพบอาการขาดธาตุสังกะสีได้
^ ซีลีเนียม. แม้ในกลางศตวรรษที่ XX ซีลีเนียมไม่ได้ถูกพิจารณาโดยวิทยาศาสตร์โภชนาการเท่านั้น แต่ยังถือว่าเป็นองค์ประกอบที่เป็นพิษอย่างมากด้วยคุณสมบัติในการก่อมะเร็ง อย่างไรก็ตามในยุค 60 แล้ว พบว่า ด้วยการขาดซีลีเนียมระบบหัวใจและหลอดเลือดจะทนทุกข์ทรมาน ซึ่งแสดงออกโดยหลอดเลือดโปรเกรสซีฟและความอ่อนแอของกล้ามเนื้อหัวใจและในสภาวะของการขาดซีลีเนียมเรื้อรัง cardiomyopathy ที่รักษาไม่หายเกือบสามารถพัฒนาได้ ล่าสุดระดับ การวิจัยร่วมสมัยพบการยืนยันหนึ่งในข้อสังเกตที่สำคัญของการแพทย์แผนจีนโบราณระบุว่าการที่ร่างกายได้รับซีลีเนียมอย่างเพียงพอจะช่วยชะลอกระบวนการชราและทำให้มีอายุยืนยาว . เป็นที่น่าสนใจที่จะสังเกตว่าชาเขียวที่เป็นยาที่มีชื่อเสียงซึ่งจัดทำขึ้นโดยมีจุดประสงค์เพื่อให้มีสุขภาพและอายุยืนยาวในพระราชวังของจักรพรรดิใน จีนโบราณซึ่งปลูกในจังหวัดที่มีภูเขาเหล่านั้น ในดินที่มีปริมาณซีลีเนียมสูงอยู่แล้วโดยใช้วิธีการวิเคราะห์ที่ทันสมัย
หลังจากการค้นพบซีลีเนียม พบว่าวิตามินอีและซีลีเนียมทำหน้าที่ในส่วนต่างๆ ของกระบวนการเดียวกันและเป็นส่วนประกอบซึ่งกันและกันอย่างเคร่งครัด กล่าวคือ ฤทธิ์ต้านอนุมูลอิสระของวิตามินอีจะเพิ่มขึ้นอย่างมากเมื่อใช้ร่วมกัน การทำงานร่วมกันของสารต้านอนุมูลอิสระทั้งสองมีความสนใจเป็นพิเศษในบริบทของกิจกรรมต้านมะเร็ง ดังนั้นจึงแสดงให้เห็นว่าการเตรียมซีลีเนียมควบคู่ไปกับวิตามินอีช่วยเพิ่มผลการต้านมะเร็งของเนื้องอกในการทดลองอย่างมีนัยสำคัญ
การบริโภคซีลีเนียมกับอาหารขึ้นอยู่กับสภาวะและธรรมชาติของการบริโภคอาหารและระดับของซีลีเนียมในผลิตภัณฑ์อาหาร ผักและผลไม้มักเป็นแหล่งซีลีเนียมที่ไม่ดี ตรงกันข้ามกับธัญพืช ผลิตภัณฑ์จากธัญพืช เนื้อสัตว์ (โดยเฉพาะผลพลอยได้) อาหารทะเลซึ่งมีซีลีเนียมจำนวนมาก โดยทั่วไปแล้วน้ำหนักเปียกมากกว่า 0.2 มก./กก. . องค์ประกอบทางเคมีดินและปริมาณซีลีเนียมในเมล็ดพืชส่งผลกระทบอย่างมีนัยสำคัญต่อปริมาณซีลีเนียมในเมล็ดพืช โดยเปลี่ยนแปลงจาก 0.04 มก./กก. เป็น 21 มก./กก.
โมลิบดีนัมปริมาณโมลิบดีนัมในร่างกายของผู้ใหญ่ประมาณ 7 มก. ปริมาณโมลิบดีนัมในเลือดประมาณ 0.5 ไมโครกรัมต่อ 100 มล. พบความเข้มข้นที่สูงขึ้นของธาตุนี้ในผู้คนที่อาศัยอยู่ในบริเวณที่ดินอุดมไปด้วยสารประกอบของโลหะนี้มากที่สุด ดังนั้น ในบางภูมิภาคของอาร์เมเนีย มักพบกรณีของโรคเกาต์ในหมู่ผู้อยู่อาศัยที่กินผลิตภัณฑ์ในท้องถิ่นเป็นหลัก ซึ่งพบโมลิบดีนัมในระดับสูงมาก เนื้อหาในอาหารของชาวภูมิภาคนี้คือ 10-15 มก. ในพื้นที่อื่นๆ ที่กรณีของโรคเกาต์พบได้น้อย ผู้คนได้รับโมลิบดีนัมเพียง 1-2 มก. ต่อวันจากอาหาร
โมลิบดีนัมเป็นส่วนสำคัญของเอนไซม์หลายชนิด เช่น แซนทีนออกซิเดส อัลดีไฮด์ออกซิเดส ซัลเฟตออกซิเดส เป็นที่ทราบกันว่าโมลิบดีนัมยับยั้งการเกิดฟันผุ
ความต้องการโมลิบดีนัมต่อวันโดยประมาณคือ 2 ไมโครกรัมต่อน้ำหนักตัว 1 กิโลกรัม ในรัสเซียปริมาณโมลิบดีนัมต่อวันคือ 0.27 มก.
โมลิบดีนัมที่ร่ำรวยที่สุด ประเภทต่างๆผัก (เช่น พืชตระกูลถั่ว) และอวัยวะภายในของสัตว์
โคบอลต์.ผลกระทบทางชีวภาพของโคบอลต์เป็นที่รู้จักกันมาตั้งแต่ปี 2491 เมื่อนักวิทยาศาสตร์ Rickes and Smith พบว่าอะตอมของโคบอลต์เป็นศูนย์กลางในโมเลกุลของวิตามินบี 12 ความเข้มข้นสูงสุดของโคบอลต์ในเนื้อเยื่อคือประมาณ 100 ไมโครกรัมต่อกิโลกรัม ปริมาณโคบอลต์ทั้งหมดในร่างกายของผู้ใหญ่คือ 5 มก. คนที่ทานอาหารทุกวันจะได้รับโคบอลต์ 5.63 -7.94 ไมโครกรัมซึ่งดูดซึมได้ 73 - 97%
ความต้องการโคบอลต์โดยเฉลี่ยต่อวันคือ 60 ไมโครกรัมต่อน้ำหนักตัว 1 กิโลกรัม เป็นที่เชื่อกันว่าคนต้องการโคบอลต์เฉพาะในรูปของไซยาโนโคบาลามิน (วิตามินบี 12) ในบางประเทศ สารประกอบโคบอลต์ถูกใช้เป็นสารเติมแต่งอาหารให้กับเบียร์เพื่อทำให้ฟองคงที่ อย่างไรก็ตามปรากฎว่าสารเติมแต่งดังกล่าวเป็นสาเหตุของโรคหัวใจในผู้บริโภคเบียร์ ดังนั้นการใช้สารประกอบโคบอลต์เป็นสารเติมแต่งอาหารจึงถูกยกเลิก
^
4 ผลกระทบของการแปรรูปต่อองค์ประกอบแร่ธาตุของอาหาร
ในการแปรรูปวัตถุดิบอาหารตามกฎจะมีปริมาณแร่ธาตุลดลง (ยกเว้น Na ที่เติมในรูปของเกลืออาหาร) ในอาหารจากพืชจะสูญเสียไปกับของเสีย ดังนั้นปริมาณของมาโครและโดยเฉพาะอย่างยิ่งไมโครอิลิเมนต์ในระหว่างการผลิตซีเรียลและแป้งหลังจากการแปรรูปเมล็ดพืชลดลง เนื่องจากมีส่วนประกอบเหล่านี้ในเปลือกและเชื้อโรคที่ถูกดึงออกมากกว่าในเมล็ดพืชทั้งเมล็ด การวิเคราะห์เปรียบเทียบองค์ประกอบแร่ธาตุในแป้งสาลีเกรดสูงสุดและแป้งจากธัญพืชไม่ขัดสีแสดงไว้ด้านล่าง (เนื้อหาขององค์ประกอบแสดงเป็นมิลลิกรัม / 100 กรัมของผลิตภัณฑ์):
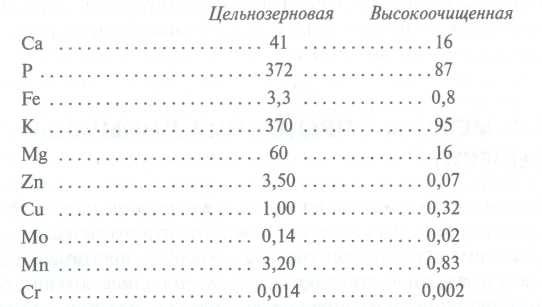
ตัวอย่างเช่น โดยเฉลี่ยแล้ว เมล็ดข้าวสาลีและข้าวไรย์มีส่วนประกอบของเถ้าประมาณ 1.7% ในขณะที่อยู่ในแป้ง ขึ้นอยู่กับความหลากหลาย ตั้งแต่ 0.5 (ในระดับสูงสุด) ถึง 1.5% (ในโฮลมีล) เมื่อทำความสะอาดผักและมันฝรั่ง แร่ธาตุ 10 ถึง 30% จะหายไป หากอยู่ภายใต้การปรุงอาหารด้วยความร้อนก็ขึ้นอยู่กับเทคโนโลยี (การทำอาหาร, การทอด, การเคี่ยว) อีก 5 ถึง 30% จะหายไป
เนื้อสัตว์ ผลิตภัณฑ์จากปลา และเนื้อสัตว์ปีกส่วนใหญ่สูญเสียธาตุอาหารหลัก เช่น แคลเซียมและฟอสฟอรัส ในระหว่างการแยกเนื้อออกจากกระดูก
ในระหว่างการปรุงอาหารด้วยความร้อน (ต้ม ทอด ตุ๋น) เนื้อสัตว์จะสูญเสียแร่ธาตุ 5 ถึง 50% อย่างไรก็ตาม หากดำเนินการแปรรูปต่อหน้ากระดูกที่มีแคลเซียมจำนวนมาก ก็สามารถเพิ่มปริมาณแคลเซียมในผลิตภัณฑ์จากเนื้อสัตว์ปรุงสุกได้ถึง 20%
ในกระบวนการทางเทคโนโลยี เนื่องจากอุปกรณ์คุณภาพสูงไม่เพียงพอ ไมโครอิลิเมนต์จำนวนหนึ่งจึงสามารถผ่านเข้าไปในผลิตภัณฑ์ขั้นสุดท้ายได้ ดังนั้นเมื่อทำขนมปัง ระหว่างการเตรียมแป้งอันเป็นผลมาจากการสัมผัสแป้งกับอุปกรณ์ ปริมาณธาตุเหล็กสามารถเพิ่มขึ้น 30% กระบวนการนี้ไม่พึงปรารถนา เนื่องจากองค์ประกอบที่เป็นพิษซึ่งอยู่ในรูปของสิ่งสกปรกในโลหะยังสามารถผ่านเข้าไปในผลิตภัณฑ์พร้อมกับเหล็กได้เมื่ออาหารกระป๋องถูกเก็บไว้ในกระป๋องสำเร็จรูป (ซึ่งก็คือการบัดกรี) กระป๋องที่มีการบัดกรีคุณภาพต่ำ หรือหากชั้นเคลือบเงาป้องกันแตก ส่วนประกอบที่เป็นพิษสูง เช่น ตะกั่ว แคดเมียม และดีบุกสามารถผ่านเข้าไปในผลิตภัณฑ์ได้
ควรคำนึงว่าโลหะจำนวนหนึ่ง เช่น เหล็กและทองแดง แม้ในระดับความเข้มข้นเล็กน้อย ก็สามารถทำให้เกิดออกซิเดชันของผลิตภัณฑ์ที่ไม่พึงประสงค์ได้ ความสามารถในการออกซิไดซ์ของตัวเร่งปฏิกิริยามีความเด่นชัดโดยเฉพาะอย่างยิ่งในความสัมพันธ์กับไขมันและผลิตภัณฑ์ที่เป็นไขมัน ตัวอย่างเช่น ที่ความเข้มข้นของธาตุเหล็กสูงกว่า 1.5 มก./กก. และทองแดง 0.4 มก./กก. ในระหว่างการเก็บรักษาเนยและมาการีนในระยะยาว โลหะเหล่านี้ทำให้เกิดกลิ่นหืนของผลิตภัณฑ์ เมื่อเก็บเครื่องดื่มในที่ที่มีธาตุเหล็กมากกว่า 5 มก./ลิตร และทองแดง 1 มก./ลิตร ภายใต้เงื่อนไขบางประการ มักจะสังเกตเห็นความขุ่นของเครื่องดื่มได้
^
5. วิธีการกำหนดสารแร่
สำหรับการวิเคราะห์สารแร่ส่วนใหญ่จะใช้วิธีทางเคมีกายภาพ - ทางแสงและไฟฟ้าเคมี
วิธีการเกือบทั้งหมดเหล่านี้จำเป็นต้องมีการเตรียมตัวอย่างเป็นพิเศษเพื่อการวิเคราะห์ ซึ่งประกอบด้วยการทำให้เป็นแร่ในเบื้องต้นของวัตถุที่ศึกษา การทำให้เป็นแร่สามารถทำได้สองวิธี: "แห้ง" และ "เปียก" การทำให้เป็นแร่ "แห้ง" เกี่ยวข้องกับการทำให้เป็นถ่าน การเผา และการเผาตัวอย่างทดสอบภายใต้เงื่อนไขบางประการ การทำให้เป็นแร่ "เปียก" ยังให้การประมวลผลของวัตถุของการศึกษา กรดเข้มข้น(ส่วนใหญ่มักเป็น HNO 3 และ H 2 SO 4)
^ วิธีการวิเคราะห์สเปกตรัม
Photoelectrocolorimetry - การวิเคราะห์ตามการวัดการดูดกลืนโดยสารละลายสีของรังสีเอกรงค์ในบริเวณที่มองเห็นได้ของสเปกตรัม การวัดจะดำเนินการโดยใช้โฟโตอิเล็กทริกคัลเลอริมิเตอร์ที่ติดตั้งฟิลเตอร์วงแคบ หากสารทดสอบไม่มีสี จะต้องถูกแปลงเป็นสารประกอบที่มีสีโดยปฏิกิริยาเคมีกับรีเอเจนต์บางชนิด (ปฏิกิริยาวิเคราะห์เชิงแสง)
สเปกโตรโฟโตเมตรีเป็นวิธีการวิเคราะห์โดยอาศัยการวัดการดูดกลืนรังสีเอกรงค์ในบริเวณอัลตราไวโอเลต ที่มองเห็นได้ และอินฟราเรดของสเปกตรัม การวัดดังกล่าวดำเนินการโดยใช้เครื่องสเปกโตรโฟโตมิเตอร์ ซึ่งใช้ปริซึมแบบกระจายและตะแกรงกระจายแสงเป็นโมโนโครมาไทเซอร์
การวิเคราะห์เชิงปริมาณของไอออนภายใต้การศึกษามักจะดำเนินการโดยใช้วิธีเส้นโค้งการสอบเทียบ
การวิเคราะห์สเปกตรัมการปล่อยวิธีการวิเคราะห์สเปกตรัมการปล่อยจะขึ้นอยู่กับการวัดความยาวคลื่น ความเข้ม และลักษณะอื่นๆ ของแสงที่ปล่อยออกมาจากอะตอมและไอออนของสารในสถานะก๊าซ การวิเคราะห์สเปกตรัมการปล่อยก๊าซทำให้สามารถกำหนดองค์ประกอบองค์ประกอบของสารอนินทรีย์และอินทรีย์ได้
ความเข้มของเส้นสเปกตรัมถูกกำหนดโดยจำนวนของอะตอมที่ถูกกระตุ้นในแหล่งกำเนิดการกระตุ้น ซึ่งไม่เพียงแต่ขึ้นอยู่กับความเข้มข้นขององค์ประกอบในตัวอย่างเท่านั้น แต่ยังขึ้นกับสภาวะของการกระตุ้นด้วย ด้วยการทำงานที่เสถียรของแหล่งกำเนิดการกระตุ้น ความสัมพันธ์ระหว่างความเข้มของเส้นสเปกตรัมและความเข้มข้นขององค์ประกอบ (หากมีขนาดเล็กเพียงพอ) จะเป็นเส้นตรง กล่าวคือ ใน กรณีนี้การวิเคราะห์เชิงปริมาณสามารถทำได้โดยใช้วิธีโค้งสอบเทียบ
แอปพลิเคชั่นที่ยิ่งใหญ่ที่สุดในฐานะแหล่งกำเนิดของการกระตุ้นได้รับอาร์คไฟฟ้า, ประกายไฟ, เปลวไฟ อุณหภูมิของส่วนโค้งสูงถึง 5,000 - 6000 ° C ในส่วนโค้ง สามารถรับสเปกตรัมขององค์ประกอบเกือบทั้งหมดได้ ด้วยการปล่อยประกายไฟ อุณหภูมิ 7000 - 10,000 ° C พัฒนาและองค์ประกอบทั้งหมดตื่นเต้น เปลวไฟให้สเปกตรัมการแผ่รังสีที่สว่างและเสถียรเพียงพอ วิธีการวิเคราะห์โดยใช้เปลวไฟเป็นแหล่งกระตุ้น เรียกว่า การวิเคราะห์การปล่อยเปลวไฟ วิธีนี้จะกำหนดองค์ประกอบมากกว่าสี่สิบธาตุ (อัลคาไลน์และดินอัลคาไลน์, Cu 2 , Mn 2 เป็นต้น)
^ สเปกโตรสโคปีการดูดซึมอะตอม . วิธีการนี้ขึ้นอยู่กับความสามารถของอะตอมอิสระของธาตุในก๊าซเปลวไฟในการดูดซับพลังงานแสงที่ความยาวคลื่นที่มีลักษณะเฉพาะของแต่ละธาตุ
ในสเปกโตรสโคปีการดูดกลืนอะตอม ความเป็นไปได้ของการซ้อนทับเส้นสเปกตรัมขององค์ประกอบต่าง ๆ นั้นถูกแยกออกจากกันเกือบทั้งหมด เนื่องจากจำนวนในสเปกตรัมนั้นน้อยกว่าในสเปกโทรสโกปีการแผ่รังสีมาก
การลดลงของความเข้มของรังสีเรโซแนนซ์ภายใต้สภาวะของอะตอมมิคดูดกลืนสเปกโทรสโกปีเป็นไปตามกฎเลขชี้กำลังของความเข้มที่ลดลงขึ้นอยู่กับความหนาของชั้นและความเข้มข้นของสาร คล้ายกับกฎของโบเกอร์-แลมเบิร์ต-เบียร์
ความคงตัวของความหนาของชั้นดูดซับแสง (เปลวไฟ) ทำได้โดยใช้หัวเผาที่มีการออกแบบพิเศษ วิธีการวิเคราะห์สเปกตรัมดูดกลืนแสงของอะตอมถูกนำมาใช้กันอย่างแพร่หลายในการวิเคราะห์วัตถุทางเทคนิคหรือทางธรรมชาติเกือบทุกชนิด โดยเฉพาะอย่างยิ่งในกรณีที่จำเป็นต้องกำหนดองค์ประกอบจำนวนเล็กน้อย
วิธีการตรวจวัดการดูดกลืนอะตอมได้รับการพัฒนาสำหรับธาตุมากกว่า 70 ธาตุ
^ 2. วิธีการวิเคราะห์ทางไฟฟ้าเคมี
ไอโอโนเมทรี วิธีการนี้ใช้เพื่อกำหนด K ไอออน , นา , Ca 2 , Mn 2 , F - , ฉัน - , สล - ฯลฯ
วิธีการนี้ขึ้นอยู่กับการใช้อิเล็กโทรดแบบคัดเลือกไอออนซึ่งเมมเบรนสามารถซึมผ่านไปยังไอออนบางชนิดได้ (ดังนั้นตามกฎแล้วการเลือกสูงของวิธีการ)
เนื้อหาเชิงปริมาณของไอออนที่กำหนดหาได้กระทำโดยใช้กราฟการปรับเทียบ ซึ่งแสดงไว้ในพิกัด E - pC หรือโดยวิธีการเพิ่มเติม แนะนำให้ใช้วิธีการเติมมาตรฐานสำหรับการวัดค่าไอออนในระบบที่ซับซ้อนซึ่งมีสารแปลกปลอมที่มีความเข้มข้นสูง
โพลาโรกราฟีวิธีการโพลาโรกราฟีกระแสสลับใช้เพื่อกำหนดองค์ประกอบที่เป็นพิษ (ปรอท แคดเมียม ตะกั่ว ทองแดง เหล็ก)
วิธีการนี้ขึ้นอยู่กับการศึกษาเส้นโค้งแรงดันกระแสที่ได้รับระหว่างอิเล็กโทรลิซิสของสารอิเล็กโตรออกซิไดซ์หรือสารอิเล็กโตรรีดิวซิ่ง ในฐานะที่เป็นอิเล็กโทรดตัวบ่งชี้ในโพลาโรกราฟี มักใช้อิเล็กโทรดแบบหยดของปรอท ซึ่งบางครั้งอาจเป็นไมโครอิเล็กโทรดที่เป็นของแข็ง เช่น แพลตตินั่ม กราไฟต์ ในฐานะที่เป็นอิเล็กโทรดอ้างอิง ปรอทที่เทลงที่ด้านล่างของอิเล็กโทรไลเซอร์หรือใช้คาโลเมลแบบครึ่งเซลล์อิ่มตัว
เมื่อแรงดันไฟฟ้าเพิ่มขึ้น จะมีช่วงเวลาที่ไอออนทั้งหมดเข้าสู่อิเล็กโทรดเนื่องจากการแพร่ระบาดในทันที และความเข้มข้นของไอออนในชั้นใกล้อิเล็กโทรดจะคงที่และเกือบเท่ากับศูนย์ กระแสที่ไหลในวงจรในเวลานี้เรียกว่ากระแสการแพร่กระจายจำกัด
การวิเคราะห์เชิงปริมาณเชิงปริมาณขึ้นอยู่กับการใช้ direct การพึ่งพาอาศัยกันตามสัดส่วนขนาดของกระแสการแพร่ต่อความเข้มข้นขององค์ประกอบที่ถูกกำหนด
^ แร่ธาตุ
ธาตุแร่ (เถ้า) พบได้ในผลิตภัณฑ์อาหารในรูปแบบของสารประกอบอินทรีย์และอนินทรีย์ พบได้ในสารอินทรีย์หลายชนิด
สารของคลาสต่างๆ - โปรตีน, ไขมัน, ไกลโคไซด์, เอ็นไซม์ ฯลฯ โดยปกติองค์ประกอบแร่ธาตุจะถูกกำหนดในขี้เถ้าหลังจากการเผาไหม้ของผลิตภัณฑ์อาหารเนื่องจากเป็นการยากที่จะระบุว่าสารใดและปริมาณขององค์ประกอบเหล่านี้รวมอยู่ด้วย
บทบาทของแร่ธาตุในชีวิตของมนุษย์ สัตว์ และพืชมีมากมายมหาศาล: กระบวนการทางสรีรวิทยาทั้งหมดในสิ่งมีชีวิตดำเนินไปโดยมีส่วนร่วมขององค์ประกอบเหล่านี้ ดังนั้นในร่างกายมนุษย์และสัตว์ แร่ธาตุจึงมีส่วนร่วมในกระบวนการพลาสติก การก่อตัวและการสร้างเนื้อเยื่อ ในการเผาผลาญของน้ำ ในการรักษาแรงดันออสโมติกของเลือดและของเหลวอื่นๆ ในร่างกาย ในการรักษาสมดุลของกรด-เบสในร่างกาย และ รวมอยู่ในความซับซ้อนของสารที่ประกอบเป็นเซลล์โปรโตพลาสซึมที่มีชีวิตในองค์ประกอบของต่อมไร้ท่อ ฯลฯ
องค์ประกอบแร่ธาตุของสิ่งมีชีวิตเปลี่ยนแปลงไปตามอายุ เมื่ออายุมากขึ้นจะสังเกตเห็นการทำให้เป็นแร่ของสิ่งมีชีวิต ดังนั้นเด็กแรกเกิดจึงมีแร่ธาตุประมาณ 34 กรัมต่อน้ำหนักตัว 1 กิโลกรัมในผู้ใหญ่เนื้อหาของสารเหล่านี้จะเพิ่มขึ้นเป็น 43 กรัมหรือมากกว่า
พบแร่ธาตุมากกว่า 70 ชนิดในร่างกายมนุษย์และสัตว์ กระบวนการทางเอนไซม์หลายอย่างที่เกิดขึ้นในเนื้อเยื่อต่างๆ ของร่างกายต้องการการมีส่วนร่วมของแร่ธาตุหลายชนิด ดังนั้น สำหรับการเปลี่ยนกรดไพรูวิกเป็นกรดอะซิติกหรือกลูโคสเป็นฟรุกโตสหรือฟอสโฟกลีเซอรอลเป็นกลูโคส-6-มานโนส-6- และฟรุกโตส-6-ฟอสเฟต การมีส่วนร่วมของไอออนแมกนีเซียมจึงเป็นสิ่งจำเป็น แคลเซียมไอออนยับยั้งการพัฒนากระบวนการนี้
แร่ธาตุมีการกระจายอย่างไม่สม่ำเสมอในเนื้อเยื่อของร่างกายมนุษย์ ในเนื้อเยื่อแข็ง ธาตุสองธาตุมีอิทธิพลเหนือ: แคลเซียม (Ca) และแมกนีเซียม (Mg) และในเนื้อเยื่ออ่อน - องค์ประกอบโมโนวาเลนต์: โพแทสเซียม (K) และโซเดียม (Na) นอกจากนี้ ฟอสฟอรัส (P) จำนวนมากยังสะสมอยู่ในเนื้อเยื่อแข็ง ซึ่งส่วนใหญ่อยู่ในรูปของเกลือฟอสเฟต ด้วยการขาดแร่ธาตุในอาหาร สารประกอบเหล่านี้จะถูกขับออกจากร่างกายและการเผาผลาญตามปกติจะหยุดชะงัก
สารแร่ที่ละลายในพลาสมาในเลือด ของเหลวระหว่างเซลล์ และของเหลวในร่างกายอื่นๆ จะสร้างแรงดันออสโมติก ซึ่งขึ้นอยู่กับความเข้มข้นของโมลาร์ของสารที่ละลายในของเหลว เกลือเพิ่มแรงดันออสโมติกในระดับที่สูงขึ้น
มากกว่าอิเล็กโทรไลต์ที่ไม่ใช่อิเล็กโตรไลต์ที่ความเข้มข้นโมลาร์เท่ากัน เนื่องจากเกลือแยกตัวออกมาเป็นไอออน แรงดันออสโมติกขึ้นอยู่กับจำนวนโมเลกุลและไอออนที่ไม่แยกตัวออกจากกัน แรงดันออสโมติกของเลือด น้ำเหลือง และของเหลวระหว่างเซลล์ของร่างกายมนุษย์และสัตว์ขึ้นอยู่กับโซเดียมคลอไรด์ (NaCl) ที่ละลายอยู่ในนั้นเป็นหลัก
แรงดันออสโมติกในของเหลวในร่างกายส่งผลต่อการกระจายของน้ำและตัวละลายในเนื้อเยื่อ ในสัตว์ที่สูงกว่า แรงดันออสโมติกจะคงที่และมีค่าเท่ากับ 7.5 - 9.0 atm การรักษาแรงดันออสโมติกให้คงที่นั้นทำได้โดยการทำงานของอวัยวะขับถ่าย ซึ่งส่วนใหญ่เป็นไตและต่อมเหงื่อ
การป้อนเกลือแร่เข้าสู่กระแสเลือดจะทำให้น้ำระหว่างเซลล์เข้าสู่กระแสเลือด ดังนั้นความเข้มข้นของเกลือในเลือดจึงลดลง น้ำและเกลือส่วนเกินจะถูกลบออกโดยไต การลดลงของน้ำในเนื้อเยื่อซึ่งสะท้อนไปยังศูนย์ประสาททำให้เกิดความกระหาย
กิจกรรมที่สำคัญตามปกติของร่างกายมนุษย์สามารถดำเนินการได้เฉพาะกับคุณสมบัติบางอย่างของของเหลวระหว่างเซลล์และสิ่งของคั่นระหว่างหน้า ในสภาพแวดล้อมที่คงที่นี้ ความสมดุลของกรด-เบสมีบทบาทสำคัญ ซึ่งปฏิกิริยาของเลือด น้ำเหลือง และของเหลวอื่นๆ ในร่างกายใกล้เคียงกับความเป็นกลาง รักษาสมดุลกรดเบสโดย ระบบที่ซับซ้อนหน่วยงานกำกับดูแลรวมกันเป็นศูนย์เดียว ระบบประสาท. สารควบคุมดังกล่าว ได้แก่ ระบบบัฟเฟอร์เลือด การแลกเปลี่ยนออกซิเจนและคาร์บอนไดออกไซด์ คาร์บอนไดออกไซด์และเกลือคลอไรด์ การทำงานของไต ปอด ต่อมเหงื่อ ฯลฯ
ในกระบวนการของการเปลี่ยนแปลงที่ซับซ้อนในร่างกายมนุษย์ของอาหารที่อุดมไปด้วยแคลเซียม แมกนีเซียม โซเดียมหรือโพแทสเซียม สารประกอบอัลคาไลน์สามารถเกิดขึ้นได้ แหล่งที่มาขององค์ประกอบที่เป็นด่าง ได้แก่ ผลไม้ ผัก พืชตระกูลถั่ว นมและผลิตภัณฑ์จากนม
ผลิตภัณฑ์อื่นๆ เช่น เนื้อสัตว์ ปลา ไข่ ชีส ขนมปัง ซีเรียล พาสต้า ในกระบวนการเปลี่ยนแปลงในร่างกายมนุษย์ให้สารประกอบที่เป็นกรด
ธรรมชาติของโภชนาการสามารถส่งผลต่อการเปลี่ยนแปลงความสมดุลของกรดเบสในเนื้อเยื่อของร่างกายมนุษย์ ความสมดุลของกรด-เบสมักจะเปลี่ยน > ด้านของความเป็นกรด อันเป็นผลจากการเปลี่ยนแปลงที่เฉียบแหลม
มาตรฐานสูงสุดที่อนุญาตสำหรับปริมาณเถ้าและเมื่อประเมินผลิตภัณฑ์ดังกล่าวจะกำหนดปริมาณ
โดยปกติแล้ว แนวคิดสองประการจะมีความแตกต่างกัน - "ขี้เถ้าทั้งหมด (ดิบ)" และ "เถ้าบริสุทธิ์" แนวคิดของ "เถ้าทั้งหมด" หมายถึงผลรวมของธาตุแร่หรือออกไซด์ของแร่ธาตุที่รวมอยู่ในโครงสร้างทางเคมีของผลิตภัณฑ์อาหารตลอดจนนำเข้าสู่ผลิตภัณฑ์ในระหว่างการผลิตหรือ "จับโดยบังเอิญเป็นสิ่งเจือปน "เถ้าบริสุทธิ์" หมายถึง ผลรวมของธาตุแร่หรือออกไซด์ของพวกมันโดยไม่มีสิ่งเจือปน
ปริมาณเถ้าของผลิตภัณฑ์ถูกกำหนดโดยการเผาไหม้ ในการทำเช่นนี้ ตัวอย่างจะถูกเผาอย่างระมัดระวังก่อน จากนั้นจึงเผาให้มีน้ำหนักคงที่ ปริมาณเถ้าที่เพิ่มขึ้นเมื่อเทียบกับบรรทัดฐานบ่งชี้การปนเปื้อนของผลิตภัณฑ์ด้วยทราย อนุภาคโลหะ และดิน
ในการตรวจสอบ "ขี้เถ้าบริสุทธิ์" เถ้าที่เกิดขึ้นจะได้รับการบำบัดด้วยกรดไฮโดรคลอริก 10% ในกรณีนี้ "ขี้เถ้าบริสุทธิ์" จะละลายในกรดไฮโดรคลอริก และสารตกค้างจะบ่งบอกถึงการมีอยู่ของสารอนินทรีย์จากต่างประเทศในผลิตภัณฑ์ ดังนั้น ในกรณีของการล้างมะเขือเทศที่ไม่ดีก่อนแปรรูป หรือในแป้งมันฝรั่งที่มีหัวล้างไม่เพียงพอ จะมีปริมาณขี้เถ้าเพิ่มขึ้นเนื่องจากแร่ธาตุจากภายนอกเจือปน
แคลเซียมในร่างกายมนุษย์พบได้ในเนื้อเยื่อกระดูกและฟัน - ประมาณ 99% แคลเซียมที่เหลือจะเข้าสู่กระแสเลือดในรูปของไอออนและในสถานะที่เกี่ยวข้องกับโปรตีนและสารประกอบอื่นๆ
ความต้องการแคลเซียมในแต่ละวันของผู้ใหญ่คือ 0.8-1.0 กรัม สตรีมีครรภ์และให้นมบุตรต้องการแคลเซียมเพิ่มขึ้นถึง 1.5-2 กรัมต่อวัน เช่นเดียวกับเด็กที่ร่างกายใช้แคลเซียมอย่างเข้มข้นเพื่อสร้างกระดูก การขาดแคลเซียมทำให้เกิดความผิดปกติของโครงกระดูก กระดูกเปราะบาง และกล้ามเนื้อลีบในร่างกาย แคลเซียมมีลักษณะเฉพาะที่แม้จะขาดอาหาร แต่ก็ยังถูกขับออกจากร่างกายในปริมาณที่มาก
แคลเซียมพบได้ในผลิตภัณฑ์อาหารในรูปของเกลือฟอสเฟตและออกซาเลตคลอไรด์ ร่วมกับกรดไขมัน โปรตีน ฯลฯ
สารประกอบแคลเซียมทั้งหมด ยกเว้น CaC! a แทบจะละลายได้ในน้ำ ดังนั้นจึงดูดซึมได้ไม่ดี
ร่างกายมนุษย์. สารประกอบแคลเซียมที่ไม่ละลายน้ำบางส่วนผ่านจากผลิตภัณฑ์ไปสู่สารละลายในกระเพาะอาหารภายใต้การกระทำของ ของกรดไฮโดรคลอริกน้ำย่อยในกระเพาะอาหาร. การดูดซึมแคลเซียมในผลิตภัณฑ์อาหารโดยร่างกายมนุษย์ขึ้นอยู่กับการมีฟอสเฟต ไขมัน สารประกอบแมกนีเซียม ฯลฯ ในอาหารเป็นอย่างมาก ดังนั้นการดูดซึมแคลเซียมจะสูงสุดเมื่ออัตราส่วนของแคลเซียมและฟอสฟอรัส I ในอาหาร ; 1.5 หรือ 1: 2 ปริมาณฟอสฟอรัสในอาหารที่เพิ่มขึ้นตามอัตราส่วนที่ระบุทำให้การดูดซึมแคลเซียมลดลงอย่างรวดเร็ว แมกนีเซียมส่วนเกินยังส่งผลเสียต่อการดูดซึมแคลเซียมโดยร่างกายมนุษย์ สารประกอบแคลเซียมที่มีกรดอิโนซิทอลฟอสฟอริกซึ่งพบได้ในปริมาณมากในเมล็ดธัญพืชและผลิตภัณฑ์จากการแปรรูป
วิตามินดีมีบทบาทสำคัญในการดูดซึมแคลเซียม ซึ่งส่งเสริมการเปลี่ยนแปลงของเกลือแคลเซียมและฟอสฟอรัสจากลำไส้เข้าสู่กระแสเลือดและการสะสมในกระดูกในรูปของแคลเซียมฟอสเฟต
ปริมาณแคลเซียมในผลิตภัณฑ์อาหารบางชนิดมีดังนี้ (มก.%): ในเนื้อไม่ติดมัน - 7; ในไข่ - 54; ในนม - 118; ในชีส - 930; ในชีสกระท่อม - 140; ในข้าวโอ๊ต - 65; ในแป้งสาลี - 15; ในข้าว - 9; ในแอปเปิ้ล - 7; ในส้ม - 45; ในวอลนัท -89; ในหัวบีท - 29; ในกะหล่ำดอก - 89; ในกะหล่ำปลีขาว - 45; ในแครอท - 56; ในมันฝรั่ง - 14. จากข้อมูลข้างต้น จะเห็นได้ว่าแหล่งแคลเซียมที่สำคัญที่สุดสำหรับมนุษย์คือผลิตภัณฑ์จากนม แคลเซียมในผลิตภัณฑ์นม เช่นเดียวกับผักและผลไม้ เป็นสารประกอบที่ย่อยง่าย
แมกนีเซียมในร่างกายมนุษย์มีแคลเซียมน้อยกว่า 30-35 เท่า แต่มีความสำคัญมาก แมกนีเซียมส่วนใหญ่พบได้ในเนื้อเยื่อกระดูก แมกนีเซียมมีบทบาทพิเศษในพืชที่มีคลอโรฟิลล์ซึ่งเป็นส่วนหนึ่งของโมเลกุลคลอโรฟิลล์ เช่นเดียวกับแคลเซียม แมกนีเซียมจะสร้างสารประกอบที่ละลายได้เพียงเล็กน้อย แมกนีเซียมจะดูดซึมได้ยากเป็นพิเศษเมื่อมีไอออน LO$
ปริมาณแมกนีเซียมในผลิตภัณฑ์อาหารบางชนิดมีดังนี้ (mg%): ในถั่ว - 139; ในข้าวโอ๊ต - 133; ในถั่ว - 107; ในข้าวฟ่าง - 87; ในขนมปังข้าวสาลี - 30; ในมันฝรั่ง - 28; ในแครอท - 21; ในกะหล่ำปลีขาว -! Anna - 12; ในแอปเปิ้ล - 8; ในมะนาว - 7; ในเนื้อ - 15; ในไข่ - 11; ในนม - 12. ดังนั้นแมกนีเซียม 2 * 35 จึงถูกพบในปริมาณที่ใหญ่ที่สุดในธัญพืชและพืชตระกูลถั่ว
ความต้องการแมกนีเซียมสำหรับผู้ใหญ่คือ 400 มก. ต่อวัน
โซเดียมมีมากในอาหาร โดยเฉพาะผลิตภัณฑ์จากสัตว์ แหล่งโซเดียมหลักสำหรับร่างกายมนุษย์คือ NaCt (เกลือทั่วไป) โซเดียมมีบทบาทสำคัญในกระบวนการเผาผลาญภายในเซลล์และเนื้อเยื่อ ประมาณ 90% ของความดันออสโมติกของพลาสมาในเลือดขึ้นอยู่กับเนื้อหาของ NaCl ในนั้น โดยปกติ โซเดียม 3.3 กรัมจะละลายในพลาสมาเลือดมนุษย์หนึ่งลิตร แนซี! นอกจากนี้ยังมีบทบาทสำคัญในการควบคุมการเผาผลาญน้ำของร่างกาย โซเดียมไอออนทำให้เกิดการบวมของเนื้อเยื่อคอลลอยด์ ดังนั้นจึงมีส่วนในการกักเก็บน้ำในร่างกาย จากร่างของ NaC! ขับออกทางปัสสาวะและเหงื่อเป็นหลัก ด้วยการทำงานและการบริโภคของเหลวที่เพิ่มขึ้น คนๆ หนึ่งจะสูญเสียเหงื่อมากถึง 3-5 ลิตร ซึ่งเป็นน้ำ 99.5% ในส่วนที่แห้งของเหงื่อ ส่วนประกอบหลักคือ NaGI
เกลือแกงซึ่งเข้าสู่ร่างกายมนุษย์ด้วยอาหารช่วยเติมเต็มการบริโภค NaCI ในเลือดและใช้เพื่อสร้างกรดไฮโดรคลอริกในน้ำย่อยรวมทั้งเพื่อสังเคราะห์ NaHCO3 โดยต่อมตับอ่อน การปรากฏตัวของ NaHCO3 อธิบายปฏิกิริยาอัลคาไลน์ของน้ำตับอ่อน ซึ่งจำเป็นสำหรับการสลายโปรตีนในอาหารโดยเอนไซม์ทริปซิน
ความต้องการโซเดียมต่อวันสำหรับผู้ใหญ่คือ 4-6 กรัมซึ่งสอดคล้องกับเกลือแกง 10-15 กรัม อาหารปกติของประชากรมีโซเดียมเพียงพอเนื่องจากเกลือแกงถูกเติมลงในอาหาร
โพแทสเซียมมีอยู่ตลอดเวลาและมีอยู่ในผลิตภัณฑ์อาหารในปริมาณมาก โดยเฉพาะจากพืช ในขี้เถ้าของพืช บางครั้งมีโพแทสเซียมมากกว่า 50% ของมวล
ในร่างกายมนุษย์ โพแทสเซียมเกี่ยวข้องกับปฏิกิริยาของเอนไซม์ การก่อตัวของระบบบัฟเฟอร์ที่ป้องกันการเปลี่ยนแปลงในปฏิกิริยาของสิ่งแวดล้อม โพแทสเซียมลดลง
ความสามารถในการกักเก็บน้ำของโปรตีน ลด hydro- (bility) ของโปรตีน และด้วยเหตุนี้จึงส่งเสริมการขับน้ำและโซเดียมออกจากร่างกาย ดังนั้น โพแทสเซียมจึงถือได้ว่าเป็นโซเดียมในทางสรีรวิทยา
ความต้องการโพแทสเซียมของผู้ใหญ่ต่อวันคือ 3-5 กรัม
เหล็กมีการกระจายอย่างกว้างขวางในธรรมชาติ โดยทั่วไปแล้ว อาหารจากธรรมชาติเกือบทั้งหมดมีธาตุเหล็ก แต่มีในปริมาณเล็กน้อย
ในสิ่งมีชีวิตของมนุษย์และสัตว์ ธาตุเหล็กเป็นส่วนหนึ่งของสารประกอบอินทรีย์ที่สำคัญที่สุด - ฮีโมโกลบินในเลือด, ไมโอโกลบิน, เอ็นไซม์บางชนิด - คาตาเลส, เปอร์ออกซิเดส, ไซโตโครมออกซิเดส ฯลฯ ฮีโมโกลบินในเลือดประกอบด้วย 2A ซึ่งเป็นธาตุเหล็กของร่างกาย พบธาตุเหล็กจำนวนมากในม้ามและตับ ธาตุเหล็กมีความสามารถในการสะสมในร่างกาย เฮโมโกลบินในเลือดจะถูกทำลายในช่วงชีวิต และธาตุเหล็กที่ปล่อยออกมาในกรณีนี้ ร่างกายสามารถนำกลับมาใช้ใหม่เพื่อสร้างฮีโมโกลบินได้
ธาตุเหล็กซึ่งเป็นส่วนหนึ่งของผักและผลไม้นั้นร่างกายดูดซึมได้ดี ในขณะที่ธาตุเหล็กในผลิตภัณฑ์จากธัญพืชส่วนใหญ่อยู่ในรูปแบบที่ร่างกายไม่สามารถย่อยได้
ความต้องการรายวันของต่อมผู้ใหญ่ของมนุษย์คือ 15 มก.
l o r เป็นส่วนหนึ่งของอาหารธรรมชาติในปริมาณเล็กน้อย ผลิตภัณฑ์จากผักมีคลอรีนน้อย ในขณะที่ผลิตภัณฑ์จากสัตว์มีคลอรีนมากกว่าเล็กน้อย ดังนั้นปริมาณคลอรีนในเนื้อวัวคือ 76 มก.% ในนม - 106 ในไข่ -
37106 ในชีส - 880 ในข้าวฟ่าง - 19 ในมันฝรั่ง - 54 ในแอปเปิ้ล - 5 มก.%
เนื้อหาของคลอรีนมีความสำคัญในเลือดและของเหลวอื่นๆ ในร่างกาย เช่นเดียวกับในผิวหนัง ปอด และไต คลอรีนในร่างกายอยู่ในสถานะแตกตัวเป็นไอออนในรูปของไอออนของเกลือของโซเดียม โพแทสเซียม แคลเซียม แมกนีเซียม แมงกานีส สารประกอบของคลอรีนในผลิตภัณฑ์อาหารสามารถละลายได้สูงและดูดซึมได้ง่ายในลำไส้ของมนุษย์ คลอรีนแอนไอออน ร่วมกับโซเดียมไอออนบวก มีบทบาทสำคัญในการสร้างและควบคุมแรงดันออสโมติกของเลือดและของเหลวอื่นๆ ในร่างกาย เกลือคลอรีนทำให้เกิดกรดไฮโดรคลอริกโดยเยื่อบุกระเพาะอาหาร
ความต้องการคลอรีนหลักคือโซเดียมคลอไรด์ซึ่งเติมลงในอาหารในรูปของเกลือ
ปริมาณโซเดียมคลอไรด์ในร่างกายมนุษย์มักจะอยู่ที่ 10-15 กรัม แต่เมื่อรับประทานอาหารที่อุดมไปด้วยเกลือคลอรีน ปริมาณคลอรีนในร่างกายมนุษย์จะมีปริมาณสูงขึ้น ความต้องการคลอรีนต่อวันของมนุษย์คือ 5-7 กรัม
กำมะถันพบได้ในปริมาณสูงสุดในผลิตภัณฑ์จากธัญพืช พืชตระกูลถั่ว ผลิตภัณฑ์จากนม เนื้อสัตว์ ปลา และโดยเฉพาะไข่ มันเป็นส่วนหนึ่งของโปรตีนเกือบทั้งหมดของร่างกายมนุษย์และมีกรดอะมิโนมากมาย - ซิสทีนเมไทโอนีน การแลกเปลี่ยนกำมะถันในร่างกายส่วนใหญ่เป็นการเปลี่ยนแปลงเป็นกรดอะมิโนที่ระบุ นอกจากนี้ยังเกี่ยวข้องกับการก่อตัวของวิตามิน Bg (ไทอามีน) อินซูลิน และสารประกอบอื่นๆ มีกำมะถันจำนวนมากในโปรตีนของเนื้อเยื่อที่รองรับเช่นในเคราตินของผมเล็บ ฯลฯ
เมื่อสารประกอบถูกออกซิไดซ์ในร่างกาย ส่วนสำคัญของกำมะถันจะถูกขับออกทางปัสสาวะในรูปของเกลือของกรดซัลฟิวริก
ความต้องการรายวันของผู้ใหญ่สำหรับกำมะถันที่มีงานปานกลางคือประมาณ 1 กรัม
ไอโอดีนมีอยู่ในร่างกายของผู้ที่มีสุขภาพแข็งแรง โดยมีน้ำหนัก 70 กก. ในปริมาณประมาณ 25 มก. ครึ่งหนึ่งของจำนวนนี้อยู่ในต่อมไทรอยด์ ส่วนที่เหลืออยู่ในกล้ามเนื้อ เนื้อเยื่อกระดูก และในเลือด สารอนินทรีย์ไอโอดีนในต่อมไทรอยด์ถูกแทนที่ สารประกอบอินทรีย์- ไทรอกซิน, ไดไอโอโดไทรอกซีน, ไตรไอโอโดไทรอกซีน ไอโอดีนถูกดูดซึมโดยต่อมไทรอยด์อย่างรวดเร็ว และหลังจากป้อนเข้าไปไม่กี่ชั่วโมง มันจะกลายเป็นสารอินทรีย์
การเชื่อมต่อ สารเหล่านี้กระตุ้นกระบวนการเผาผลาญในร่างกาย เมื่อปริมาณไอโอดีนเข้าสู่ร่างกายไม่เพียงพอด้วยอาหาร กิจกรรมของต่อมไทรอยด์จะหยุดชะงักและเกิดโรคร้ายแรงที่เรียกว่าคอพอกเฉพาะถิ่น
ไอโอดีนจำนวนมากที่สุดพบได้ในผลิตภัณฑ์จากพืชและสัตว์ในพื้นที่ชายฝั่งทะเล ซึ่งมีความเข้มข้นในน้ำทะเล อากาศ และดินบริเวณชายฝั่ง ไอโอดีนน้อยสะสมในพืชและสิ่งมีชีวิตของสัตว์บนภูเขาหรือห่างไกลจากบริเวณชายฝั่งทะเลของไอโอดีน
ปริมาณไอโอดีนในผลิตภัณฑ์จากธัญพืช ผัก ปลาน้ำจืด ไม่เกิน 5-8 ไมโครกรัมต่อผลิตภัณฑ์ดิบ 100 กรัม เนื้อวัว ไข่ เนย ผลไม้ มีไอโอดีนในปริมาณที่สูงกว่า คะน้าทะเล, ปลาทะเลและน้ำมันปลามีปริมาณไอโอดีนสูงสุด ผลไม้ Feijoa ที่ปลูกบนชายฝั่งทะเลดำของจอร์เจียสะสมไอโอดีนได้ถึง 390 ไมโครกรัมต่อมวลผลไม้ 100 กรัม ซึ่งมากกว่าปริมาณธาตุนี้ในผักและผลไม้อื่นๆ
ในพื้นที่ที่ผลิตภัณฑ์อาหารมีปริมาณไอโอดีนไม่เพียงพอ โพแทสเซียมไอโอไดด์จะถูกเติมลงในเกลือแกงในอัตรา 25 กรัม K1 ต่อเกลือแกงหนึ่งตัน ด้วยอาหารปกติคนบริโภคไอโอดีน 200 ไมโครกรัมต่อวันด้วยเกลือเสริมไอโอดีน อย่างไรก็ตาม เมื่อเก็บเกลือเสริมไอโอดีน ไอโอดีนจะค่อยๆ หายไป ดังนั้นหลังจากผ่านไป 6 เดือนเกลือเสริมไอโอดีนก็จะขายเป็นเกลือแกงธรรมดา
ความต้องการไอโอดีนของมนุษย์ในแต่ละวันคือ 100-260 ไมโครกรัม
ฟลูออรีนมีบทบาทสำคัญในกระบวนการพลาสติกระหว่างการก่อตัวของเนื้อเยื่อกระดูกและเคลือบฟัน ฟลูออรีนปริมาณมากที่สุดมีความเข้มข้นในกระดูก - 200-490 มก./กก. และฟัน - 240-560 มก./กก.
น้ำดูเหมือนจะเป็นแหล่งหลักของฟลูออไรด์ในร่างกายมนุษย์ โดยฟลูออไรด์ของ Doda ดูดซึมได้ดีกว่าฟลูออไรด์ในอาหาร ปริมาณฟลูออรีนในน้ำดื่มมีตั้งแต่ 1 ถึง 1.5 มก./ลิตร การขาดฟลูออรีนในน้ำมักจะส่งผลกระทบ
39nne กับการพัฒนาของโรคฟันที่เรียกว่าฟันผุ ฟลูออรีนส่วนเกินในน้ำทำให้เกิดฟลูออโรซิสซึ่งโครงสร้างปกติของฟันถูกรบกวน คราบปรากฏบนเคลือบฟันและความเปราะบางของฟันเพิ่มขึ้น เด็กโดยเฉพาะอย่างยิ่งต้องทนทุกข์ทรมานจากการขาดฟลูออรีนหรือส่วนเกิน
ความต้องการฟลูออรีนในแต่ละวันของมนุษย์ยังไม่ได้รับการจัดตั้งขึ้น เป็นที่เชื่อกันว่าปริมาณฟลูออไรด์ที่เหมาะสมในน้ำดื่มเพื่อสุขภาพควรอยู่ที่ 0.5-1.2 มก./ลิตร
ทองแดงในร่างกายของสัตว์พร้อมกับธาตุเหล็กมีบทบาทสำคัญในกระบวนการสร้างเม็ดเลือด กระตุ้นกระบวนการออกซิเดชันและสัมพันธ์กับการเผาผลาญของธาตุเหล็ก มันเป็นส่วนหนึ่งของเอนไซม์ (แลคเตส, แอสคอร์เบตออกซิเดส, ไซโตโครมออกซิเดส ฯลฯ ) เป็นส่วนประกอบโลหะ
ในพืช ทองแดงช่วยเพิ่มกระบวนการออกซิเดชัน เร่งการเจริญเติบโต และเพิ่มผลผลิตของพืชหลายชนิด
ในปริมาณเล็กน้อยที่พบทองแดงในผลิตภัณฑ์จากธรรมชาติ ทองแดงจะไม่เป็นอันตรายต่อร่างกายมนุษย์ แต่ปริมาณทองแดงที่สูงอาจทำให้เกิดพิษได้ ดังนั้นการรับประทานทองแดง 77-120 มก. พร้อมกันอาจทำให้เกิดอาการคลื่นไส้ อาเจียน และท้องร่วงในบางครั้ง ดังนั้นเนื้อหาของทองแดงในผลิตภัณฑ์อาหารจึงถูกควบคุมโดยข้อบังคับปัจจุบันของกระทรวงสาธารณสุขของสหภาพโซเวียต ต่อ 1 กิโลกรัมของผลิตภัณฑ์ขึ้นอยู่กับเนื้อหาของของแข็งในนั้นอนุญาตให้ใช้ทองแดงตั้งแต่ 5 ถึง 30 มก. ดังนั้นในการวางมะเขือเทศเข้มข้นปริมาณทองแดงไม่ควรเกิน 30 มก. / กก. ในน้ำซุปข้นมะเขือเทศ - 15-20 ในผักกระป๋อง - 10 ในแยมและแยมผิวส้ม - 10 ในผลไม้แช่อิ่ม - 5 มก. / กก.
ทองแดงสามารถเข้าไปในผลิตภัณฑ์อาหารได้ในระหว่างการผลิต - จากชิ้นส่วนทองแดงของอุปกรณ์ เมื่อทำการบำบัดไร่องุ่นด้วยยาฆ่าแมลงที่มีทองแดง ฯลฯ
ความต้องการทองแดงต่อวันสำหรับผู้ใหญ่คือ 2 มก.
สังกะสีพบได้ในเนื้อเยื่อของสัตว์และพืชทุกชนิด ด้วยการขาดธาตุสังกะสีในร่างกายของหญิงสาว
ในพืชการเจริญเติบโตของพวกมันล่าช้าและด้วยความบกพร่องในดินจึงเกิดโรคพืชหลายชนิดซึ่งมักจะนำไปสู่ความตาย
สังกะสีเป็นส่วนหนึ่งของเอ็นไซม์หลายชนิด และบทบาทของมันในโมเลกุลของเอนไซม์คาร์บอนิกแอนไฮไดเรส ซึ่งเกี่ยวข้องกับการจับและการขับคาร์บอนไดออกไซด์ออกจากร่างกายของสัตว์นั้นมีความสำคัญเป็นพิเศษ สังกะสีมีความจำเป็นต่อการทำงานปกติของฮอร์โมนต่อมใต้สมอง ต่อมหมวกไต และตับอ่อน ยังส่งผลต่อการเผาผลาญไขมัน เพิ่มการสลายไขมัน และป้องกันไขมันพอกตับ
สังกะสีในอาหารในปริมาณมากอาจทำให้เกิดพิษได้ อาหารที่เป็นกรดและไขมันจะละลายสังกะสีที่เป็นโลหะ ดังนั้นจึงไม่ยอมรับการปรุงอาหารหรือเก็บอาหารในอุปกรณ์หรือเครื่องใช้สังกะสี พิษของสังกะสีคล้ายกับพิษของทองแดง แต่เด่นชัดกว่าและมาพร้อมกับอาการแสบร้อนและปวดในปากและท้อง อาเจียน ท้องร่วง และหัวใจอ่อนแอ อนุญาตให้ใช้เครื่องใช้สังกะสีสำหรับเก็บน้ำดื่มเย็นเท่านั้น เนื่องจากในกรณีนี้ความสามารถในการละลายของสังกะสีจะเล็กน้อย
ความต้องการสังกะสีต่อวันสำหรับผู้ใหญ่คือ 10-15 มก. ความต้องการสังกะสีเพิ่มขึ้นในช่วงการเจริญเติบโตและวัยแรกรุ่น ด้วยอาหารปกติบุคคลจะได้รับสังกะสีในปริมาณที่เพียงพอจากอาหาร
ตะกั่วพบได้ในผลิตภัณฑ์จากสัตว์และพืชในปริมาณที่น้อยมาก ดังนั้นในแอปเปิ้ล ลูกแพร์ องุ่น สตรอเบอร์รี่ ปริมาณตะกั่วประมาณ 0.1 มก. ต่อผลิตภัณฑ์ 1 กิโลกรัมในนม - 0.8 ในเนื้อสัตว์ - 0.05 ในปลาสเตอร์เจียน - 0.06 มก. ต่อ 1 กก.
ตะกั่วเป็นโลหะที่เป็นพิษสำหรับมนุษย์ มีความสามารถในการสะสมในร่างกาย ส่วนใหญ่อยู่ในตับ และทำให้เกิดพิษเรื้อรังอย่างรุนแรง
ด้วยการใช้ตะกั่ววันละ 2-4 มก. กับอาหาร อาจตรวจพบสัญญาณของพิษตะกั่วหลังจากผ่านไปสองสามเดือน
41 อาหารปนเปื้อนด้วยตะกั่วอาจมาจากภาชนะ บัดกรี เคลือบ อุปกรณ์ และยาฆ่าแมลงที่มีตะกั่ว ส่วนใหญ่มักเกิดพิษจากตะกั่วเมื่ออาหารถูกจัดเก็บไว้ในภาชนะดินเผาที่เคลือบด้วยตะกั่วเคลือบไม่ดี
เนื่องจากมีความเป็นพิษสูง ไม่อนุญาตให้มีสารตะกั่วในผลิตภัณฑ์อาหาร
ดีบุกมีอยู่ในผลิตภัณฑ์อาหารในปริมาณเล็กน้อย ดังนั้นพบดีบุก 0.14 มก./กก. ในตับของโคและแกะผู้ 0.003 ในไต 0.63 ในปอด และ 0.019 มก./กก. ในสมอง
ดีบุกไม่ใช่โลหะที่เป็นพิษเช่นตะกั่ว สังกะสีหรือทองแดง ดังนั้นจึงอนุญาตให้ใช้ในปริมาณที่จำกัดในอุปกรณ์ของสถานประกอบการด้านอาหาร เช่นเดียวกับการชุบผิวดีบุกซึ่งเตรียมกระป๋องดีบุกไว้เพื่อป้องกันการกัดกร่อน อย่างไรก็ตาม บ่อยครั้งในระหว่างการเก็บรักษาอาหารกระป๋องในกระป๋องเป็นเวลานาน มวลของผลิตภัณฑ์มีปฏิสัมพันธ์กับการเคลือบดีบุกของกระป๋อง อันเป็นผลมาจากการที่เกลือดีบุกของกรดอินทรีย์ก่อตัวขึ้น กระบวนการนี้ใช้งานได้ดีเป็นพิเศษเมื่อมีผลิตภัณฑ์ที่มีความเป็นกรดสูงในผลไม้กระป๋อง ปลากระป๋อง และผักใน ซอสมะเขือเทศและอื่นๆ ในระหว่างการเก็บรักษาในระยะยาวเนื้อหาของกระป๋องในอาหารกระป๋องจะเพิ่มขึ้นอย่างมาก ปริมาณดีบุกจะเพิ่มขึ้นอย่างรวดเร็วโดยเฉพาะในผลิตภัณฑ์ที่อยู่ในกระป๋องโลหะเปิดที่เคลือบด้วยดีบุก
เพื่อเพิ่มการป้องกันกระป๋องจากการกัดกร่อน เคลือบพิเศษทนกรดหรือเคลือบเพิ่มเติมกับพื้นผิวของดีบุก หรือสร้างฟิล์มบาง ๆ ของดีบุกออกไซด์เสถียรบนผิวของดีบุก
แมงกานีสมีการกระจายอย่างกว้างขวางในผลิตภัณฑ์จากสัตว์และพืช มีส่วนสำคัญในการสร้างเอ็นไซม์ การสร้างกระดูก กระบวนการสร้างเม็ดเลือด และกระตุ้นการเจริญเติบโต ในพืช แมงกานีสช่วยเพิ่มกระบวนการสังเคราะห์แสงและการก่อตัวของกรดแอสคอร์บิก
ผลิตภัณฑ์จากพืชส่วนใหญ่มีแมงกานีสมากกว่าผลิตภัณฑ์จากสัตว์ ดังนั้นเนื้อหาของแมงกานีสในผลิตภัณฑ์จากธัญพืชถึง 1-15 มก. ต่อ 1 กก. ในใบ
ผัก - 10-20 ในผลไม้ - 0.5-1 ในนม - 0.02-0.03 ในไข่ - 0.1-0.2 ในตับของสัตว์ - 2.65-2.98 มก. ต่อ 1 กก.
ด้วยการขาดแมงกานีสในดิน พืชเริ่มป่วยและพัฒนาได้ไม่ดี ผลผลิตของผลไม้ ผัก และพืชผลอื่นๆ ลดลง การเติมไมโครปุ๋ยที่มีแมงกานีสลงในดินช่วยเพิ่มผลผลิต
ความต้องการรายวันสำหรับผู้ใหญ่สำหรับแมงกานีสคือ 5-10 มก. ต่อวัน
ไอโซโทปกัมมันตภาพรังสีมีอยู่ในร่างกายมนุษย์ซึ่งเข้าและออกจากร่างกายอย่างต่อเนื่อง มีความสมดุลระหว่างการบริโภคสารกัมมันตรังสีเข้าสู่ร่างกายและการกำจัดออกจากร่างกาย ผลิตภัณฑ์อาหารทั้งหมดประกอบด้วยไอโซโทปกัมมันตภาพรังสีของโพแทสเซียม (K40), คาร์บอน (C14), ไฮโดรเจน (H3) และเรเดียมด้วยผลิตภัณฑ์ที่สลายตัว
ความเข้มข้นสูงสุดอยู่ที่โพแทสเซียม (K40) ไอโซโทปมีส่วนร่วมในการเผาผลาญพร้อมกับไอโซโทปที่ไม่มีกัมมันตภาพรังสี
เป็นที่เชื่อกันว่าในช่วงเวลาทางธรณีวิทยาที่ใกล้ที่สุดไม่มีการเปลี่ยนแปลงความรุนแรงของรังสีบนโลกมากนักดังนั้นในสัตว์และ ดอกไม้พัฒนาภูมิคุ้มกันในระดับหนึ่งของรังสีเหล่านี้ แต่สิ่งมีชีวิตมีความไวต่อความเข้มข้นสูง ความเข้มข้นเล็กน้อยช่วยเพิ่มการเจริญเติบโตของสิ่งมีชีวิตความเข้มข้นขนาดใหญ่ทำให้เกิดการปรากฏตัวของอนุมูลอิสระอันเป็นผลมาจากการละเมิดกิจกรรมที่สำคัญของอวัยวะและเนื้อเยื่อแต่ละส่วนรวมถึงสิ่งมีชีวิตทั้งหมด
ที่ ระเบิดปรมาณูไอโซโทปกัมมันตภาพรังสีตกลงบนพื้นผิวโลก ก่อให้เกิดมลพิษต่อบรรยากาศ น้ำ ดินและพืช ไอโซโทปกัมมันตภาพรังสีเข้าสู่ร่างกายมนุษย์ผ่านทางอาหาร บรรยากาศ และน้ำ
เป็นที่ยอมรับกันว่าเมื่อผลิตภัณฑ์อาหารได้รับรังสีของไอโซโทปกัมมันตภาพรังสี อายุการเก็บรักษาจะเพิ่มขึ้น และการงอกของมันฝรั่งจะล่าช้า แต่โดยปกติ อาหารฉายรังสีอาจมีกลิ่นและรสเฉพาะ และอาจเกิดสารพิษขึ้นได้ จำเป็นต้องมีการทดลองระยะยาวเพื่อกำหนดความปลอดภัยของผลิตภัณฑ์ดังกล่าว
คำถามทดสอบ
องค์ประกอบทางเคมีอะไรเป็นธาตุอาหารหลัก?
หน้าที่ของแร่ธาตุในร่างกายมนุษย์คืออะไร?
บทบาทของแคลเซียมในร่างกายมนุษย์คืออะไร?
องค์ประกอบทางเคมีใดที่จัดเป็นธาตุติดตามและหน้าที่ของธาตุเหล่านี้ในร่างกายมนุษย์คืออะไร?
ธาตุเหล็กมีบทบาทอย่างไรในร่างกายมนุษย์และในอาหารประเภทใดที่พบ?
การขาดสารไอโอดีนในร่างกายมีผลเสียอย่างไร และจะหลีกเลี่ยงได้อย่างไร?
การแปรรูปวัตถุดิบและผลิตภัณฑ์อาหารทางเทคโนโลยีประเภทใดทำให้เกิดการสูญเสียแร่ธาตุ?
ยกตัวอย่างการทำงานร่วมกันของธาตุและวิตามินบางชนิด
คุณรู้วิธีการใดในการกำหนดเนื้อหาของมาโครและไมโครอิลิเมนต์